عدد اکسایش (oxidation number) یک اتم در یک ترکیب شیمیایی به مجموع بارهای الکتریکی ظاهری که به آن اتم نسبت داده شده است گفته می شود.

البته توجه داشته باشید که این تعریف با فرض اینکه پیوند ها یونی می باشند کاربرد دارد. در ترکیبات کووالانسی بر اساس یکسری قواعد اختیاری، اعداد اکسایش را تعیین می کنند. در واقع عدد اکسایش نحوه شکسته شدن یک پیوند شیمیایی را در طی انجام واکنش تعیین می کند. در ادامه این مقاله در نشریه جهان شیمی فیزیک به بررسی عدد اکسایش و نحوه محاسبه آن پرداخته می شود. لطفا با ما همراه باشید.
عدد اکسایش برای نخستین بار توسط چالزکی یورگنسن در هنگام مطالعه بر روی کربن بیان شد. وی یکسان نبودن کربن در دو مولکول مختلف را به اعداد اکسایش و حالت های مختلف اکسایش ربط داد. متخصصان شیمی معدنی در واکنش های اکسایش – کاهش از این اعداد استفاده می کنند. همچنین این اعداد در شیمی کوئوردینانسیون برای طبقه بندی فلزات واسطه کاربرد دارد. در شیمی آلی تفاوت کربن در مولکول های مختلف (مثلا CH۴ و C۲H۶) باعث استفاده از اعداد اکسایش شده است.
تعیین اعداد اکسایش
اعداد اكسايش در واقع نشان دهنده اینست که يك اتم در مقابل اتم های نزدیک خود در يك تركيب دارای چه مقدار بار مثبت و يا بار منفی می باشد. در پيوند های يونی، الكترون به طور كامل از يك اتم به اتم مجاور منتقل می شود. بنابراین می توان گفت که عدد اكسايش يك اتم در اين گونه پيوند ها برابر با همان تعداد الكترونی است كه جا به جا شده است.
به بیان دیگر، در یک ترکیب یونی فلزات به اندازه ظرفیت خود در ترکیب، بار مثبت و غیر فلزات نیز به اندازه ظرفیت خود بار منفی می گیرند. این بارها همان اعداد اکسایش آنها می باشد. به عنوان مثال در ترکیب یونی NaCl، اتم سدیم یک الکترون از دست می دهد (Na → Na+ + e) و دارای عدد اکسایش (۱+) و اتم کلر یک الکترون می گیرد (-Cl + e → Cl)، بنابراین دارای عدد (۱-) می باشند.
از طرفی در ترکیبات کووالانسی (كه اشتراك الكترون صورت می گيرد نه انتقال کامل الکترون)، این بارها را نسبی فرض می کنند. در واقع به كمك الكترونگاتيويته اتم ها اعداد اكسايش را تعيين می كنند. در این حالت، هر پيوند را به صورت جداگانه در نظر می گیرند، پس به اتم الكترونگاتيوتر بار منفی و به اتم الكتروپوزتيو بار مثبت نسبت می دهند. با فرض اینکه بار الکتریکی به طور کامل بین اتم های درگیر در پیوند منتقل شده است، می توان به هر اتم یک بار الکتریکی ظاهری نسبت داد. به این بار الکتریکی ظاهری و نسبی عدد اکسایش آن اتم گفته می شود.
در نتیجه می توان گفت، عدد اکسایش برابر است با تعداد الکترون های ظرفیت اتم در حالت آزاد منهای تعداد الکترون های اتم در مولکول با فرض شکستن پیوند ها به صورت یونی.
روش های تعیین اعداد اکسایش
برای تعیین اعداد اکسایش اتم ها در ترکیبات، قوانینی وجود دارد که کار را راحت می کند. بنابراین با پیروی از این قوانین می توان عدد اکسایش اتم ها در ترکیبات را تعیین کرد. برای تعیین کردن اعداد اکسایش ترکیبات به ویژه ترکیبات کووالانسی دو راه مختلف وجود داد که عبارتند از :
١- استفاده از ساختار الکترون – نقطه ای
٢- استفاده از قواعد
استفاده از ساختار الکترون – نقطه ای
ساختار الکترون – نقطه ای در مواردی کاربرد دارد که تعداد اتم ها در ترکیب مورد نظر زیاد باشد. همچنین زمانیکه از یک عنصر، چند اتم در ترکیب مورد نظر (مثلا در ترکیبات آلی اتم های کربن با اعداد اکسایش مختلف وجود دارند) باشد از این روش بهره می بریم. برای استفاده از این روش باید چهار مرحله زیر را دنبال کنید.
١- ابتدا ساختار الکترون ـ نقطهای ترکیب مورد نظر رسم می شود.
۲- تمام پیوند های تشکیل شده در ترکیب، یونی فرض می گردد. بنابراین جفت الکترون پیوندی را به اتم با الکترونگاتیویته بیشتر اختصاص می دهند. اگر پیوند، بین اتم های جور هسته تشکیل شده باشد، به دلیل الکترونگاتیوی یکسان اتم های دو سر پیوند، به هر اتم تنها یکی از الکترون های پیوندی را نسبت می دهند.
٣- تمام الکترون های غیر پیوندی بر روی هر اتم باقی می ماند.
۴- در نهایت عدد اکسایش را با کمک رابطه (عدد اکسایش هر اتم برابر است با عدد یکان شماره گروه منهای تعداد الکترون های لایه والانس نسبت داده شده به آن اتم) بدست می آورند.
برای اینکه مطلب فوق را بهتر متوجه شوید به عنوان مثال عدد اکسایش اتم های موجود در مولکول هیدروژن پراکسید (H۲O۲) محاسبه شده است.
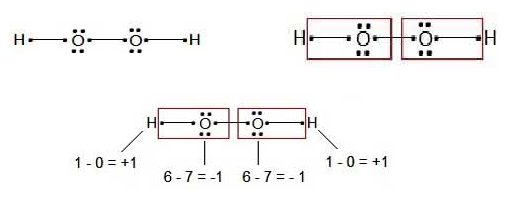
قواعد تعیین عدد اکسایش
از این روش معمولا در ترکیبات معدنی و یا ترکیباتی که تعداد اتم های آنها کم باشد استفاده می شود. دانستن مجموعه نکات زیر مهم و الزامی می باشد.
۱- عدد اکسایش عنصرها در حالت آزاد، اتم های ترکیب نشده و یا اتم هایی که فقط عناصر مولکولی تشکیل داده اند برابر با صفر است. به عنوان مثال اعداد مربوط به P۴ ،Cu ،S۸ ،H۲ و O۲ صفر می باشد.
۲- عدد اکسایش یون های تک اتمی برابر با بار یون می باشد. برای مثال عدد مس در کاتیون +Cu برابر با ۱+ است.
۳- اعداد اکسایش فلزات همواره مثبت و برابر با ظرفیت آنها می باشد. به عنوان مثال اعداد اکسایش فلزات گروه اول و دوم جدول تناوبی به ترتیب برابر با ۱+ و ۲+ می باشند.
۴- اعداد اکسایش در نافلزات اصلی می توانند از شماره گروه تا شماره گروه منهای هشت تغییر کند. مثلا عدد اکسایش اتم نیتروژن که متعلق به گروه پنج اصلی است، می تواند در محدوده ۳- تا ۵+ تغییر کند.
۵- عدد اکسایش هیدروژن معمولا برابر با ۱+ می باشد. اما در هیدرید های فلزی برابر با ۱- می شود. به ترکیباتی که دارای یون هیدرید (–H) باشند، ترکیب هیدرید گفته می شود مانند KH.
۶- عدد اکسایش فلوئور (الکترونگاتیوترین عنصر) در تمام ترکیبات فلوردار (به استثنای F۲ ) همواره برابر با ۱- می باشد.
۷- عدد اکسایش اکسیژن معمولا برابر با ۲- می باشد. در مورد اکسیژن چند مورد استثنا هم وجود دارد که جداگانه به آن می پردازیم.
۸- عدد اکسایش سایر هالوژن ها (Cl، Br و I) در اغلب ترکیبات برابر با ۱- می باشد. اما اگر با عناصری که الکترونگاتیویته بیشتری دارند، پیوند تشکیل دهند می توانند اعداد اکسایش ۱+، ۳+، ۵+ و ۷+ نیز داشته باشند.
عناصری وجود دارند که همیشه در ترکیبات خود فقط یک نوع عدد را نشان می دهند. این عناصر به همراه عدد اکسایش آن ها عبارتند از : فلزات گروه یک اصلی (۱+)، فلزات گروه دو اصلی (۲+)، فلوئور (۱-)، آلومینیوم (۳+)، اسکاندیم (۳+)، روی (۲+) و نقره (۱+).
اعداد اکسایش اکسیژن
همانطور که بیان شد تقریبا در بیشتر موارد، عدد اکسایش اتم اکسیژن ۲- می باشد. موارد استثنا در ادامه لیست شده اند.
۱- عدد اکسایش اکسیژن در پراکسید ها، برابر با ۱- می باشد. در این ترکیبات پیوند یگانه اکسیژن – اکسیژن وجود دارد، بنابراین دو اتم اکسیژن هم ارز می باشند. در نتیجه هر یک از دو اتم اکسیژن باید عددی برابر با ۱- داشته باشند تا مجموع بار آنها برابر با بار یون شود.
۲- عدد اکسایش اکسیژن در سوپر اکسید ها، برابر با ۰/۵- می باشد. ترکیب سوپر اکسید به ترکیبی گفته می شود که در آن رادیکال −O۲ وجود دارد. لازم به ذکر است که این اعداد همواره اعدادی صحیح می باشند. اما میانگین اعداد اکسایش چند اتم از یک عنصر ممکن است اعشاری باشد. در سوپراکسید ها عدد اکسایش یک اکسیژن برابر با ۱- و عدد اتم دیگر برابر با صفر است، پس میانگین اعداد ۱/۲- می شود.
۳- اگر اکسیژن با اتم فلوئور پیوند دهد، از آن جهت که فلوئور الکترونگاتیوترین عنصر جدول تناوبی است، بنابراین عدد اکسایش اکسیژن برابر با ۲+ خواهد بود (مثلا مولکول OF۲).
۴- در مولکول O۲F۲ عدد اکسایش اکسیژن برابر با ۱+ می باشد.
۵- در یون +O۲ که به نام دیوکسیژنیل مشهور است، عدد اکسایش اکسیژن برابر با ۱/۲+ است.
عدد اکسایش عناصر واسطه
عناصر فلزات واسطه توانایی بدست آوردن اعداد اکسایش متفاوت را دارند. به عنوان مثال معمول ترین اعداد در منگنز برابر با ۲+، ۳+، ۴+، ۶+ و ۷+ می باشد. این تنوع در عناصر میانی سری عناصر واسطه بیشترین مقدار است. برای عناصر واسطه نیز همانند سایر عناصر جدول تناوبی، پایین ترین درجه اکسایش برابر با صفر است (در عناصر آزاد که با عنصر دیگری ترکیب نشده اند). علاوه بر آن این عدد در فلزات واسطه خارجی، از صفر تا زمانیکه مجموع الکترون های اوربیتال ها ns و (n-1)d شود تغییر می کند. در واقع داریم:
مجموع الکترون های ns و (n-1)d ≥ اعداد اکسایش فلزات واسطه خارجی ≥ صفر
عدد اکسایش ترکیبات خنثی و باردار
مجموع اعداد اکسایش اتم ها در یک ترکیب خنثی برابر با صفر می باشد، زیرا ترکیبات از نظر بار الکتریکی خنثی می باشند. درحالیکه این اعداد در یک یون برابر با بار یون است. با کمک این دو اصل می توان عدد اکسایش اتم مورد نظر را محاسبه کرد. به عنوان نمونه عددهای اتم های کلر و کروم در دو ترکیب زیر بدست آمده است.
HClO۳ → (+۱) +X + 3(-2) =0 X =+5
Cr۲O۷ ۲-→ ۲(X) +7(-2) = -2 X =+6
اعداد اکسایش کربن در ترکیبات آلی
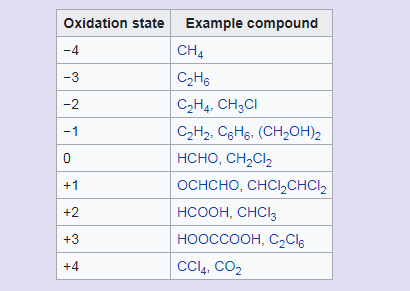
اگر اتم کربن به اتم های F، O، N و Cl پیوند داده باشد، به دلیل الکترونگاتیویته کمتر اتم کربن نسبت به این اتم ها، به ازای هر پیوند یک ۱+ برای اتم کربن در نظر می گیریم. درحالیکه اگر کربن با هر عنصر دیگری پیوند داده باشد، به ازای هر پیوند یک ۱- برای اتم کربن در نظر گرفته می شود. ذکر این نکته خالی از لطف نیست که بدانید عدد اکسایش اتم کربن موجود در متانول برابر با ۲-، در تمام انواع الکل های نوع اول ۱-، در الکل های نوع دوم برابر با صفر و در الکل های نوع سوم ۱+ می باشد. به طور کلی اعداد اکسایش اتم کربن در ترکیبات در بازه ۴+ تا ۴- قرار دارد. در جدول زیر نمونه هایی از این اعداد مربوط به اتم های کربن را مشاهده می کنید.
محاسبه عدد اکسایش در کمپلکس ها
برای پیدا کردن عدد اکسایش اتم مرکزی در کمپلکس ها، پيدا کردن بار ليگاند ها مهم می باشد. اگر کمپلکس از لحاظ الكتريكی خنثی باشد، بنابراین مجموع اعداد تمام ليگاند ها و اتم مرکزی صفر می باشد. در نتیجه با دانستن بار ليگاند ها، می توان عدد اکسايش اتم مرکزی را محاسبه کرد. همانند ترکیبات باردار، در يك کمپلکس باردار، مجموع اعداد اكسايش ليگاند ها و اتم مرکزی برابر با بار الكتريكی آن يون خواهد بود. مثلا عدد اکسايش اتم مرکزی پلاتين در کمپلکس pt(NH۳)۴ برابر با ۴+ می باشد.
عدد اکسایش شیمی دوازدهم
عدد اکسیداسیون یک مفهوم اساسی در شیمی است که نشان دهنده درجه اکسیداسیون یک اتم در یک ترکیب است. عدد اکسایش تعداد الکترون های از دست رفته یا به دست آمده را منعکس می کند و ما را در پیش بینی واکنش های شیمیایی راهنمایی می کند. درک اعداد اکسیداسیون می تواند اسرار پیوندهای شیمیایی و واکنش ها را باز کند.
اتم ها از طریق دادن و پذیرش الکترون هایی با بار منفی ترکیب میشوند، پیوند یونی تشکیل میدهند، یا الکترونها را به اشتراک میگذارند و پیوند کووالانسی تشکیل میدهند. به طور معمول، پیوندهای یونی بین فلزات و غیر فلزات تشکیل می شود، در حالی که پیوندهای کووالانسی فقط بین غیر فلزات تشکیل می شوند. عدد اکسیداسیون یک اتم نشاندهنده تعداد الکترونهایی است که به اتمهای دیگر داده، پذیرفته شده یا با آنها به اشتراک گذاشته شده است، و زمانی که الکترونها را از دست داده یا به اشتراک گذاشته باشد، مثبت و زمانی که الکترونهای اتم دیگری را به دست آورده یا به اشتراک گذاشته، منفی خواهد بود.
در اصل، اکسیداسیون به معنای ترکیب با اکسیژن بود. فرآیند مخالف، حذف اکسیژن، به عنوان کاهش شناخته شد. به عنوان مثال، هنگامی که کلسیم با اکسیژن ترکیب می شود، اکسیژن دو الکترون را از کلسیم خارج می کند و بار ۲- را به دست می آورد و کلسیم با بار ۲+ باقی می ماند.
اکسیداسیون نیازی به اکسیژن ندارد. امروزه اکسیداسیون به معنای از دست دادن الکترون ها و کاهش، افزایش الکترون ها است. به عنوان یک قاعده، عناصری که در گوشه سمت چپ پایین جدول تناوبی قرار دارند، بیشترین تمایل را برای از دست دادن الکترون دارند، در حالی که عناصری که به سمت گوشه سمت راست بالا هستند، بیشترین تمایل را برای به دست آوردن الکترون دارند. اکسیژن تمایل زیادی به حذف الکترون از عناصر دیگر دارد و بنابراین یک عامل اکسید کننده است. با این حال، عناصر دیگر نیز می توانند اکسید شوند. به عنوان مثال، فلوئور یک عامل اکسید کننده حتی قوی تر است.