یون چیست و یونها چگونه تشکیل می شوند؟
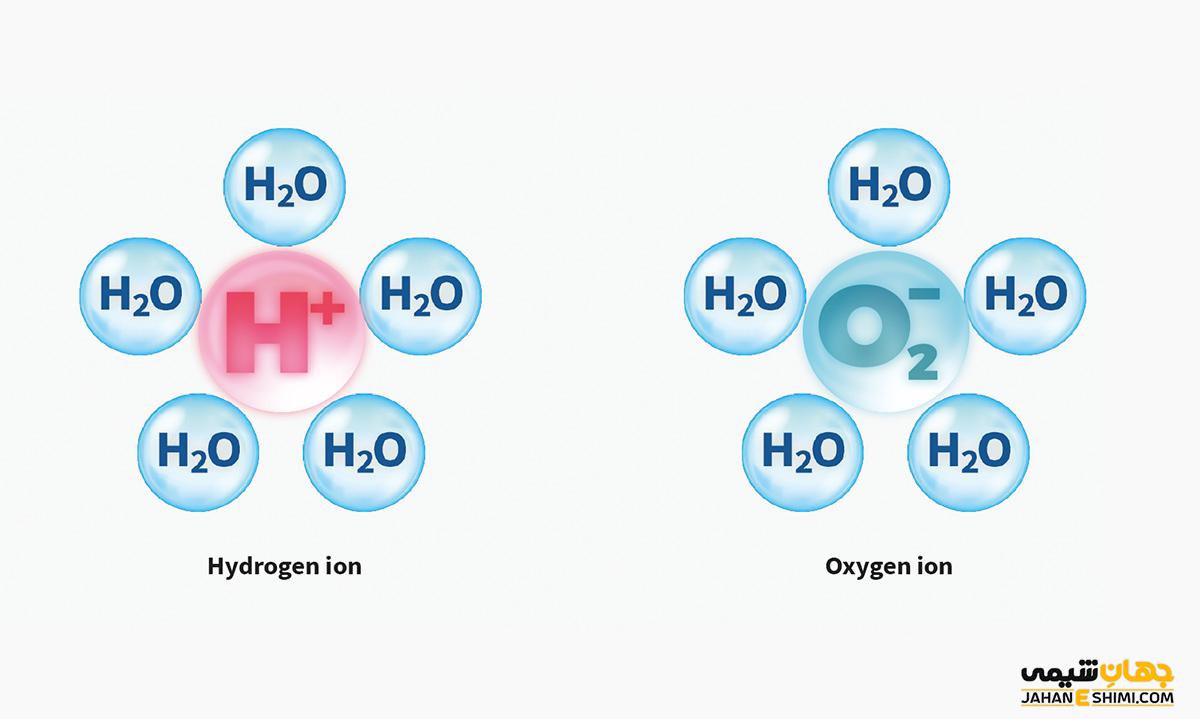
یون یکی از ذرات اتمی حاوی بار الکتریکی است که می توان به دو روش شیمیایی و فیزیکی آن را تولید کرد. اگر یک اتم خنثی یک یا چند الکترون از دست بدهد

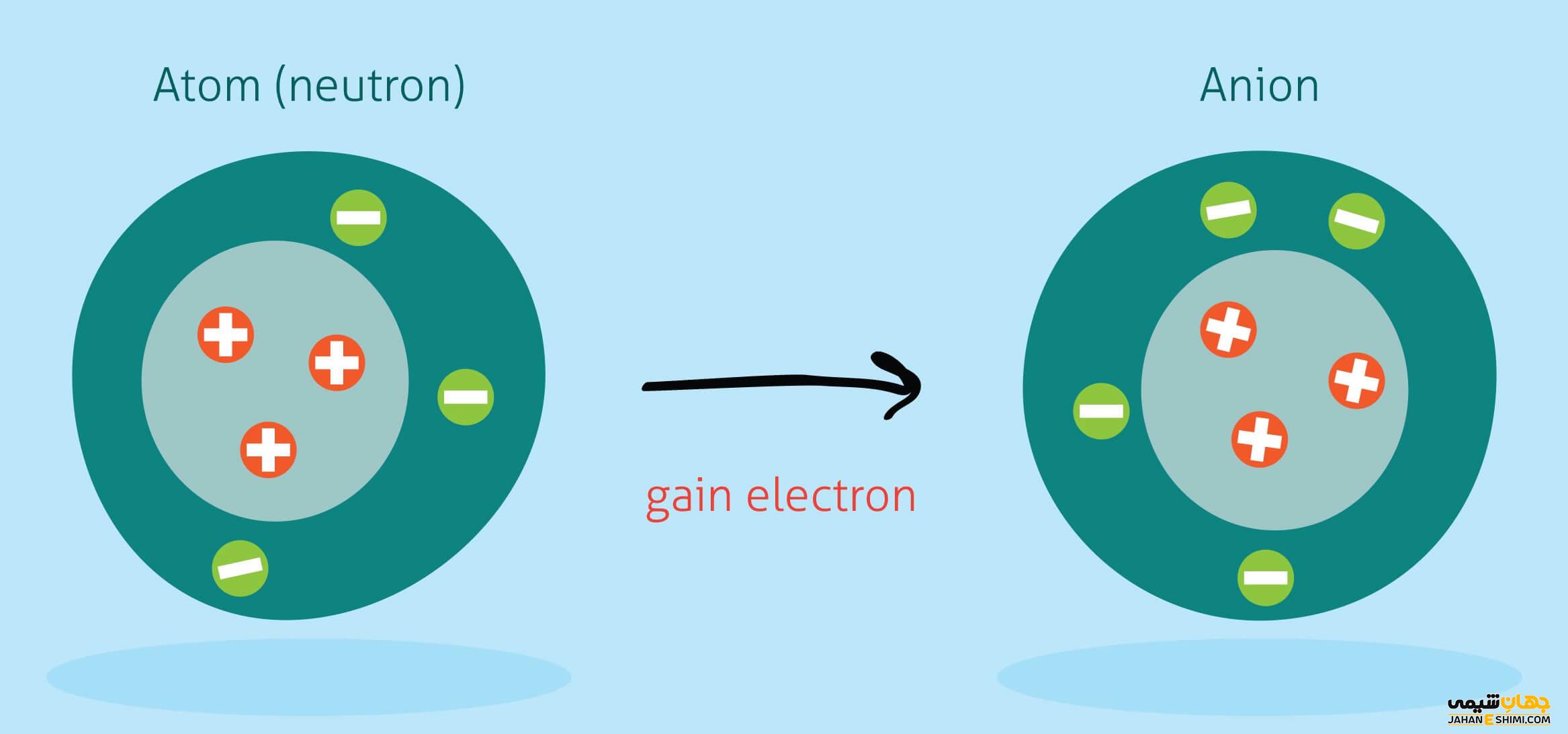
دارای بار مثبت شده و به عنوان کاتیون شناخته می شود. اگر اتمی الکترون دریافت کند دارای بار منفی می شود و به عنوان آنیون شناخته می شود.
به عنوان مثال هنگامی که سدیم (Na) الکترون از دست می دهد به یون مثبت +Na تبدیل می شود و وقتی که کلر (Cl) الکترون می گیرد به یون منفی – Cl تبدیل می شود. هنگام نوشتن فرمول شیمیایی یک یون بار خالص آن بلافاصله پس از ساختار شیمیایی مولکول/اتم به صورت فوق نوشته می شود.
اگر یک یون تنها از یک نوع اتم تشکیل شده باشد می توان آن را یون اتمی یا یون تک اتمی نامید. از طرف دیگر اگر یونی از دو یا چند اتم تشکیل شده باشد می توان آن را یون چند اتمی یا یون مولکولی نامید. شما در مبحث یون چیست علوم هشتم با این ذرات واکنش پذیر آشنا شده اید، برای کسب اطلاعات بیشتر در این رابطه در ادامه مقاله با ما در نشریه جهان شیمی فیزیک همراه باشید.
یون چیست؟
یون را می توان به عنوان یک گونه شیمیایی تعریف کرد که دارای بار مثبت یا منفی است. اصطلاح «یون» را همچنین می توان برای اشاره به اتم ها یا مولکول هایی استفاده کرد که دارای بار خالص غیر صفر هستند.
بنابراین همه یونها یا تعداد بیشتری پروتون نسبت به الکترون ها در ساختار کلی اتمی یا مولکولی خود دارند یا تعداد بیشتری الکترون نسبت به پروتون ها در ساختار اتمی/مولکولی خود دارند.
یون هایی که تعداد پروتون های بیشتری نسبت به الکترون ها دارند دارای بار خالص مثبت هستند. این یونها معمولا کاتیون نامیده می شوند. از سوی دیگر یون هایی که تعداد الکترون های بیشتری نسبت به پروتون ها دارند دارای بار منفی خالص هستند. این یونها معمولا به عنوان آنیون شناخته می شوند.
توجه به این نکته ضروری است که نیروهای جاذبه الکترواستاتیک که بین کاتیون های دارای بار مثبت و آنیون های دارای بار منفی بوجود می آید، نیروی محرکه تشکیل پیوندهای یونی هستند. هنگامی که دو یون دارای بار متضاد یک پیوند یونی با یکدیگر تشکیل می دهند ترکیب یونی تشکیل می دهند.
تاریخچه کشف یون
سایقه معرفی واژه «یون» به شیمی دان و فیزیکدان برجسته انگلیسی مایکل فارادی در سال ۱۸۳۴ تعلق دارد. او از این اصطلاح برای توصیف ترکیب شیمیایی که از یک الکترود به محلول آبی حرکت می کند، استفاده کرد .
اصطلاح یون از کلمه یونانی یون گرفته شده است که به معنی «رفتن» است. اگرچه فارادی هرگز حرکت ذرات را از یک الکترود به الکترود دیگر تشخیص نداد، اما آزمایشات انجام شده وی را به این نتیجه رساند که فلزات تمایل به حل شدن در محلول های خاصی به نام الکترولیت دارند در حالی که ممکن است در الکترود دیگر رسوب تشکیل بدهند. این بدان معناست که باید در ماده ای که تحت تاثیر جریان الکتریکی قرار دارد حرکتی وجود داشته باشد.

یونها چگونه تشکیل می شوند؟
روش های مختلفی برای به وجود آمدن یونها وجود دارد. به عنوان مثال، برخورد خود به خودی بین مولکول های یک مایع یا ترکیب مایع – گازی می تواند منجر به حذف یکی از الکترون ها از اتم/مولکول شود. درنتیجه این منجر به تشکیل یک یون با بار مثبت و یک الکترون آزاد می شود.
این نوع یونیزاسیون معمولا با عنوان یونیزاسیون فیزیکی شناخته می شود. الکترون آزاد نیز ممکن است به اتم یا مولکول دیگری متصل شود و در نتیجه یک آنیون با بار منفی جدید ایجاد شود.
یکی دیگر از فرایندهای مهم که از طریق آن می توان یون ها را ایجاد کرد، از طریق فعل و انفعالات شیمیایی است. به عنوان مثال، هنگامی که یک ترکیب یونی مانند نمک در یک حلال مناسب (مانند آب) حل می شود اتم های تشکیل دهنده نمک تجزیه می شوند و یون های آزاد تشکیل می دهند. وقتی نمک معمولی که به کلرید سدیم نیز معروف است در آب حل شود، تجزیه می شود تا کاتیون های سدیم و آنیون های کلرید تشکیل شود.
سایر فرایندهای قابل توجه که از طریق آنها می توان یون ها را تشکیل داد شامل عبور جریان مستقیم از محلول های رسانای خاص است که منجر به تشکیل یون در محلول می شود.همچنین به انحلال آندها از طریق فرآیند یونیزاسیون مقدار زیادی یون آزاد ایجاد می کند.
خواص یونها
یونها در فاز گازی به شکل یونهای جداگانه وجود دارند اما در فازهای متراکم به صورت کاتیونها و آنیونها وجود دارند که از نظر الکتریکی ترکیباتی خنثی هستند. این ذرات در محلول ها به صورت الکترولیت وجود دارند و ممکن است برای مهاجرت محدود یا نسبتا آزاد باشند.
یونها در حالت گازی ایده آل که یونهای جدا شده یا برهنه نامیده می شوند فاقد قدرت برهم کنش با سایر ذرات یا محیط اطراف هستند و معمولا تک اتمی هستند یا از تعداد کمی اتم تشکیل شده اند.
ویژگی های اولیه یونهای مجزا میزان بار الکتریکی و جرم آنها است. برخی دیگر از ویژگی های یونهای مجزا حساسیت مغناطیسی، قطبی بودن و نرمی/سختی است.
در فازهای متراکم برای یونها می توان اندازه های مشخصی تعیین کرد که به دلیل وجود دافعه قوی مدارهای الکترونی است. ویژگی یونهای موجود در محلول ها با مقادیر ترمودینامیکی از جمله ظرفیت حرارتی مولار استاندارد و آنتروپی مشخص می شود.
انواع یون
توجه داشته باشید که هنگام بحث تبدیل اتم به یون فقط الکترون ها هستند که اضافه یا حذف می شوند. زیرا افزودن یا حذف پروتون ها کل هویت عنصر را تغییر می دهد نه فقط بار آن.
یون های مثبت و منفی نام های خاصی دارند. یونهای مثبت کاتیون و یونهای منفی آنیون نامیده می شوند . یک راه برای به خاطر سپردن این اسامی این است که در مورد پیشوند «anti» فکر کنید که به طور کلی دارای مفهوم منفی است درست مانند یک آنیون دارای بار منفی. یونها می توانند اتم ها، مولکول ها یا ترکیبات واحدی باشند.
یونهای تک اتمی از یک اتم دارای بار تشکیل شده اند، یون های چند اتمی، گروهی از اتم ها هستند که به هم متصل شده اند و دارای بار مثبت یا منفی کلی هستند و به آنها یون های چند ظرفیتی نیز گفته می شود.
این آنیون ها و کاتیون ها، خواه تک اتمی باشند یا چند اتمی اگر بار یکسانی داشته باشند واکنش مشابهی با یکدیگر خواهند داشت. مثلا کاتیون +H با آنیون -Cl پیوند ایجاد می کند تا HCl یا کلرید هیدروژن تشکیل شود. یک کاتیون +H نیز با یک یون فلوئور -F واکنش نشان داده و HF یا فلوراید هیدروژن را تشکیل می دهد. یون هیدروژن با آنیون فلوئور و آنیون کلر واکنش یکسانی نشان می دهد زیرا هر دو آنیون دارای بار یکسانی هستند.
اگر یونی حاوی الکترون های جفت نشده باشد، یون رادیکال نامیده می شود که بسیار واکنش پذیر است. یونهای چند اتمی حاوی اکسیژن مانند کربنات و سولفات را اکسی آنیون می نامند. یونهای مولکولی که حداقل دارای یک پیوند کربن به هیدروژن هستند یونهای آلی نامیده می شوند.
یون پایدار چیست؟
اگر تعداد نوترون های اتم را بر تعداد الکترون ها تقسیم کنیم و عدد به دست آمده کمتر از ۱.۵ باشد، یون پایدار است . اگر عدد به دست آمده بیشتر از ۱.۵ باشد یون ناپایدار است. به عنوان مثال یون طلا یک یون پایدار است.
کاتیون و آنیون چیست؟
یون ها به دو دسته کلی تقسیم می شوند که شامل کاتیون و آنیون هستند.
کاتیون ها
کاتیون ها یونهایی هستند که بار مثبت دارند زیرا تعداد ذرات پروتون در این یونها از تعداد الکترون ها بیشتر است. نماد کاتیون با یک علامت مثبت فوقانی متصل به فرمول شیمیایی نشان داده می شود.
به عنوان مثال در نماد شیمیایی Ca +۲ عدد ۲ میزان بار است و علامت مثبت یعنی این یون دارای ۲ بار مثبت است. در صورتی که هیچ عددی قبل از علامت بعلاوه وجود نداشته باشد، فرض می شود که بار یون۱ است.
آنیون ها
آنیون ها یونهای دارای بار منفی هستند. تعداد الکترون ها در یک آنیون از تعداد پروتون ها بیشتر است در نتیجه باعث بار منفی می شود. لازم به ذکر است که تعداد نوترون ها هنگام تعیین اینکه اتم یا مولکول آنیون است یا کاتیون اهمیتی ندارد. مشابه کاتیونها، آنیونها نیز با عددی که بار آن را قبل از علامت منفی نشان می دهد، مشخص می شوند.
به عنوان مثال یون کلر -Cl یک بار منفی را حمل می کند. به منظور جلوگیری از هرگونه سردرگمی در به خاطر سپردن یون مثبت و منفی، می توانید با تصور حرف «t» در کاتیون نماد بعلاوه آن را به خاطر بسپارید در حالی که حرف «n» در آنیون را می توان برای به خاطر سپردن علامت منفی این یون به کار برد.
به این ترتیب به راحتی می توانید تعاریف را به درستی به خاطر بیاورید. از نظر علمی متضادها جذب هم می شوند بنابراین طبیعی است که کاتیون ها، آنیون ها را جذب کنند زیرا آنها دو بار الکتریکی متضاد هستند.
با رعایت این اصل دو کاتیون همیشه یکدیگر را دفع خواهند کرد زیرا دارای بار مشابه هستند. این جاذبه و دافعه اساس واکنش شیمیایی را تشکیل می دهد. ترکیبات به ویژه نمک ها به راحتی توسط کاتیون ها و آنیون ها تشکیل می شوند. همچنین بهتر است بدانید که یک یون تحت تاثیر میدان مغناطیسی قرار می گیرد زیرا یک بار الکتریکی است.
مثالهایی از یونهای مختلف
نمونه هایی از کاتیونهای ساده (کاتیونهای تک اتمی)
- کاتیون آلومینیوم – با فرمول شیمیایی Al+۳ نشان داده شده است .
- کاتیون کلسیم – با فرمول شیمیایی Ca+۲ نشان داده می شود .
نمونه هایی از کاتیون چند اتمی (کاتیون های مولکولی)
- کاتیون هیدرونیوم – با فرمول شیمیایی +H3O نشان داده شده است.
- کاتیون آمونیوم- توسط فرمول شیمیایی +NH4 مشخص می شود.
نمونه هایی از آنیون های ساده (آنیون های تک اتمی)
- آنیون فلوراید- با فرمول شیمیایی -F نشان داده می شود.
- آنیون کلرید – با فرمول شیمیایی -Cl نشان داده می شود.
نمونه هایی از آنیون های چند اتمی (آنیون های مولکولی)
- آنیون نیترات – با فرمول شیمیایی -NO3 نشان داده می شود.
- آنیون نیتریت – با فرمول شیمیایی -NO2 نشان داده می شود.
آنیون هایی که از ترکیبات آلی تشکیل می شوند
برخی از آنیونها از طریق دافعه اولیه برخی اسیدهای آلی تشکیل می شوند. آنیون های دیگر از ترکیبات آلی خاصی مشتق شده اند. نمونه های متداول آنیون هایی که از ترکیبات آلی مشتق شده اند در زیر فهرست شده است.
- آنیون فرمات- با فرمول شیمیایی -HCOO نشان داده می شود.
- آنیون استات – با فرمول شیمیایی -CH3COO نشان داده می شود.
- آنیون سیانور – با فرمول شیمیایی –CN نشان داده می شود.
ترکیب یونی چیست؟
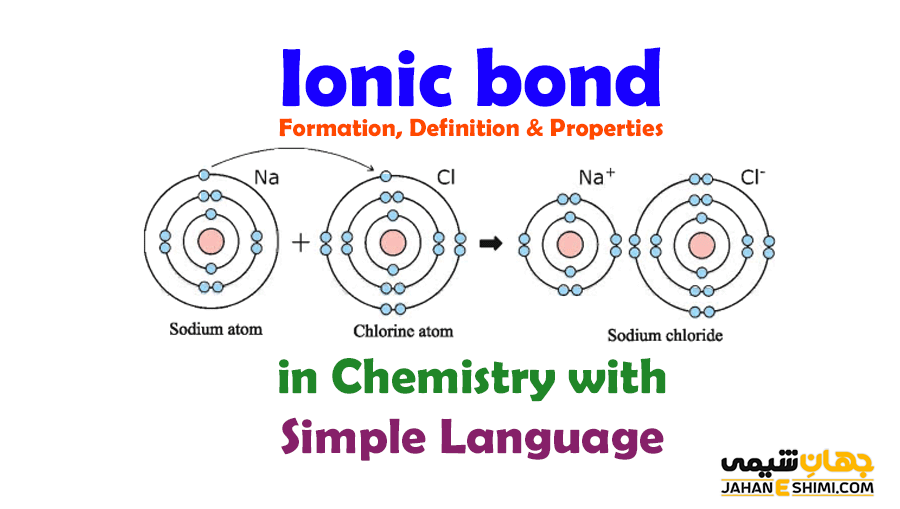
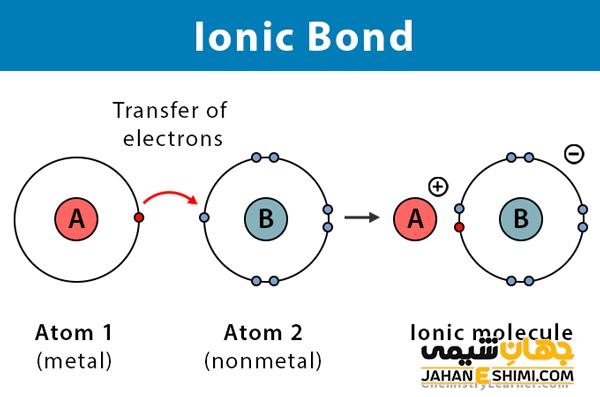
ترکیبات یونی نوعی از ترکیبات شیمیایی هستند که در آن یونهای دارای بار مخالف یک فلز و یک غیر فلز برای ایجاد پیوند یونی به یکدیگر جذب می شوند. ترکیب تشکیل شده از یونهای پیوندی خواص بسیار متفاوتی با عناصر تشکیل دهنده خود دارند.
در واکنش یک فلز و یک غیر فلز هنگامی که الکترونها از فلز به غیر فلز منتقل می شوند، ترکیبات یونی تشکیل می شوند. که این در حالی است که اتم های اولیه خنثی هستند زیرا تعداد پروتون ها و الکترون های مساوی دارند.
یون ها دارای بار خالص هستند و این زمانی اتفاق می افتد که اتمی الکترون از دست می دهد یا به دست می آورد. تعداد پروتون ها در یون ثابت می ماند، بنابراین از دست دادن یا افزایش الکترون ها منجر به ذره ای می شود که دارای بار خالص مثبت یا منفی است.
فلزات الکترون از دست می دهند و کاتیون هایی ایجاد می کنند که یونهای دارای بار مثبت خالص هستند در حالی که غیر فلزات الکترون را برای تشکیل آنیونها که یون با بار منفی خالص هستند، به دست می آورند .
در شکل گیری ترکیبات یونی، کاتیونها و آنیونهای با بار مخالف یکدیگر را به صورت الکترواستاتیک جذب کرده و پیوندهای یونی قوی ایجاد می کنند. کاتیونها و آنیونهای متعدد توسط پیوندهای یونی کنار هم نگه داشته می شوند تا یک ساختار بلوری جامد یا مشبک به نام ترکیب یونی ایجاد شود.
در مثال کلرید سدیم، سدیم یک فلز است و الکترون ظرفیتی خود را از دست می دهد تا یون مثبت با بار ۱+ تشکیل شود. اتم کلر الکترون از دست رفته توسط سدیم را جذب کرده و در نتیجه ترکیب یونی کلرید سدیم تشکیل می شود.
ویژگی ترکیبات یونی
ترکیبات یونی را اغلب می توان با ویژگی های آنها شناسایی کرد. بیشتر ترکیبات یونی دارای ویژگی های زیر هستند.
- ترکیبات یونی به صورت جامدات سخت، شکننده و بلوری وجود دارند.
- ترکیبات یونی دارای نقاط ذوب و نقاط جوش بسیار بالایی هستند.
- ترکیبات یونی به راحتی تجزیه نمی شوند.
- بیشتر ترکیبات یونی در آب محلول هستند و محلول های الکترولیت را تشکیل می دهند.
- ترکیبات یونی هنگام حل شدن در آب یا ذوب شدن، جریان الکتریکی را هدایت می کنند.
علاوه بر نمک سفره یا NaCl، بسیاری از ترکیبات یونی رایج در زندگی روزمره وجود دارد. به عنوان مثال فلوراید موجود در خمیردندان به صورت ترکیب یونی فلوراید سدیم NaF است. بسیاری از دئودورانت ها حاوی ترکیب یونی کلرید کلسیم CaCl 2 هستند. این ترکیب همچنین در آب و هوای سرد در جاده ها برای کاهش نقطه انجماد آب استفاده می شود. اکثر نمک های غذایی خریداری شده حاوی یدید پتاسیم، KI است. یون یدید یک یون مهم برای سلامت تیروئید انسان است. زنگ آهن نیز در نتیجه واکنش آهن با اکسیژن برای تولید اکسید آهن تولید می شود که یک ترکیب یونی است.
ترکیبات یونی چند اتمی
یونهایی که از یک عنصر واحد تولید شده اند، یونهای تک اتمی نامیده می شوند. با این حال، برخی از ترکیبات یونی حاوی یونهای چند اتمی هستند. یونهای چند اتمی یونهایی هستند که از دو یا چند اتم با پیوند کووالانسی تشکیل شده اند. در واقع یک یون چند اتمی الکترون هایی را برای تشکیل یک یون به دست آورده یا از دست داده است. برخی از نمونه های رایج یونهای چند اتمی عبارتند از:
یون هیدروکسید -OH، یون نیترات NO-۳، یون آمونیوم NH-۴، یون سولفاتSO4-۲ و یون فسفاتPO4-۳
بسیاری از ترکیبات معمولی یونی حاوی یون های چند اتمی هستند به عنوان مثال:
آنتی اسیدها – برای مبارزه با سوزش سر دل به کار می روند و حاوی هیدروکسید منیزیم Mg (OH) ۲ هستند.
گچ – گچ تخته سیاه حاوی کربنات کلسیم CaCO3 است.
جوش شیرین – نام متداول بی کربنات سدیم با فرمول شیمیایی NaHCO3 است که هنگام پختن کلوچه، نان و سایر غذاهای پخته استفاده می شود.
کود معمولی– نیترات آمونیوم -NH4NO3 از دو یون چند اتمی تشکیل شده است.
روش نوشتن فرمول ترکیبات یونی
اولین قدم این است که نماد هر یون را بنویسید، فلز یا یون مثبت و نماد غیر فلز بعد از فلز نوشته شود. در مورد یونهای چند اتمی، فرمول کامل یون چند اتمی نوشته می شود و فرمول باید متعادل سازی شود این بدان معناست که کل بار مثبت باید برابر کل بار منفی یونهای موجود در فرمول باشد. در این فرمول زیرنویس ها اضافه می شوند تا کل بار مثبت و منفی از نظر اندازه برابر شود.
خواص ترکیبات یونی
ترکیبات یونی به دلیل پیوندهای قوی که کاتیون ها و آنیون ها را در کنار هم نگه می دارد، ویژگی های مشابه زیادی دارند. خواص ترکیبات یونی عبارتند از:
جامدات کریستالی
ترکیبات یونی جامدات کریستالی متشکل از میلیون ها کاتیون و آنیون هستند که در یک الگوی تکراری به هم متصل شده اند. به دلیل این ساختار بلوری، یونها به طور محکم در محل خود نگه داشته شده اند. این امر از خم شدن بلورها جلوگیری می کند و در عوض بلورهای یونی را بسیار شکننده می کند.
رنگ
ترکیبات یونی که دارای یک عنصر نماینده به عنوان یون مثبت خود هستند معمولا دارای رنگ سفید هستند. با این حال ترکیبات یونی تشکیل شده از فلزات انتقالی معمولا یون های رنگی را تشکیل می دهند. فلزات انتقالی با اوربیتال های d ناقص رنگ هایی از قرمز در نیترات کبالت (II) تا کریستال های آبی سولفات مس (II) و سبز کلرید نیکل (II) را نشان می دهند.
نقطه ذوب و جوش بالا
ترکیبات یونی به عنوان مواد جامد در دنیای امروزی بسیار مورد استفاده قرار می گیرند زیرا دارای نقطه ذوب و جوش بسیار بالایی هستند. به عنوان مثال نمک روی اجاق گاز خانگی معمولی ذوب نمی شود زیرا کلرید سدیم برای ذوب شدن باید به دمای ۸۰۱ درجه سانتی گراد برسد.
نقاط ذوب بالا نتیجه پیوندهای یونی بسیار قوی در این ترکیبات است. برای ذوب شدن یک ترکیب یونی، پیوندهای یونی باید شکسته شوند. از آنجا که پیوندهای یونی بسیار قوی هستند، برای شکستن آنها به مقدار زیادی انرژی گرمایی نیاز است.
رساناهای جریان الکتریکی
هنگامی که ترکیبات یونی در آب حل می شوند یا ذوب می شوند، تجزیه شده یا به کاتیون های فلزی و آنیون های غیر فلزی تجزیه می شوند. این یون ها در محلول الکتریسیته را هدایت می کنند بنابراین ترکیبات یونی در این شرایط رسانای خوبی هستند. اما به عنوان یک بلور جامد، یونها بی حرکت هستند و الکتریسیته را هدایت نمی کنند. در واقع ترکیبات یونی به شکل جامد، عایق هستند.
چگونه بار یون را بدست اوریم
یون اتمی است که دارای بار الکتریکی است زیرا یک یا چند الکترون خود را از دست داده یا به دست آورده است. در شیمی یون های دارای بار مثبت کاتیون و یون های دارای بار منفی آنیون نامیده می شوند. یونها بسته به شرایط خاص، مانند وجود تشعشعات یونیزان یا بار الکتریکی قوی مانند صاعقه، میتوانند در محلولها یا به تنهایی وجود داشته باشند.
هنگامی که یک اتم یک یا چند الکترون ظرفیت خود را از دست می دهد، دارای بار مثبت می شود (این کاتیون نامیده می شود). برعکس، هنگامی که یک اتم یک یا چند الکترون به دست آورد، بار منفی (آنیون) می شود. شما می توانید بار یک اتم را بر اساس تعداد الکترون هایی که از بین رفته یا به دست می آیند محاسبه کنید.
بسیاری از مواد در محلول های آبی یون تشکیل می دهند، اما این امر به ویژه در مورد نمک ها، اسیدها و بازها صادق است. یون های آنها در آب تجزیه می شوند. با این حال، اسیدهای ضعیف و بازهای ضعیف به طور کامل در آب تجزیه نمی شوند. حتی آب خالص تا حدی به یون های هیدرونیوم و یون هیدروکسیل (فرآیندی که به نام خود یونیزاسیون شناخته می شود) تجزیه می شود.
یون ها نقش مهمی در طبیعت، به ویژه در سیستم های بیولوژیکی دارند. آنها علاوه بر کمک به حفظ ساختار سلول ها، در بسیاری از فرآیندهای سلولی مانند انتقال مواد مغذی و دفع مواد زائد نقش دارند. در موجودات چند سلولی مانند انسان، یون ها در انتقال سیگنال ها از مغز به سایر اندام ها بسیار مهم هستند.
یون ها در آزمایشات شیمی و تولید صنعتی نیز مهم هستند. به عنوان مثال، آنها برای تولید انواع مختلف باتری و تهیه محصولات شیمیایی مانند استخراج هیدروژن و اکسیژن از آب از طریق الکترولیز استفاده می شوند. یون ها همچنین در فرآیند آبکاری الکتریکی که بر واکنش های ردوکس غیر خود به خودی متکی است، دخیل هستند.
سخن پایانی
یونها ذرات بسیار واکنش پذیری هستند که به طور طبیعی در مقادیر زیاد روی زمین وجود ندارند مگر از طریق شعله های آتش، رعد و برق، جرقه های الکتریکی و غیره تشکیل شوند. اکثر یونها به سرعت با یونهای بار مخالف واکنش می دهند تا مولکول های خنثی یا نمک ها را تولید کنند که پایدارتر هستند. یونها مسئول پدیده های متنوعی از درخشندگی خورشید گرفته تا وجود یونوسفر زمین هستند. به عنوان ذرات باردار واکنشی آنها همچنین در تصفیه هوا با ایجاد اختلال در رشد میکروب ها و در وسایل خانگی مانند آشکارسازهای دود مورد استفاده قرار می گیرند.



















یک دیدگاه