مولکول قطبی چیست ؟ چگونه می توان آن را تشخیص داد ؟
در علم شیمی مولکول ها و همچنین پیوند های بین اتم ها را می توان بر اساس قطبیت به دو دسته قطبی و نا قطبی (غیر قطبی) تقسیم بندی کرد.

بین مولکول قطبی با پیوند قطبی تفاوت زیادی وجود دارد. در واقع به مولکولی گفته می شود که دارای قطب مثبت و منفی باشد. یعنی یک سمت مولکول مثبت و سمت دیگر آن منفی است. یک مولکول می تواند علی رغم داشتن پیوندهای قطبی، مولکولی ناقطبی باشد که در ادامه به آن خواهیم پرداخت. نشریه جهان شیمی فیزیک قصد دارد در این مقاله و مقاله مشابه دیگر به بررسی قطبیت مولکول ها و ویژگی های آنها بپردازد. در اینجا می خواهیم با مفهوم این نوع مولکولها آشنا شویم. لطفا با ما همراه باشید.
فهرست مطالب
تفاوت مولکول و پیوند
مهمترین سوالی که در ابتدا با آن مواجه می شویم این است که پیوند با مولکول چه فرقی دارد ؟ پیوند در واقع رابط بین دو اتم می باشد. می توان پیوند را به صورت طنابی در نظر گرفت که دو اتم در دو سر آن متصل شده اند. اما مولکول ها از یک یا چند پیوند بین اتم ها به وجود می آیند. ساده ترین شکل مولکول ها، یک مولکول دو اتمی است که تنها از یک پیوند تشکیل شده است. با افزایش تعداد اتم ها و در نتیجه افزایش تعداد پیوند ها، مولکول های چند اتمی تشکیل می شوند.
قطبیت پیوند یا پیوند قطبی
قطبیت پیوند یعنی چی ؟ قطبیت پیوند به همراه استحکام پیوند و طول پیوند سه ویژگی اصلی پیوند های شیمیایی می باشند. پیوند های بین اتم ها در یک مولکول یا قطبی اند یا غیر قطبی. چنانچه دو اتم مختلف با هم پیوند تشکیل دهند، به دلیل اختلاف الکترونگاتیوی اتم ها، الکترون های پیوندی بیشتر به سمت یکی از اتم ها کشیده می شوند. در واقع چگالی ابر الکترونی بر روی اتم با الکترونگاتیوی بالاتر قرار می گیرد.
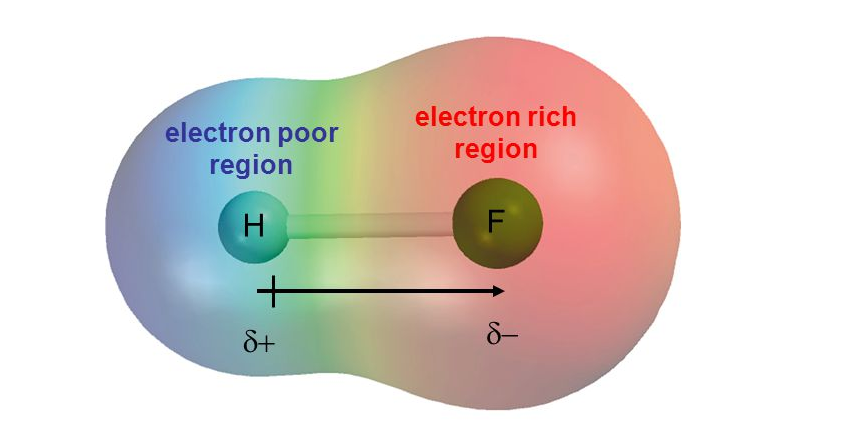
بنابراین مقداری بار جزیی منفی بر روی اتم الکترونگاتیوتر و هم زمان مقداری بار جزئی مثبت بر روی اتم با الکترونگاتیوی کمتر به وجود می آید. در این صورت پیوند دارای یك سر مثبت و یك سر منفی می شود که در نتیجه پیوند قطبی ایجاد می شود. برای نشان دادن مقادیر بار جزیی از علامت دلتا (δ) استفاده می شود. در شکل زیر می توانید توزیع ابر الکترونی در یک پیوند کووالانس قطبی را مشاهده نمایید.
نکته
قدرت پیوند متناسب با تفاوت الکترونگاتیویته اتم های شرکت کننده در پیوند است. به عنوان مثال پیوند O-H به دلیل اختلاف الکترونگاتیویته بیشتر بین اتم های اکسیژن و هیدروژن قطبی تر از پیوند C-H است. از جمله پیوندهای قطبی می توان به پیوندهای Cl-O، N-H، Be-Cl، H-Br، O-F، S-O، P-H و C=O اشاره کرد.
برای نشان دادن قطبیت پیوند از بردار قطبیت کمک می گیریم. به عنوان نمونه بردار قطبیت مولکول HCl در زیر نشان داده شده است. همانطور که در شکل نشان داده شده است، بردار قطبیت دارای جهت، راستا و مقدار می باشد. جهت بردار قطبیت از سمت اتم با الکترونگاتیویته کمتر به سمت اتم با الکترونگاتیویته بیشتر می باشد. از طرفی، راستای آن موازی با راستای پیوند و مقدارش با اختلاف الکترونگاتیویته اتم های دو سر پیوند برابر خواهد بود.
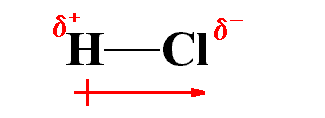
مولکول قطبی
مولکول قطبی چیست ؟ در واقع به مولکولی گفته می شود که دارای قطب مثبت و منفی باشد. یعنی یک سمت مولکول مثبت و سمت دیگر آن منفی است. بنابراین زمانیکه بارهای مثبت و منفی در مولکول به طور مساوی پخش نشده اند، مولکول قطبی خواهد بود. در واقع می توان گفت که مرکز بارهای مثبت و منفی در این مولکول بر هم منطبق نیستند.
نکته جالب اینجاست که مولکول های خنثی نیز می توانند در دسته این مولکول ها قرار بگیرند. در واقع بر خلاف خنثی بودن مولکول، تجمع چگالی الکترون ها در یک قسمت مولکول، بیشتر از سایر قسمت های آن می باشد، در نتیجه مولکول دارای دو قطب مثبت و منفی شده، بنابراین مولکول قطبی می شود. مثال این مورد مولکول اوزون هست که در ادامه مقاله به آن خواهیم پرداخت.
معمولا برای اینکه یک مولکول در این دسته مولکول ها قرار بگیرد باید دو شرط اولیه زیر را داشته باشد. این دو شرط عبارتند از: مولکول حداقل یک پیوند کووالانسی قطبی داشته باشد و همچنین برآیند بردارهای ممان دو قطبی مولکول یکدیگر را خنثی نکرده و برابر با عددی غیر صفر باشد.
در بعضی موارد علی رغم اینکه مولکول چند اتمی از پیوندهای یکسان تشکیل شده است، اما پیوندها در ساختار مولکول طوری قرار گرفته اند که چگالی ابر الکترونی در ساختار یکنواخت نیست. بنابراین مولکول قطبی است. از این رو در بررسی مولكول ها علاوه بر قطبی بودن پیوند های کووالانسی، باید به شكل هندسی مولكول نیز توجه کنیم.
نحوه تشخیص مولکول های قطبی
راه تشخیص سریع مولکول قطبی چیست ؟ همانطور که در این مقاله بیان شد قطبی بودن یک مولکول به قطبیت پیوند و شکل هندسی مولکول بستگی دارد. بنابراین برای تشخیص قطبیت یک مولکول بهتر است علاوه بر الکترونگاتیویته، به ساختار لوویس و جفت الکترون های غیر پیوندی اتم مرکزی نیز نگاه کنیم.
به طور کلی می توان گفت که این مولکول ها چه زمانیکه اتم مرکزی با اتمهایی با الکترونگاتیویته های مختلف پیوند داده و چه زمانیکه جفت الکترون ناپیوندی دارد، شکل ساختار نا متقارن است. برای بررسی راحت تر مولکول ها، می توان مولکول ها را به دو دسته مولکول های دو اتمی و مولکول های چند اتمی طبقه بندی کرد و هر دسته رو جداگانه بررسی نمود.
قطبیت مولکول های دو اتمی
در مولکول های دو اتمی، قطبیت پیوند در قطبی بودن مولکول تاثیر مستقیم دارد. در این مولکول ها چون تنها از یک پیوند تشکیل شده اند، بنابراین اگر پیوند کووالانسی قطبی باشد مولکول هم قطبی خواهد بود. در واقع اگر دو اتم تشكیل دهنده مولكول، ناجور هسته باشند، به دلیل اختلاف الکترونگاتیویته اتم های دو سر پیوند، یک سر مولکول دارای بار جزئی منفی و سر دیگر آن دارای بار جزئی مثبت می شود. بنابراین قطبی خواهد بود.
برای نمونه مولکول HCl را در نظر بگیرید. در این مولکول به دلیل بالاتر بودن الکترونگاتیویته اتم کلر نسبت به اتم هیدروژن، جفت الكترون های پیوندی به سمت اتم کلر می باشند. در واقع این بخش از مولکول HCl دارای قطب منفی بوده که با δ− نشان داده می شود. بخش دوم مولکول، یعنی اتم هیدروژن قطب مثبت و دارای بار جزئی مثبت می باشد (با δ+ نشان داده میشود). توجه داشته باشید که به نواحی باردار مولکول قطبی، قطب های مولکول نیز گفته می شود.
قطبیت مولکول های چند اتمی
بررسی قطبیت مولکول های چند اتمی به سادگی مولکول های دو اتمی نیست. در این مولكول ها ساختار و شكل هندسی مولكول نیز در تعیین قطبی یا نا قطبی بودن آن تاثیر به سزایی دارد. حتی می توان گفت که ساختار و شکل فضایی مولکول چند اتمی مهم تر از قطبی یا نا قطبی بودن پیوندها است.
بنابراین همان طور که قبلا بیان شد در مولکول های چند اتمی، برای قطبی بودن مولکول دو شرط اساسی داریم. این دو شرط عبارتند از: اتم مرکزی باید با اتم های مختلف پیوند داده باشد. اتم مرکزی دارای جفت الکترون نا پیوندی باشد.
برای اینکه این موضوع را بهتر متوجه شوید، مولکول های چند اتمی را در دو دسته جداگانه بررسی می کنیم. ابتدا حالتی را در نظر می گیریم که اتم مرکزی جفت الکترون نا پیوندی ندارد، بنابراین برای قطبی بودن، اتم های متصل به اتم مرکزی باید متفاوت باشند. به عنوان مثال مولکول HCN را در نظر بگیرید، در این مولکول، اتم مرکزی کربن به اتم های متفاوت هیدروژن و نیتروژن متصل شده است.
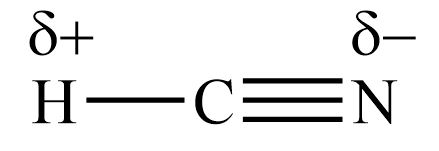
بررسی مولکول آب
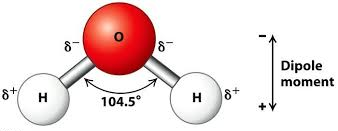
در حالت دوم، اتم مرکزی دارای جفت الکترون غیر پیوندی است. برای نمونه به مولکول H۲O دقت کنید. ساختار هندسی آب به دلیل داشتن جفت الکترون های نا پیوندی به شکل خمیده است. جفت الکترون های غیر پیوندی را می توان به عنوان قطب منفی، و هسته اتم اکسیژن را به عنوان قطب مثبت در نظر گرفت. پس برای جفت الکترون های نا پیوندی آب نیز می توان ممان دو قطبی در نظر گرفت.
از طرفی الکترونگاتیویته اتم اکسیژن نسبت به اتم هیدروژن بیشتر است، بنابراین الکترون های اشتراکی را به سمت خود می کشد. بنابراین جهت گشتاور دو قطبی از سمت اتم هیدروژن به سمت اتم اکسیژن است. به دلیل ساختار فضایی مولکول آب، جمع برداری ممان های دو قطبی نسبت به هم صفر نمی شود، بنابراین مولکول آب قطبی است. در شکل زیر گشتاور دوقطبی این مولکول نشان داده شده است.
بررسی مولکول اوزون
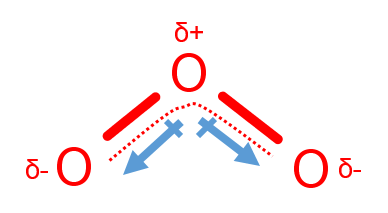
در بسیاری از موارد، قطبیت پیوند ها همسو با قطبی بودن مولکول است. اما موارد استثنا نیز وجود دارد (O۳). مولکول اوزون از سه اتم یکسان اکسیژن با پیوند های کووالانسی غیر قطبی تشکیل شده است، اما بر خلاف انتظار مولکول اوزون قطبی است. به دلیل هم ارز بودن اتم های اکسیژن در دو سر مولکول، این مولکول را می توان با ساختار رزونانس نشان داد.
قطبی بودن اوزون به دلیل شکل هندسی خمیده مولکول می باشد. در این مولکول، اتم مرکزی (یکی از اتم های اکسیژن) دارای بار جزئی مثبت و دو اتم اکسیژن دیگر دارای بار جزئی منفی هستند. بنابراین جهت گیری اتم ها در ساختار به گونه ای است که برآیند بردارهای ممان دو قطبی غیر صفر بوده و مولکول قطبی می شود.
انحلال پذیری مولکول های قطبی
این مولکول ها را می توان هم به عنوان حل شونده در نظر گرفت و هم به عنوان حلال. در انحلال پذیری مواد در شیمی، قانونی وجود دارد که می گوید شبیه، شبیه را در خود حل میکند. به عبارت دیگر، یک حل شونده در حلالی که ساختار شیمیایی مشابه با آن داشته باشد به خوبی حل می شود. این مولکول ها آب دوست اند، بنابراین این مولکول ها در حلال های قطبی، انحلال پذیری خوبی دارند. به بیان دیگر در حلال های قطبی، مولکول هایی که گشتاور دو قطبی غیر صفر دارند، حل می شوند.
حل شدن مواد در آب چگونه انجام می شود؟
مایعات قطبی مانند آب می توانند حلال بسیاری از مولکول های قطبی و همچنین ترکیبات یونی باشند. ظرفیت انحلال یک حلال قطبی، به طور مستقیم به قطبیت آن حلال بستگی دارد. در واقع یک حل شونده قطبی قوی اوره به شدت در آب حلال می شود اما در حلال هایی با قطبیت کمتر انحلالپذیری کمتری را نشان می دهد.
در ادامه انحلال پذیری ترکیبات یونی در حلال های قطبی مانند آب را بررسی می کنیم. ترکیبات یونی از قطب های منفی و مثبت تشکیل شده اند. در زمان انحلال، یون های مثبت ترکیبات یونی به وسیله قطب های منفی مولکول های حلال و یون های منفی ترکیبات یونی به وسیله قطب های مثبت مولکول های حلال جذب میشوند. بنابراین یون های مثبت و منفی ترکیبات یونی از بلور جدا شده و در آب شناور و در واقع حل می شوند.
لیست مولکول های قطبی
در پاراگراف زیر نمونههایی از این مولکول ها آورده شده است. برای اینکه دلیل قطبی بودن هر کدام را تشخیص دهید، لظفا مقاله را دوباره مرور نمایید.
مولکولهای قطبی دو اتمی:
Hcl, HF, HI, HBr, NO, CO, HCN
مولکولهای قطبی چند اتمی:
SO۲, H۲O, NH۳, N۲O, POCl۳, O۳, NO۲, PCl۳, CHCl۳, CH۲O, CoCl۲, CH۲Cl۲
جهت گیری در میدان الکتریکی
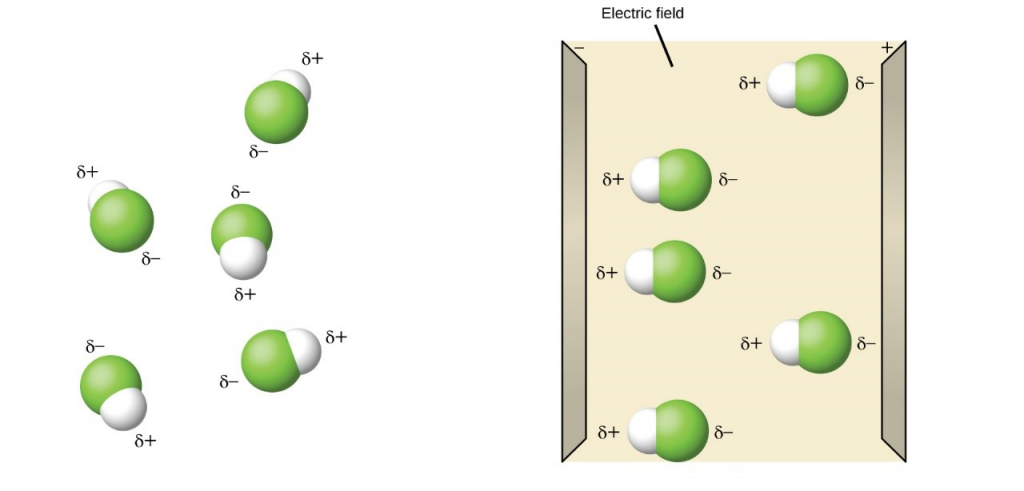
همان طور که در این مقاله بیان شد، این مولکول ها ، سرهای مثبت و منفی دارند، بنابراین این مولکول ها در یک میدان الکتریکی جهت گیری می کنند. جهت گیری این مولکول ها در یک میدان الکتریکی، به گونه ای است که سر مثبت مولکول به سمت صفحه منفی و سر منفی آن به سمت صفحه مثبت قرار می گیرند. در شکل زیر یک این نوع مولکول را در حضور میدان و در غیاب میدان الکتریکی مشاهده می کنید.
روش تشخیص قطبی یا ناقطبی بودن مولکول
در مولکول قطبی توزیع الکترون ها بین اتم های درگیر ناهموار است و در نتیجه یک گشتاور دوقطبی ایجاد می شود. اصطلاح قطبیت برای توصیف تفاوت در قطب های الکتریکی یک مولکول استفاده می شود که سپس تعیین می کند که مولکول چقدر قطبی است. تعیین قطبی بودن یا نبودن یک مولکول از مجموع تمام پیوندهای موجود در مولکول حاصل می شود.
قطبیت زمانی ایجاد می شود که یک پیوند با اتم هایی که در الکترونگاتیوهایشان تفاوت دارند تشکیل شود. هنگامی که یکی از اتم ها میل الکترونی بالاتری داشته باشد، جفت الکترون های مشترک را به سمت خود جذب می کند که توزیع الکترون ها را تغییر می دهد.
اگر تفاوت در الکترونگاتیوی قابل توجه باشد، یک پیوند قطبی با شکل می گیرد. اگر اختلاف بسیار زیاد باشد، یکی از اتم ها الکترونها را کاملاً به سمت خود می کشد و در نتیجه یک پیوند یونی ایجاد می شود.
قطبیت اغلب در مورد پیوندهای کووالانسی بیان می شود، زیرا این پیوندها از اشتراک الکترون ها تشکیل می شوند. مولکول های قطبی در حضور میدان الکتریکی خود را در جهت خاصی جهت می دهند. انتهای مثبت مولکول ها به سمت قطب منفی میدان هدایت می شود، در حالی که انتهای منفی به سمت قطب مثبت هدایت می شود.
در مورد مولکول هایی با بیش از دو اتم، هندسه مولکول ها باید در نظر گرفته شود تا قطبیت آنها مشخص شود. در ترکیبات چند اتمی، قطبیت به گشتاور دوقطبی خالص تمام پیوندهای کووالانسی موجود در مولکول بستگی دارد.
در مقابل مولکول های غیرقطبی مولکول هایی هستند که در آنها الکترون ها به طور مساوی بین اتم های درگیر به اشتراک گذاشته شده اند و دارای گشتاور دوقطبی صفر هستند. مولکولهای غیرقطبی زمانی تشکیل میشوند که دو اتم درگیر در یک پیوند شیمیایی، میل مشابهی نسبت به الکترونها داشته باشند که توزیع برابر الکترونها را بین آنها ممکن میسازد. پیوندهای غیرقطبی واقعی فقط بین مولکول های دواتمی یک عنصر مانند N2 و O2 وجود دارد.
مولکول قطبی و ناقطبی شیمی دهم
مولکول ها از اتمهای مختلف تشکیل شده اند و خواص فیزیکی و شیمیایی آنها بستگی به ساختار و توزیع بار الکتریکی در داخل مولکول دارد. یکی از ویژگیهای مهم مولکولها، قطبیت آنها است. قطبیت به نحوه توزیع بار الکتریکی در مولکول اشاره دارد. در مولکول قطبی بار الکتریکی مثبت و منفی در آن به طور نامتقارن توزیع شده باشد. این عدم تقارن باعث ایجاد یک دو قطبی الکتریکی در مولکول می شود. در مولکول های قطبی پیوندهای قطبی وجود دارد و شکل هندسی مولکول به گونه ای است که بارها به صورت یکنواخت توزیع نشده اند. یک مثال از مولکول قطبی، مولکول آب (H₂O) است که در آن اتم اکسیژن بار منفی نسبی و اتم های هیدروژن بار مثبت نسبی دارند.
مولکول ناقطبی برعکس مولکول قطبی دارای توزیع بار الکتریکی یکنواخت و متقارن هستند بنابراین مولکول هیچ بار الکتریکی ندارد. نمونههایی از مولکولهای ناقطبی شامل گازهای نجیب و مولکولهای هیدروکربن ساده مانند متان (CH₄) هستند.
درک تفاوت بین مولکولهای قطبی و ناقطبی برای دانش آموزان اهمیت زیادی دارد زیرا بر خواص فیزیکی و شیمیایی مواد مانند نقطه جوش، حلالیت و واکنشپذیری تاثیرگذار است. علاوه بر این مولکول های قطبی معمولاً در حلالهای قطبی حل می شوند و مولکولهای ناقطبی در حلالهای ناقطبی بهتر حل می شوند. این موارد برای درک واکنش های شیمیایی بسیار مفید است.



















