عناصر گروه خانواده اکسیژن – گروه ۱۶ جدول تناوبی
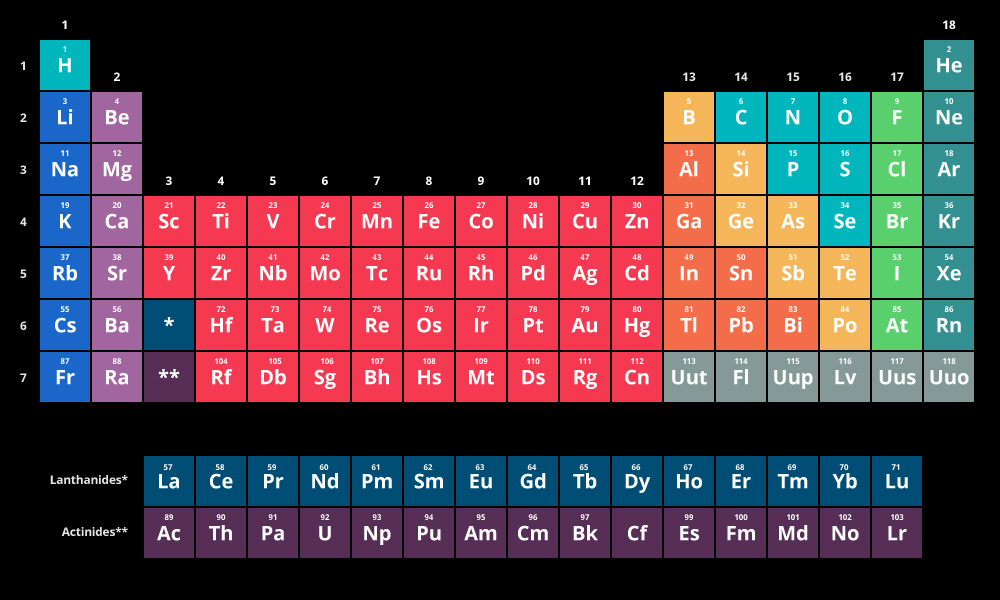
عناصر گروه ۱۶ جدول تناوبی شامل اکسیژن، گوگرد، سلنیوم، تلور و پولونیم (رادیواکتیو) می باشد. آرایش الکترونی عناصر گروه ششم اصلی به ns۲np۴ ختم می شود.

اکسیژن و گوگرد غیر سمی و مفید هستند اما عناصر سنگین تر این گروه سمی و خطرناک اند. در این مقاله نشریه جهان شیمی فیزیک به بعضی از رفتارها و خواص عناصر این گروه می پردازیم.
فهرست مطالب
تاریخچه پیدایش اکسیژن
اولین عنصر گروه ۱۶ جدول تناوبی گازی است بی رنگ، بی بو و بی مزه که اکسیژن نام دارد. وجود این گاز برای حیات تمام جانداران بسیار ضروری است. این عنصر اولین بار توسط شیل با آزمایش سوزاندن اکسید منگنز کشف شد. هم زمان با او دانشمندی به نام پریستلی با تابش مستقیم نور خورشید به اسیدمرکوریک به وجود هوایی پی برد که می توانست سوختن را با شدت بیشتری انجام دهد. در نهایت آنتوان لاوازیه بود که به ماهیت واقعی اکسیژن پی برد.
خواص اکسیژن
اکسیژن با گرفتن دو الکترون و تبدیل شدن به یون O۲- به آرایش اوکتت می رسد و ترکیبات یونی مثل CaO را به وجود می آورد و همچنین می تواند با عناصر دیگر پیوندهای کووالانسی یگانه یا دوگانه تشکیل دهد. اگرچه پیوند O-O در مولکول اکسیژن پیوند قوی است با این اکسیژن می تواند در بسیاری از واکنش ها شرکت کند. اکسیژن عدد اکسایش 2- را دارد به جز مواردی استثنا که اعداد اکسایش ۰، ۱- و ½- دارد. در مولکول OF۲ چون فلوئور الکترونگاتیوتر از اکسیژن است عدد اکسایش اکسیژن ۲+ و در O۲F۲ برابر ۱+ است.

تهیه اکسیژن
بیشترین مقدار اکسیژن از راه تقطیر جزء به جزء هوای مایع حاصل می شود. در آزمایشگاه اکسیژن را از تجزیه حرارتی کلرات پتاسیم در مقابل کاتالیزورMnO۲ به دست می آورند.
2KClO۳(l) → 3O۲(g) + 2KCl(s)
همچنین اکسیژن را می توان از الکترولیز آب تولید کرد. گاز اکسیژن را به شکل مایع داخل مخزن هایی نگهداری می کنند.
ترکیبات اکسیژن
اوزون
آلوتروپ اکسیژن اوزون با فرمول مولکولی O۳ است که یک اکسنده ی قوی است و می تواند فلزاتی مثل نقره و جیوه را اکسید کند. این مولکول گازی است به رنگ آبی روشن که در حالت مایع به رنگ آبی تیره می شود. اوزون طبق واکنش زیر تشکیل می شود.
3O۲(g) → 2O۳(g)
تغییرات آنتالپی واکنش ۲۸۵ کیلوژول می باشد.
واکنش اکسیژن با هیدروژن ( آب و هیدروژن پروکسید)
آب
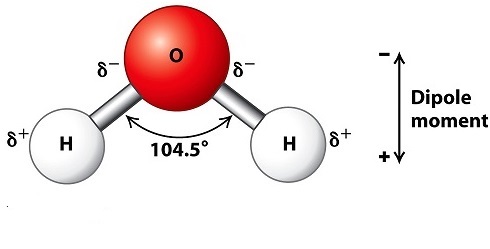
مولکول آب از پیوند دو اتم هیدروژن به یک اتم اکسیژن با زاویه ۱۰۵ درجه ساخته شده است. پیوند H-O اختلاف الکترونگاتیوی زیادی داشته و بسیار قطبی است پس آب یک مولکول قطبی است. وجود گشتاور دوقطبی زیاد در آب باعث شده که اتم های اکسیژن وهیدروژن آن دارای بار جزئی به ترتیب منفی و مثبت بوده و توانایی تشکیل پیوند هیدروژنی داشته باشد. پس در حالت مایع مولکول های آب با پیوند هیدروژنی در کنار یکدیگر قرار می گیرند و این پیوندها مدام در حال شکسته شدن و تشکیل شدن می باشند. در حالت جامد هر اتم اکسیژن با چهار اتم هیدروژن پیوند هیروژنی و کووالانسی دارد که دریک آرایش منظمی قرار گرفتند که همین ساختار منظم باعث منبسط شدن یخ شده و یخ روی آب شناور می ماند. یکی دیگر از خصوصیات آب قابلیت حلالیت آن است. آب خاصیت اکسندگی، کاهندگی، بازی و اسیدی دارد. همین رفتار آن را به یک ترکیب بی نظیر در جهان تبدیل کرده است.
پروکسید هیدروژن
در این ترکیب مولکول های کوووالانسی قطبی پروکسیدهیدروژن با پیوندهای هیدروژنی به یکدیگر متصل می شوند. پروکسید هیدروژن یک اکسید کننده قوی و کاهنده ضعیف می باشد. برای تهیه این ترکیب در صنعت ابتدا اسیدسولفوریک را با الکترولیز کردن به پروکسی دی سولفوریک اسید تبدیل می کنند و در مرحله بعد از واکنش پروکسی دی سولفوریک اسید با آب H۲O۲ حاصل می شود.
واکنش اکسیژن با عناصرگروه های مختلف جدول تناوبی
اکسید فلزات قلیایی
از ترکیب اکسیژن با فلزات قلیایی اکسیدها با فرمول M۲O ایجاد می شود همه این اکسیدها در آب خاصیت بازی دارند. لیتیم با اکسیژن با شعله قرمز می سوزد و درمقابل اکسیژن اضافی می تواند پراکسید تولید کند. سدیم در واکنش سوختن با اکسیژن شعله نارنجی پررنگ ایجاد کرده و محصول واکنش مخلوط اکسید سدیم Na۲O و پراکسید سدیم Na۲O۲ خواهد بود. از حرارت دادن پتاسیم در مجاورت هوا بدون شعله ورشدن پتاسیم پراکسید K۲O۲ و سوپراکسید KO۲ تولید می شود.
اکسید فلزات قلیایی خاکی
اکسیژن در گروه ۱۶ جدول تناوبی با فلزات قلیایی خاکی به جز بریلیم (به دلیل اندازه کوچک و انرژی یونش بالا) اکسیدهایی به فرمول MO را می دهند. برای انجام این واکنش گرما لازم است و اکسیدهای تولید شده حلالیت کمتری نسبت به اکسیدهای فلزات قلیایی در آب دارند. در بین این عناصر فقط استرانسیم و باریم می توانند در مقابل اکسیژن اضافی پراکسید تولید کنند. اکسیدهای فلزات قلیایی خاکی نیز مانند اکسیدهای گروه اول در آب تولید هیدروکسید می کنند که خاصیت قلیایی دارند.
اکسیدهای عناصر گروه های دیگر
عناصر گروه سوم اصلی با اکسیژن اکسیدهای با فرمول M۲O۳ می دهند که اکسیدهای فلزات این گروه درآب خاصیت بازی و اکسیدهای نافلزات آن ها در آب خاصیت اسیدی دارند. در این میان اکسید آلومینیم Al۲O۳ یک آمفوتر است.
کربن در واکنش با اکسیژن مونوکسید کربن و دی اکسید کربن می دهد. که هردو خاصیت اسیدی دارند. سیلیسیم با اکسیژن فقط SiO۲ تولید می کند که خاصیت اسیدی کمی دارد و حلالیتش در آب پایین است. بقیه اکسیدهای عناصر گروه ۱۴ خاصیت آمفوتری دارند.
توجه
عناصر گروه های بعدی جدول تناوبی با اکسیژن اکسیدهایی با فرمول های مختلف شیمیایی با خصوصیات مختلف می دهند. از این ترکیبات می توان به NO۲، N۲O۵، N۲O۳، P۴O۶، P۴O۱۰، O۲، O۳، SO۲ و نمونه های دیگر را نام برد. اما هالوژن ها اکسیدهایی که ایجاد میکنند بسیار ناپایدارند. به صورت پایدار هالوژن ها به جای اکسید با اکسیژن اکسی اسیدها را تولید می کنند.
خواص گوگرد
دومین عنصر گروه ۱۶ جدول تناوبی گوگرد است که در طبیعت به صورت ترکیبات سولفید و سولفات یافت می شود. این عنصر به صورت آزاد نیز در چشمه های آب گرم و مناطق آتشفشانی وجود دارد. این عنصر نافلز بوده، بسیار سبک و زرد کم رنگ است. به دو شکل گوگرد رومبیک و مونوکلینیک وجود دارد. در هنگام سوختن رنگ شعله را آبی کرده و هنگام ترکیب با هیدروژن بوی تخم مرغ فاسد شده را می دهد. گوگرد در آب نامحلول است و درحالت های مختلف دارای شکل های متفاوتی است که در حالت جامد ساختار حلقه گوگردی S۸ را دارد. وقتی گوگرد جامد گرما داده شود حلقه های S۸ تاحدی شکسته شده و زنجیرهای S۴ و S۶ می دهد. تمام آلوتروپ های گوگرد عایق الکتریسیته هستند.
از بین ۲۳ ایزوتوپ گوگرد ایزوتوپ های گوگرد-۳۲، گوگرد-۳۳، گوگرد- ۳۴، گوگرد-۳۶ و و ایزوتوپ رادیواکتیو گوگرد-۳۵ پایدارند. عددهای اکسایش گوگرد ۲-، ۲+، ۴+ و ۶+ است.
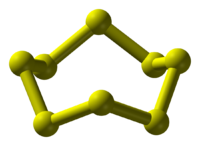
ترکیبات گوگرد
گوگرد تقریبا با تمام عناصر جدول تناوبی به جزء گازهای نجیب پیوند برقرار میکند.
اززواکنش گوگرد با هیدروژن، سولفید هیدروژن به دست می آید که گازی است بسیار سمی با بویی شبیه به تخم مرغ گندیده که در آب خاصیت اسیدی دارد. یکی از خواص مهم گوگرد تشکیل ویژگی زنجیری شدن آن است که از کاهش گوگرد حاصل می شود. از سوزاندن گوگرد اکسیدهای گوگرد مثل SO۲ و SO۳ حاصل می شود. اسیدهای حاصل از این اکسیدها به ترتیب اسید سولفورو H۲SO۳ و اسید سولفوریک H۲SO۴ می باشد. از هالیدهای گوگرد می توان گاز SF۶ را نام برد که در ترانسفورماتورها به عنوان گاز عایق کاربرد دارد. از ترکیبات نیتروژن دار تیوسیانات با فرمول مولکولی SCN– را داریم که از اکسیداسیون آن تیوسیانوژن حاصل می شود.
نکته
از ترکیب سولفیدهیدروژن با نمک های فلزی سولفیدهای فلزی حاصل می شود که نقش نیمه هادی دارند. از ترکیبات آلی این عنصر تیول ها (R-SH) و تیواترها (R-S-R) را داریم. اسید سولفونیک ها ترکیبات آلی دیگری هستند که در شوینده ها کاربرد دارند.
کاربردهای گوگرد
مهمترین کاربرد گوگرد از گروه خانواده نیتروژن در تولید اسیدسولفوریک است. از این اسید در تولید کودهای فسفاته، تصفیه آب و پالایش نفت استفاده می شود. دی سولفید حاصل از واکنش گوگرد با متان در تولید سلفون کاربرد دارد. از کلسیم سولفات آبدار در ترکیب سیمان استفاده می شود. همچنین از گوگرد در تولید کرم صورت، آنتی بیوتیک، پنی سیلین، مواد ضدعفونی کننده، ساخت کبریت، عامل ثابت کننده در عکاسی و همین طور تولید آفت کش و ضدقارچ استفاده می شود.
خواص و کاربردهای سلنیوم
عنصری که در گروه ۱۶ جدول تناوبی بین گوگرد و تلور قرار گرفته سلنیوم است. سلنیوم یک شبه فلز با عدد اتمی ۳۴ که بیشتر به حالت ترکیب در طبیعت وجود دارد. سلنیوم یک آنتی اکسیدان قوی است و وجودش برای بدن بسیار ضروری است. این عنصر هدایت الکتریکی چندین برابر در روشنایی نسبت به تاریکی دارد. از سلنیوم در صنایع الکترونیک، فتوکپی، رنگ سازی، عینک سازی، عکاسی، لاستیک سازی، داروسازی و پزشکی استفاده می شود. از اثرات آن روی بدن می توان به درمان ناباروری، ناراحتی های پوستی، حفظ جوانی، درمان سرطان و شوره سر اشاره کرد.
گروه های جدول تناوبی
طبقه بندی عناصر به شما در خواندن جدول تناوبی کمک می کند ساختار جدول تناوبی مدرن ممکن است برای ناظر معمولی عجیب به نظر برسد، اما طراحی آن هدفی را دنبال می کند. هر عنصر با توجه به وزن اتمی و عدد آن قرار می گیرد. ستون های عمودی گروه هستند و ردیف های افقی هستند.
گروه ها (ستون های عمودی)
عناصر بر اساس خواص شیمیایی آنها در ستون ها دسته بندی می شوند. یک عدد رومی – یا، در جدول تناوبی مدرن، یک عدد عربی – هر ستون را مشخص می کند. این تعداد الکترون هایی است که یک عنصر در لایه بیرونی خود دارد که به الکترون های ظرفیتی معروف هستند.
الکترون های ظرفیتی تعداد الکترون هایی هستند که یک عنصر برای پیوند با عناصر دیگر برای ساختن مولکول ها در دسترس است.
گروه ۱ متشکل از فلزات قلیایی است – چیزهایی مانند سدیم، پتاسیم و سزیم که به چگالی فلزات دیگر نیستند و بسیار واکنش پذیر هستند. برخی از آنها حتی در تماس با آب یا هوا منفجر می شوند.
گروه ۲ شامل فلزات قلیایی زمین مانند کلسیم و منیزیم است که به راحتی به یکدیگر متصل می شوند. اتم های آنها کوچکتر از اتم های گروه ۱ است.
گروه های ۳ تا ۱۲ فلزات انتقالی هستند. این گروه بیشتر جدول تناوبی را تشکیل می دهد. در سمت راست، برخی از فلزات و همچنین فلزات و نافلزها را خواهید یافت. متداول ترین نافلزات گروه ۱۷، هالوژن ها، و گروه ۱۸، گازهای نجیب هستند که با هیچ چیز پیوند ندارند. وقتی یک گروه را از بالا به پایین می خوانید، به عنوان “خواندن یک گروه” شناخته می شود.
دورهها (ردیفهای افقی)
اطراف هسته هر عنصر یک پوسته است که اوربیتال نیز نامیده می شود و فقط می تواند تعداد معینی الکترون را در خود نگه دارد. عناصر جدول تناوبی بر اساس تعداد پوسته هایی که دارند به ردیف ها تقسیم می شوند. به عبارت دیگر، تمام عناصر یک دوره دارای تعداد اوربیتال های اتمی یکسانی هستند.
سنگین ترین نافلز گروه ۱۶
سلنیوم یکی از نافلزهای سنگین گروه شانزدهم جدول تناوبی است که جایگاه ویژه ای در شیمی معدنی و صنایع پیشرفته دارد. این عنصر جز عناصر کمیاب موجود در طبیعت است معمولاً از پالایش مس و دیگر فلزات سنگین به دست می آید. سلنیوم دارای چندین آلوتروپ است که هر یک خصوصیات متفاوتی از جمله رنگ، رسانایی و پایداری شیمیایی نشان میدهند و بطور گسترده در حوزه فناوری مورد استفاده قرار می گیرند. حساسیت به نور سلنیوم باعث شده که زمینه هدایت الکتریکی و توسعه سلولهای خورشیدی و فتوسل های مورد توجه قرار بگیرد.
سلنیوم به عنوان سنگین ترین نافلز گروه ۱۶ از نظر زیستی نیز بسیار مهم است و در برخی آنزیم های آنتی اکسیدان و فرایندهای حیاتی مانند تنظیم عملکرد غده تیروئید مشارکت دارد. با اینحال سلنیوم یک نافلز سمی است که فقط به مقدار بسیار کم در چرخه زیستی و غذایی اهمیت دارد. توانایی سلنیوم در تشکیل ترکیبات گوناگون، از جمله سلنیدها و سلناتها همواره مورد توجه دانشمندان بوده است تا اثرات آن بر سلامت انسان مشخص شود.



















