ترمودینامیک چیست؟ – قوانین آن و تعاریف مفاهیم ترمودینامیکی
ترمودینامیک به عنوان علمی جامع به مطالعه و بررسی گرما و انرژی می پردازد. این علم شامل بسیاری از دستگاه های کوچک و بزرگی چون جامدات، گاز الکترونی، موجودات زنده، خورشید و موارد دیگر می شود. چون به طور تقریبی تمام قوانین در فیزیک به نوعی با صحبت از انرژی، بیان می شوند، پس این علم بدون ترمودینامیک نمی تواند پیش برود. این علم به مطالعه و بررسی انرژی حرکتی و نحوه انتقال انرژی در حرکت می پردازد. این مقاله نشریه جهان شیمی فیزیک ما را با ترمودینامیک و قوانین مربوط به آن آشنا می کند.
ترمودینامیک چیست؟
علمی که به مطالعه انرژی و گرما پرداخته و در واقع دو کلمه ترمو و دینامیک تشکیل دهنده آن هستند که به معنای نیروی گرما است، ترمودینامیک نامیده می شود. این علم مربوط به انرژی، دما و آنتروپی می شود. این که انرژی چگونه می تواند در اتم ها، گردبادها و سیاه چاله ها منتقل شود را با این علم می توان توضیح داد. با قوانین ترمو دینامیک می توانیم به توضیح علت از بین نرفتن انرژی و همچنین به چگونگی تبدیل آن به شکل های مختلف پرداخت. مهمتر از همه این که با استفاده از قانون دوم این علم، به پایان رسیدن جهان هستی به اثبات می رسد.
این علم می تواند با استفاده از متغیرهای قابل مشاهده ای چون دما، آنتروپی، فشار و انرژی داخلی، حالت های مواد و قوانینی که بین آن ها وجود دارد و همچنین روابط موجود در بین آن ها را توضیح می دهد. مطالعه درباره انرژی، تبدیل آن به حالت های مختلف و توانایی انرژی برای انجام کار در علم ترمو دینامیک بیان می شود.

در اینجا ابتدا به تعریف مفاهیمی می پردازیم که در بیان قوانین این علم به ما کمک می کند.
تعریف انرژی و جرم
به توانایی انجام کار، انرژی می گویند که به دو نوع انرژی جنبشی و پتانسیل تقسیم می شود. واحد انرژی بر حسب ژول بیان می شود. یک ژول برابر است با نیرویی یک نیوتنی که می تواند جسمی را به اندازه یک متر جابجا کند. صورت های مختلفی از انرژی به شکل انرژی گرمایی، شیمیایی، هسته ای، گرانشی، الکتریکی، مغناطیسی و … وجود دارد.
به مقدار ماده ای که یک جسم دارد، به عنوان جرم جسم تعریف می شود. به عبارتی با استفاده از حد و میزان مقاومت یک جسم در برابر نیروی وارد شده از طرف آن، می توان به اندازه گیری آن پرداخت. از نیروی گرانشی زمین در هنگام تعیین جرم یک جسم، صرف نظر می شود.
میزان جرم و انرژی در یک سیستم ثابت و تغییرناپذیراست، این را به عنوان قانون نسبیت جرم و انرژی می شناسند. در این قانون (E = mc۲) که به قانون اینشتین معروف است، جرم و انرژی نه تولید می شود و نه از بین می رود. بلکه فقط می تواند از شکلی به شکل دیگر تبدیل شود.
تعریف گرما، انتقال آن و کار
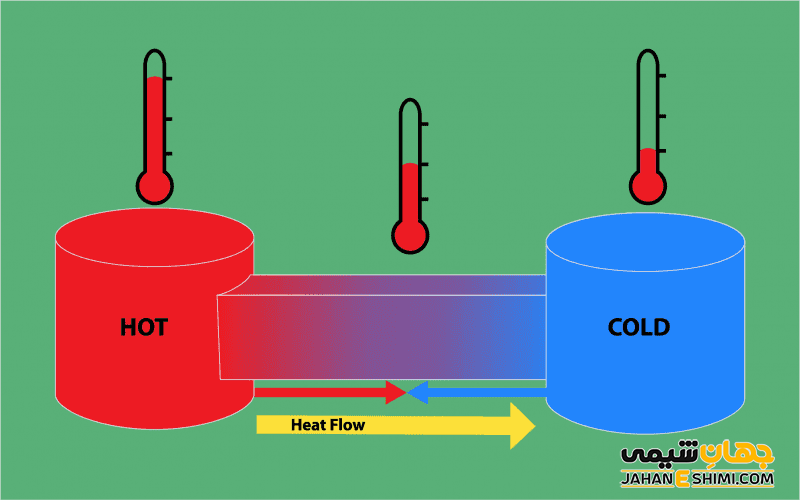
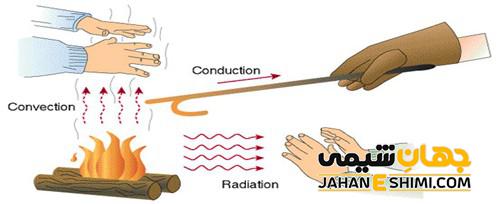
همان طور که گفته شد، انرژی می تواند به صورت های دیگر تبدیل شود. یکی از شکل های انرژی، گرما است. به وجود آمدن گرما به شکل خود به خودی نبوده و هیچ وقت نیز از بین نمی رود. وقتی در یک محیط اختلاف دما وجود داشته باشد، گرما از جایی که دمای بالایی دارد به محیطی با دمای کمتر منتقل می شود. انتقال گرما می تواند به سه روش رسانش، همرفت و یا تابش صورت بگیرد.
عامل انجام کار، نیرو است. نیروی وارد شده بر جسمی ساکن که می تواند در جهت وارد شدن آن نیرو، حرکت کند، عامل انجام کار است. مقدار کار را که با واحد ژول بیان می شود از رابطه زیر به دست می آورند.
W = F.d
یعنی حاصل ضرب نیرو در جابه جایی، کار است. کار تابع مسیر بوده و وابسته به سابقه سیستم است.
تعادل ترمودینامیکی
تعادل ترمودینامیکی را برای یک سیستم مجزا و یا چند سیستمی که در ارتباط با هم هستند تعریف می کنند. به شرایطی که در درون سیستم و یا بین سیستم ها، هیچ اثری از جریانی از ماده و انرژی وجود نداشته باشد. وقتی تعادل ترمودینامیکی در یک سیستمی برقرار باشد، یکی و یا همه تعادل های حرارتی، تابشی، گرمایی و شیمیایی نیز در آن سیستم حکم فرماست. از شرایط برقراری این تعادل موارد زیر است.
وقتی یک سیستمی ایزوله باشد، میزان آنتروپی آن بالاترین حد خواهد بود و سیستمی دارای حجم و دمای ثابتی باشد، میزان انرژی آزاد هلموهلتز در آن کمترین مقدار است. اما سیستمی با دارا بودن حجم و فشار ثابت، دارای کمترین مقدار انرژی آزاد گیبس خواهد بود.
قوانین ترمودینامیک
علم ترمو دینامیک به مطالعه گرما و نسبت آن با گرما و انرژی پرداخته و علم انرژی و آنتروپی است. با استفاده از قوانین این علم می توان نیازهای کار و انرژی تعریف می شود. برای اولین بار قوانین ترمو دینامیک در قرن نوزدهم میلادی، همزمان با انقلاب صنعتی به وجود آمد.
قانون اول ترمودینامیک
طبق این قانون جرم و انرژی به وجود نمی آیند و از بین هم نمی روند. بلکه فقط می توانند به شکل های مختلفی از هم تبدیل شوند. جامد، مایع، گاز و پلاسما شکل های تبدیلی این مواد و انرژی به همدیگر است. به عبارتی بر اساس این قانون ورودی و خروجی هر ماشینی با هم برابر است.
با توجه به این قانون می توان گفت که تغییرات انرژی یک سیستم برابر است با انرژی ورودی منهای انرژی خروجی سیتم است.
E = Ein – EOUT∆
براساس این قانون تغییرات انرژی محیط به اضافه تغییرات انرژی سیستم برابر با صفر خواهد بود.

قانون دوم ترمودینامیک
از نظر فلسفی قانون دوم ترمو دینامیک دارای اهمیت زیادی است تا جایی که برخی بر این عقیده استوارند که از راه این قانون می توان ثابت کرد که دنیا متناهی و تمام شدنی است. این قانون که به قانون آنتروپی نیز معروف است به دو شکل بیان می شود. وجود نقص در قانون اول را از این موضوع که نمی تواند درباره کیفیت انرژی و جهت انتقال آن اطلاعاتی ارائه دهد، می توان متوجه شد. چون قانون اول ترمو دینامیک درباره کمیت انتقال انرژی بحث می کند و برای امکان واقع شدن یک واکنش و یا این که این واکنش انجام نشود، نمی تواند کافی باشد.
دو صورت بیان قانون دوم
٭ اولین شکل بیان به این ترتیب است که هیچ تاثیری نمی تواند بر یک سیستم و محیط، طوری باشد که تمام گرمایی را که جذب کرده تبدیل به کار کند.
٭ دومین بیان این است که در هیچ عملکردی نمی توان از یک سطحی که دمای کمتری دارد، گرما را به سطحی دیگر که دمای بالایی دارد، منتقل کرد.
به عبارتی بر طبق این قانون گرما به کار تبدیل می شود ولی این تبدیل نمی تواند به شکل صد در صد باشد یعنی در تبدیل تمام گرما به کار، محدودیت وجود دارد.
با بیان کلوین می توان گفت، بازده و راندمان ۱۰۰٪ را در هیچ ماشین گرمایی نمی توان یافت.
با بیان کالوزیوس نیز می توان گفت که هیچ ماشین و وسیله ای را نمی توان درست کرد که بتواند گرما و حرارت را از یک محیط یا مخزنی با دمای کم به مخزنی دیگر با دمای زیاد منتقل کند.
مثالی در درک مفهوم قانون اول و قانون دوم ترمودینامیک
وقتی یک فنجان چای در یک اتاقی گذاشته شود، به مرور سرد می شود. این فرایند را با این توصیف که انرژی که به هوای اطراف فنجان منتقل می شود برابر همان انرژی است که چای از دست می دهد. این موضوع بیان کننده قانون اول است. اما چون فنجان چای نمی تواند به مرور میزان گرمای بیشتری به دست آورد، نقص قانون اول است. این اتفاق مربوط به قانون دوم و پدیده آنتروپی است. چون قانون دوم بیان کننده مهم بودن کیفیت در کنار کمیت بوده و نشان دهنده یک جهتی بودن فرایند است.
سیستم ترمودینامیکی
به مجموعه ای از وسیله ها برای بررسی ماده، یک سیستم ترمو دینامیکی گفته می شود. هر سیستم از یک حجم محدودی تشکیل شده است که با یک مرز موهومی یا غیر موهومی از بقیه محیط دنیا سوا می شود. مرز رابط بین سیستم و محیط برای تبادل گرما، کار و یا ماده است. چها رنوع مرز ساده، قابل حرکت، حقیقی و موهومی وجود دارد. تغییراتی که در انرژی درونی سیستم به واسطه عبور ماده، گرما و یا انرژی به وجود می آید، باید در معادله موازنه انرژی لحاظ شود.
انواع سیستم های ترمودینامیکی
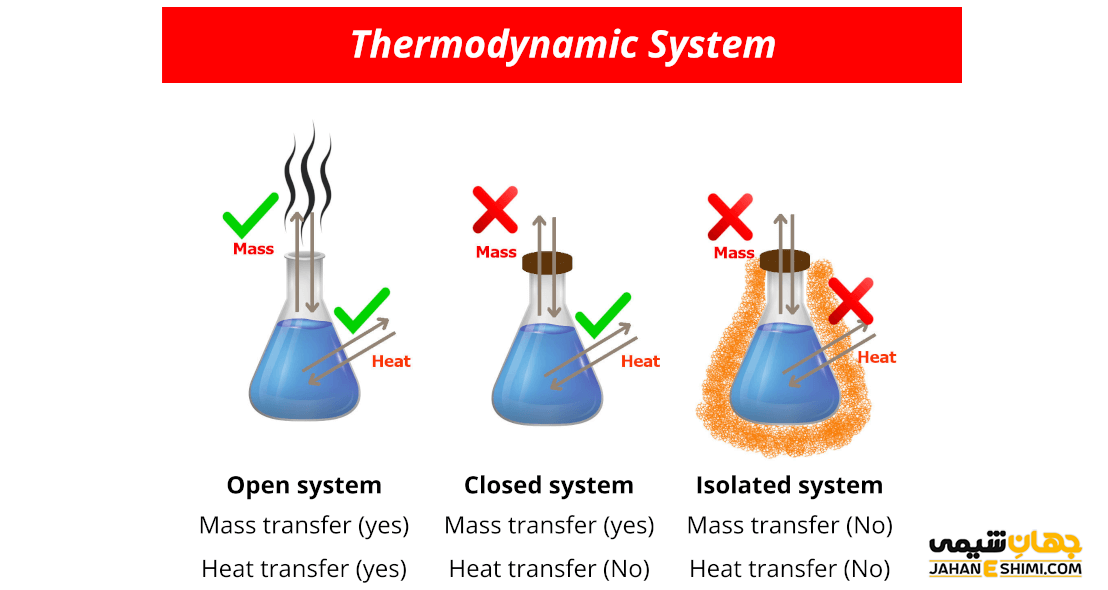
سیستم ایزوله که در این نوع از سیستم ها هیچ تبادل ماده و انرژی بین سیستم و محیط وجود ندارد. نوع دیگر سیستم بی دررو است که در این نوع از سیستم ها، گرما از مرز توانایی عبور ندارد. مورد بعدی سیستم هادی است که در این سیستم بر خلاف سیستم بی دررو، گرما از مرز عبور می کند. اما سیستم بسته مورد بعدی است که ویژگی این سیستم عدم عبور ماده از مرز سیستم است. سیستم باز هم نوعی است که در این سیستم از مرز سیستم و محیط، ماده، کار و گرما عبور می کند.
دسته بندی ترمودینامیک
ترمو دینامیک را می توان به دو دسته کلاسیک و آماری تقسیم کرد.

کلاسیک
از دیدگاه میکروسکوپی در نوع کلاسیک از این علم، کمیت هایی مانند سرعت، انرژی، جرم و اندازه حرکت مد نظر قرار می گیرد. درک این حواس از طریق حواس پنجگانه امکان ندارد. اما از دیدگاه ماکروسکوپی خواصی که از طریق حواس پنجگانه قابل درک و در آزمایشگاه قابل اندازه گیری است، مورد بررسی قرار می گیرد.
آماری
مقدارهای متوسطی برای همه ذره های موجود در سیستم با توجه به نظریه های موجود در آمار و احتمال در نظر گرفته می شود. در این نوع از ترمو دینامیک، عمل مطابق با در نظر گرفتن مدلی از اتم مد نظر، انجام می شود. از خواص و ویژگی هایی که ذرات تشکیل دهنده یک سیستم و برهمکنش هایی که بین آن ها با محیط وجود دارد، می توان خواص ماکروسکوپی مانند انرژی، فشار، حجم، دما و آنتروپی را به دست آورد. علاوه بر این می توان با استفاده از ترمو دینامیک آماری، قوانین ترمو دینامیکی از نظر کمیت با زبان مکانیک آماری، در صورت تعریف کمیت های ماکروسکوپی بر اساس کمیت های میکروسکوپی، قابل بیان خواهد بود.
انواع فرآیندهای ترمو دینامیکی
در صورت یکی بودن حالت ابتدایی و انتهایی یک فرآیند، به آن فرآیند چرخه ای می گویند. اگر گرمایی بین مرزهای سیستم عبور کند، فرآیند را بی دررو می گویند. وقتی حجم سیستم ثابت باشد، فرآیند را هم حجم می گویند. فشار سیستم ثابت باشد، فرآیند را هم فشار می گویند. دمای سیستم ثابت باشد، فرآیند را هم دما می گویند.
ترمودینامیک در زندگی
ترمودینامیک مطالعه انتقال گرما و انرژی است. این روی بسیاری از جنبههای روتین ما تأثیر میگذارد، از نحوه پختن وعدههای غذایی گرفته تا راحتی محیط های داخلی. ترمودینامیک نقش مهمی در فرآیند پخت و پز دارد، جایی که انتقال حرارت و کنترل دما ضروری است. هنگام پخت و پز روی اجاق گاز یا فر، ترمودینامیک بر انتقال گرما از منبع گرما به غذا نظارت می کند. به عنوان مثال، هنگام جوشاندن آب ماکارونی، حرارت شعله اجاق گاز به قابلمه منتقل می شود و باعث افزایش دمای آب می شود. ترمودینامیک همچنین بر روشهای پخت و پز مانند پخت و کباب کردن تأثیر میگذارد، جایی که مکانیسمهای همرفت، هدایت و انتقال حرارت تشعشع برای پخت یکنواخت و کارآمد غذا مورد استفاده قرار میگیرند. در اجاقهای مایکروویو، ترمودینامیک بر جذب تشعشعات مایکروویو توسط مولکولهای آب در غذا نظارت میکند که منجر به گرم شدن و پخت سریع میشود.
ترمودینامیک برای عملکرد سیستم های تبرید و تهویه مطبوع که در حفظ محیط های داخلی راحت و حفظ کالاهای فاسد شدنی مفید هستند، مرکزی است. این سیستم ها از اصول ترمودینامیکی مانند فشرده سازی، تراکم و تبخیر برای انتقال گرما از مکانی به مکان دیگر استفاده می کنند. به عنوان مثال، در یک یخچال، یک کمپرسور گاز مبرد را فشرده می کند و دما و فشار آن را افزایش می دهد. همانطور که گاز از طریق سیم پیچ های کندانسور جریان می یابد، گرما را به هوای اطراف آزاد می کند و باعث می شود که آن را به مایع تبدیل کند. مبرد مایع سپس از طریق یک دریچه انبساط جریان می یابد، جایی که با تغییر فاز به گاز کم فشار، گرما را از داخل یخچال جذب کرده و آن را خنک نگه می دارد. در واحدهای تهویه مطبوع، فرآیند مشابهی برای حذف گرما از هوای داخلی رخ می دهد و راحتی خنک کننده را در هوای گرم فراهم می کند.



















با سلام رابطه جریان های ترمودینامیک با تئوری آشوب خوبی معلوم وآشکار نشده است وبا اینک با جریانات ناشناخته ای روبرو هستم که ماهیت آنها نمی دانیم ، برای همکاری آماده ام