
در علم ترمودینامیک، اثر ژول- تامسون (Joule–Thomson effect) به تغییرات دمای ایجاد شده در آنتالپی ثابت و در اثر تغییرات فشار گفته می شود. این پدیده در واقع نشان دهنده تغییرات ترمودینامیکی در گازها یا مایعات، در هنگام عبور از یک دریچه متخلخل یا ولو است. به عبارت دیگر، اثر ژول- تامسون که با نام های اثر کلوین- ژول (Kelvin-Joule effect)، اثر ژول- کلوین (Joule-Kelvin effect) و یا انبساط ژول- تامسون (Joule-Thomson expansion) نیز شناخته می شود، در حقیقت تغییر دمای یک سیال که از یک منطقه با فشار بیشتر به سمت منطقه با فشار کمتر جریان دارد، می باشد. در ادامه این مقاله در نشریه جهان شیمی فیزیک به بررسی اثر ژول- تامسون پرداخته می شود. لطفا با ما همراه باشید.
فهرست مطالب
تاریخچه
این اثر به افتخار جیمز پرسکات ژول (James Prescott Joule) و ویلیام تامسون (William Thomson, 1st Baron Kelvin) که آن را برای اولین بار در سال ۱۸۵۲ میلادی کشف کردند، نامگذاری شده است. این اثر در حقیقت پس از کار قبلی ژول در مورد انبساط ژول، که در طی آن یک گاز ایده آل در خلا تحت انبساط آزاد قرار می گیرد و دما بدون تغییر است، دنبال شد.

فرآیند ژول- تامسون
فرآیند ژول-تامسون (Joul-Thomson process)، چگونگی کاهش دمای یک گاز را در طی فرآیند انبساط آدیاباتیک و برگشت پذیر بررسی می کند. هدف از این انبساط، بررسی قانون سوم ترمودینامیک است. در فرآیند انبساط ژول تامسون، آنتالپی سیستم ثابت خواهد بود. بنابراین تحول مورد بررسی یک تحول ایزوآنتالپیک (انبساط هم آنتالپی) نامیده می شود. در اینجا، سیستم مورد بررسی ایزوله نگه داشته می شود، پس با محیط اطراف هیچ انتقال حرارتی ندارد. جالب است بدانید که به این فرآیند، فرآیند خفقان (throttling process) نیز گفته می شود.
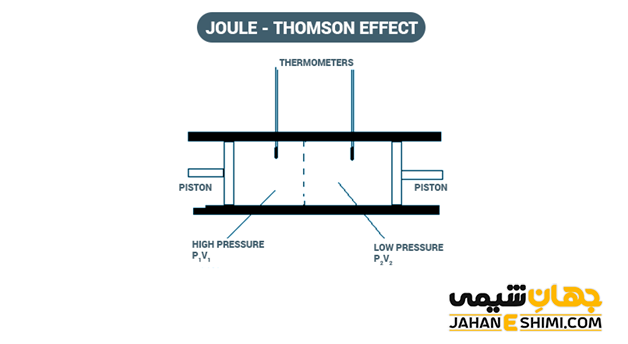
در پدیده ژول- تامسون، دما و فشار نسبت مستقیمی با یکدیگر دارند. بنابراین اگر فشار به بیرون نشت پیدا کند، فشار کم شده و با کاهش آن، دما نیز کاهش پیدا می کند. در نتیجه محیط سرد می شود. به عبارت دیگر، یکی از نتایج اثر ژول- تامسون، کاهش دمای گاز طبیعی (همزمان با کاهش فشار) در خطوط لوله خواهد بود. این کاهش دما عاملی برای یخ زدگی این خطوط محسوب می شود. به طور کلی، در دمای اتاق، همه گازها (به استثنای گازهای هیدروژن، هلیوم و نئون) در اثر فرآیند ژول- تامسون سرد می شوند.

فرآیند خفقان اهمیت فنی بالایی دارد. زیرا این فرآیند در حقیقت قلب ماشین های حرارتی همچون یخچال، پمپ حرارتی، کولر گازی و میعان کننده ها محسوب می شود. لازم به ذکر است که فرآیند خفقان یک فرآیند غیر قابل بازگشت است. بنابراین در خطوط ورودی (به ویژه نواحی اتصالات فلنجی)، مبدل های حرارتی، ری ژنراتور ها و یا سایر اجزای ماشین های حرارتی به عنوان یک منبع تلفات در نظر گرفته می شود که می تواند کارایی دستگاه را محدود کند. با سفت کردن پیچ و مهره های فلنج بالا، تعویض رینگ یا اسپیریال وسط دو فلنج و در نهایت رفع نشت، در کمترین زمان یخ آب می شود.
آزمایش ژول- تامسون
در آزمایش ژول تامسون، یک سیستم منزوی که امكان تبادل كار و گرما با محیط اطراف ندارد را در نظر بگیرید. سیستم به کمک یك جداره كه سوراخ های بسیار ریزی دارد، به دو بخش تقسیم می شود. سیستم در دو طرف، دارای دما و فشار نامساوی است. روش انبساط ژول- تامسون به اینصورت است که در طی آن، یک گاز یا مایع در فشار P1 به ناحیه ای با فشار پایین تر P2 بدون تغییر قابل توجهی در انرژی جنبشی جریان یابد. فرآیند ذاتا برگشت ناپذیر است. به علاوه در طول این فرآیند، آنتالپی بدون تغییر باقی می ماند. فرآیند تا زمان انتقال کامل گاز یا مایع به طرف ناحیه کم فشار، ادامه پیدا می کند. اگر در فرآیند انبساط، گاز نیتروژن مورد استفاده قرار گیرد، در نهایتT2 < T1 خواهد شد. به بیان ساده تر، همزمان با فرآیند انبساط، گاز سرد شده است.
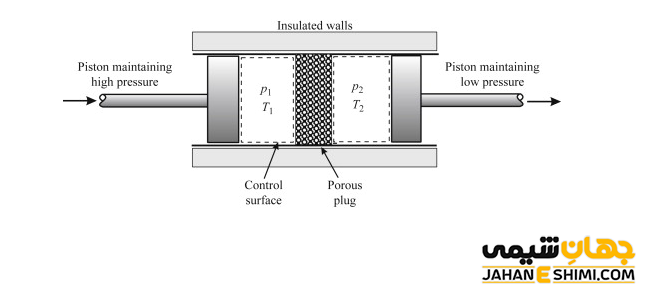
در این سسستم کار انجام می شود که باعث تغییر در انرژی داخلی خواهد بود. اینکه انرژی داخلی در نهایت افزایش یا کاهش یابد، با انجام کار بر روی سیال یا توسط سیال تعیین می شود. انرژی داخلی به وسیله حالت های اولیه و نهایی انبساط و همچنین خواص سیال تعیین می گردد. کار انجام شده در این فرآیند انبساط، مجموع کار انجام شده در هر بخش است. معادله کار انجام شده را می توان به صورت زیر نوشت:
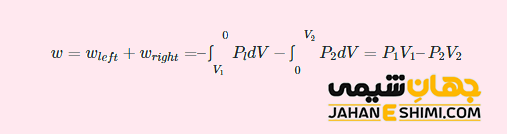
از آنجاییکه سیستم ایزوله است، بنابراین تبادل گرما وجود ندارد. از این رو می توان این رابطه را به شکل زیر، بازآرایی کرد:

ضریب ژول- تامسون
ضریب ژول تامسون (µJT) به صورت تغییرات دما (dT) نسبت به تغییرات فشار (dP) در آنتالپی ثابت تعریف می شود. این ضریب برای هر گاز، یك مقدار خاص است که مقدار آن به ذات گاز بر میگردد.
(تغییرات فشار / تغییرات دما) = ضریب ژول تامسون
µJT= (T2-T1) / (P2-P1)
اگر ضریب ژول- تامسون مثبت باشد، در نتیجه کاهش فشار باعث کاهش دما می گردد. به بیان دیگر، انبساط گاز باعث سرد شدن و تراکم گاز مورد بررسی باعث گرم شده آن می شود. زیرا مثبت بودن ضریب ژول تامسون نشان دهنده هم جهت بودن دما و فشار است. در حالیکه، اگر ضریب ژول- تامسون منفی باشد، کاهش فشار سبب افزایش دما می شود. به عبارت دیگر، انبساط گاز سبب گرم شدن و تراکم آن سبب سرد شدن گاز می شود. زیرا منفی بودن ضریب ژول تامسون نشان دهنده غیر هم جهت بودن دما و فشار می باشد.

مقدار این ضریب در اغلب گاز ها، به استثنای هلیم و هیدروژن، مثبت است. همانطور که مشخص است، ضریب ژول تامسون خاصیتی شدتی خواهد بود. زیرا در واقع نسبت تغییرات دو خاصیت شدتی را نشان می دهد. مقدار تجربی این ضریب از اندازه گیری تغییرات دما و فشار گاز مورد بررسی بین دو لحظه متفاوت بدست می آید. این ضریب را همچنین می توان از نظر حجم گاز (V)، ظرفیت حرارتی آن در فشار ثابت (CP ) و ضریب انبساط حرارتی آن (α) به صورت معادله زیر بیان کرد.

واحد ضریب ژول تامسون بیشتر بر حسب کلوین بر پاسکال یا درجه سانتیگراد بر پاسکال ذکر می شود. همانطور که بیان شد، این ضریب به نوع گاز، دما و فشار گاز قبل از انبساط بستگی دارد.
ضریب ژول- تامسون گاز ایده آل
ضریب ژول- تامسون گاز های کامل یا ایده آل، صفر است. زیرا آنتالپی یک گاز به دمای آن بستگی دارد. بر طبق تعریف، یک گاز کامل به گازی گفته می شود که نیرو های بین مولکولی آن صفر باشد. در این صورت، تراکم و یا انبساط یک گاز که موجب تغییر فاصله میان مولکول ها می شود، انرژی درونی سیستم را تغییر نخواهد داد. در نتیجه تغییرات گرمایی نیز وجود ندارد.
اما در واقعیت به دلیل برهمكنش بین ذرات گاز، گاز كامل وجود ندارد. بنابراین مقدار این ضریب می تواند مثبت یا منفی باشد. در حقیقت، علامت آن بر حسب نوع گاز و تابع دما و فشاری است که بر گاز مورد نظر اعمال شده است. اگر ضریب ژول تامسون، در دستگاه (T-P) رسم شود، یک منحنی بسته سهمی شکل ایجاد می گردد که بر روی این منحنی، ضریب ژول- تامسون برابر با صفر است.
دمای وارونگی
دمای وارونگی ژول- تامسون (Joule–Thomson inversion temperature) به دمایی گفته می شود که در آن دما، علامت ضریب ژول تامسون تغییر کند. جالب است بدانید که تمام گاز های واقعی، یک نقطه وارونگی دارند. دمای این نقطه، به فشار گاز قبل از انبساط بستگی دارد.
همانطور که بیان شد، اگر ضریب ژول تامسون را در دستگاه (T-P) رسم کنید، یک منحنی بسته سهمی شکل ایجاد می شود. به بیان ساده تر، دمای وارونگی در مرز منحنی تغییرات دما بر حسب فشار قرار می گیرد. در این دما، ضریب ژول- تامسون از منفی به مثبت تغییر می کند. در یک فشار معین، خط هم فشار تغییر دما، منحنی رسم شده را در دو نقطه مختلف قطع می کند. به این دو نقطه، دمای پایین و دمای بالای وارونگی گفته می شود. در حقیقت در دما های بالاتر و پایین تر از این دو دما، علامت ضریب ژول تامسون منفی و در بین این دو دما، علامت ضریب ژول تامسون مثبت می باشد.
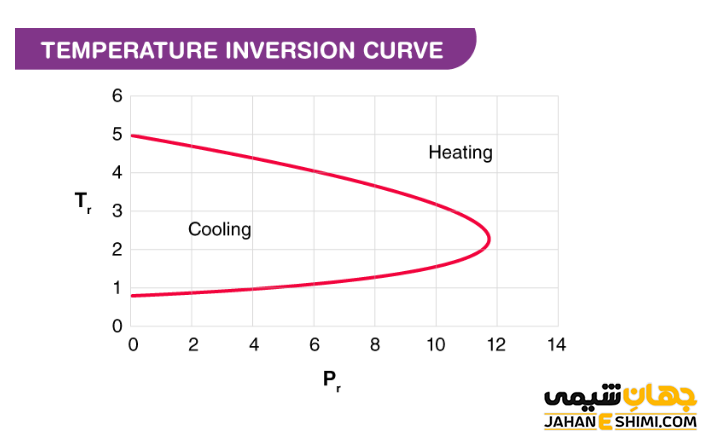
اگر دمای گاز مورد نظر با دمای وارونگی برابر باشد، در نتیجه ضریب ژول تامسون برای آن گاز صفر خواهد بود. چنین گازی تحت تاثیر فشار یا حجم قرار نمی گیرد. در واقع، گاز های ایده آل در هنگام انبساط در آنتالپی ثابت، گرم یا سرد نمی شوند. پس انرژی یک گاز کامل فقط به دما وابسته است. منحنی وارونگی ژول- تامسون در فرآیند های صنعتی بسیار مهم است. زیرا آگاهی از علامت ضریب ژول- تامسون می تواند تغییرات دما در فرآیند های هم انتالپی را پیش بینی کند.
کاربرد ها
ضریب و منحنی ژول- تامسون در طراحی و یا اجرای خطوط لوله و همچنین فرآیند های صنعتی مانند جابجایی گاز طبیعی مورد استفاده قرار می گیرند. به عبارت دیگر، یکی از نتایج بسیار مهم اثر ژول- تامسون در حقیقت کاهش دمای گاز طبیعی به صورت همزمان با کاهش فشار آن گاز در خطوط لوله می باشد. این کاهش، عاملی برای یخ زدن این خطوط محسوب می شود. کاربرد ضریب ژول- تامسون بیشتر در یخچال ها و سرد کننده ها است. اثر ژول- تامسون به عنوان یک فرآیند استاندارد در تکنیک لینده (Linde technique) در صنایع پتروشیمی کاربرد دارد. در این صنایع، از اثر ژول تامسون برای میعان کردن گاز ها و یا کاربرد های برودتی همچون تولید اکسیژن مایع، آرگون و نیتروژن استفاده می کنند.
ضریب ژول تامسون گاز طبیعی
ضریب ژول تامسون اندازه گیری تغییر دمای گاز هنگام انبساط یا فشرده شدن آن در شرایط آنتالپی ثابت است و در درک رفتار گاز در ترمودینامیک بسیار مهم است. این به طور گسترده در تبرید و کاربردهای برودتی مورد استفاده قرار می گیرد، زیرا تعیین می کند که دمای گاز با توجه به فشار، به ویژه در طی فرآیندهای انبساط یا فشرده سازی، چگونه تغییر می کند.
ضریب ژول- تامسون اندازه گیری تغییر دمای گاز هنگام انبساط یا فشرده شدن در شرایط آنتالپی ثابت است. این به ما کمک می کند تا بفهمیم دمای گاز با توجه به فشار آن چگونه تغییر می کند.
ضریب ژول تامسون (μ) به عنوان مشتق جزئی دما (T) با توجه به فشار (P) در آنتالپی ثابت (H) تعریف می شود. از نظر ریاضی به صورت: μ = (∂T/∂P)ᵣ = (ΔT/ΔP)_(H ثابت) که ΔT تغییر دما، ΔP تغییر در فشار است، و زیرنویس “r” نشان می دهد.
ضریب ژول تامسون به طور گسترده در کاربردهای تبرید و برودتی استفاده می شود. این به ما کمک می کند تا بفهمیم گازها چگونه دما را در هنگام انبساط تغییر می دهند، که در طراحی سیستم های خنک کننده و مبدل های حرارتی بسیار مهم است. اثر Joule-Thomson اساس بسیاری از فرآیندهای تبرید از جمله مواردی است که در تهویه مطبوع و یخچال استفاده می شود.
۱.ضریب ژول تامسون برای گازهایی که در اثر انبساط سرد می شوند (مانند بیشتر گازهای واقعی) مثبت و برای گازهایی که در اثر انبساط گرم می شوند منفی است (مثال: هیدروژن و هلیوم در دمای اتاق). ۲. برای یک گاز ایده آل، ضریب ژول تامسون صفر است، به این معنی که هیچ تغییری در دما در هنگام انبساط یا تراکم در آنتالپی ثابت وجود ندارد. این به این دلیل است که گازهای ایده آل هیچ نیروی بین مولکولی یا اثر اندازه مولکولی ندارند.



















