گشتاور دوقطبی یا ممان دوقطبی چیست؟ – گشتاور دوقطبی ذرات بنیادی
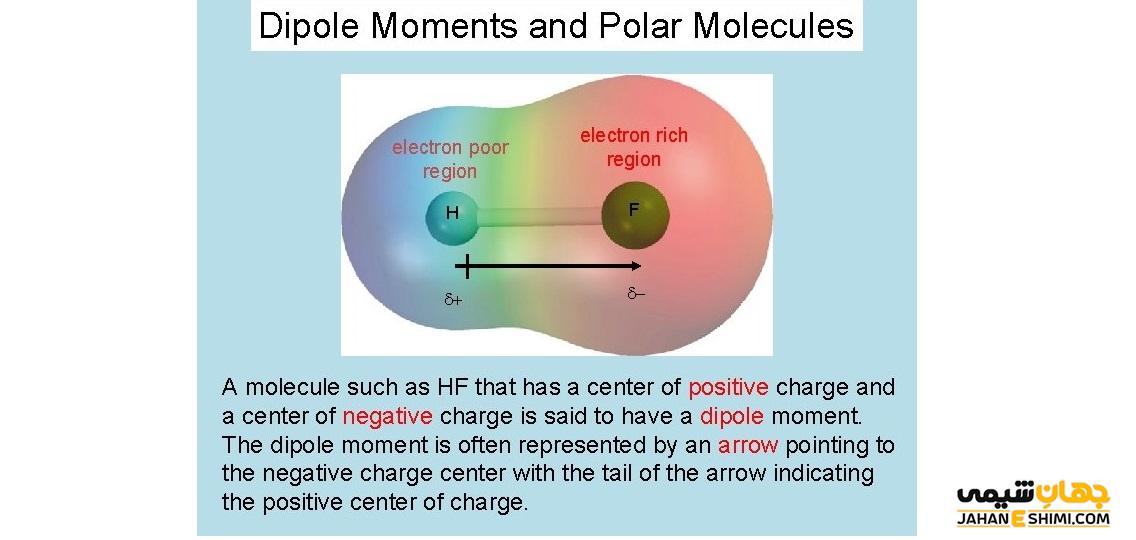
به معیار سنجش و اندازه گیری قطبیت یک پیوند، گشتاور دوقطبی یا ممان دوقطبی می گویند. به عبارتی قطبیت کلی سیستم و جدایی بارهای الکتریکی مثبت و منفی در یک سیستم با استفاده از گشتاور دوقطبی اندازه گیری می شود. در SI واحدی که برای اندازه گیری گشتاور دوقطبی یا ممان دوقطبی به کار می رود، کولن متر (C.m) است. واحد اندازه گیری این کمیت در فیزیک و شیمی اتمی، دبی (D) است. به تعریف گشتاور دوقطبی یا ممان دوقطبی در این مقاله نشریه جهان شیمی فیزیک می پردازیم.
فهرست مطالب
قطبیت پیوند
اتم های عناصر مختلف می توانند الکترون ها را به سمت خود بکشند که به توانایی آن ها در میزان کشش الکترون ها به سمت اتم ها، الکترونگاتیوی می گویند. الکترونگاتیوی در یک گروه از جدول تناوبی با حرکت از بالا به پایین به علت افزایش میزان شعاع، کاهش می یابد. همچنین میزان الکترونگاتیوی عناصر در یک دوره از جدول تناوبی با حرکت از چپ به راست جدول، به دلیل زیاد شدن بار موثر هسته، افزایش می یابد. با این تعریف، فلوئور به عنوان الکترونگاتیوترین عناصر و سزیم به عنوان الکتروپوزیتیوترین عناصر در جدول تناوبی است.

بر این اساس می توان گفت، فلزات عناصری هستند که الکترونگاتیوی کمتر از اتم هیدروژن دارند و نافلزات عناصری با الکترونگاتیوی بیشتر از هیدروژن هستند. اما عناصری که الکترونگاتیوی آن ها در حدود هیدروژن است به نام شبه فلزات خوانده می شوند. وقتی پیوندی بین دو اتم با اختلاف الکترونگاتیوی تشکیل می شود، جفت الکترون های پیوندی با کشیده شدن به سمت اتم الکترونگاتیوتر، آن را دارای بار جزئی منفی می کنند. اتم دیگر که ابر الکترونی در اطراف آن کمتر شده است، دارای بار جزئی مثبت می شود. این پیوند قطبی است.
توجه
اگر بین دو اتم تشکیل دهنده پیوند، هیچ اختلاف الکترونگاتیوی وجود نداشته باشد، در این هنگام پیوند، قطبی خواهد بود. مانند پیوندی که بین دو اتم یکسان مانند هیدروژن تشکیل می شود. در نتیجه مولکول هیدروژن (H۲) یک مولکول غیرقطبی است.
گشتاور دوقطبی چیست؟
یک شیء را در فیزیک می توان به صورت یک نقطه متمرکز نشان داد. وقتی دو نقطه باردار که یکی بار +q و دیگر بار –q داشته باشند، در فاصله ی r از هم قرار گیرند، تشکیل یک دوقطبی الکتریکی را می دهند. جهت دو قطبی از سمت بار منفی به بار مثبت است. در فرمول گشتاور دوقطبی ممکن است به جای r از s استفاده شود. در واقع s همان فاصله هر بار تا مرکز دوقطبی بوده و به اندازه نصف r است. پس در فرمول گشتاور دوقطبی به جای r باید از 2s استفاده کرد. فرمول محاسبه گشتاور دوقطبی یا ممان دوقطبی به شکل زیر است.
r ͯ δ = μ
در این فرمول اندازه بار بر حسب esu و فاصله بین آن ها بر حسب سانتی متر بیان می شود. فرمول گشتاور دوقطبی در کل از حاصل ضرب قدر مطلق بار الکتریکی در میزان فاصله دو بار الکتریکی از هم به دست می آید. وجود قدر مطلق در فرمول نشان می دهد که عدد به دست آمده برای ممان دوقطبی، همیشه مثبت و غیر منفی است. مقدار صفر به دست آمده از فرمول گشتاور دوقطبی نشان دهنده غیرقطبی بودن مولکول است. اما اگر به دست آمده از این فرمول بزرگتر از صفر باشد، مولکول قطبی است.
گشتاور پیوند
گشتاور پیوند در مولکول های دو اتمی، برابر و مساوی با گشتاور دوقطبی مولکول خواهد بود. مقدار گشتاور دو قطبی که در یک پیوند خاص وجود دارد، یکسان در ترکیبات مختلف خواهد بود. همچنین هر چه اختلاف الکترونگاتیوی دو اتم تشکیل دهنده یک پیوند، بیشتر باشد میزان گشتاور دو قطبی یا ممان دوقطبی آن بیشتر می شود. مقدار گشتاور دو قطبی در پیوند دو اتمی هیدروژن – کربن، به علت نزدیک بودن مقدار الکترونگاتیوی این دو اتم، کم است. طول پیوند نیز در این دو اتم کوتاه است. اما در مورد پیوند کربن- کلر، چون اختلاف الکترونگاتیوی این دو اتم زیاد است (الکترونگاتیوی کربن برابر ۲,۵ و برای کلر برابر ۳)، مقدار ممان دو قطبی، عدد بزرگی است.
به دلیل بزرگتر مقدار الکترونگاتیوی کلر نسبت به کربن، جفت الکترون پیوندی بیشتر به سمت کلر کشیده می شود. در نتیجه کلر دارای بار جزئی منفی و اتم کربن در این پیوند، دارای بار جزئی مثبت می شود. در نتیجه پیوند کربن – کلر یک پیوند قطبی خواهد بود. پیوندهای چندگانه ای که بین اتم ها وجود دارد، گشتاور دوقطبی بزرگی دارند. به عنوان مثال پیوند دو گانه ای که بین دو اتم کربن و اکسیژن در ترکیب آلی متانال وجود دارد، ممان دو قطبی بزگی داشته و این پیوند، قطبی است. همچنین پیوند سه گانه کربن – نیتروژن نیز به دلیل داشتن مقدار ممان دو قطبی بالا، پیوندی به شدت قطبی است.
گشتاور دوقطبی در مولکول های چند اتمی
در یک مولکول چند اتمی، بیشتر از یک پیوند وجود دارد. بنابراین تعیین قطبیت مولکول فقط با تعیین قطبیت یک پیوند و تعیین مقدار گشتاور دو قطبی آن امکان پذیر نیست. در این مولکول ها، ممان دو قطبی کل مولکول از جمع برداری ممان های دوقطبی پیوندهای تشکیل دهنده آن ها به دست می آید. به عبارتی دو عامل قطبیت پیوند و شکل هندسی مولکول، تعیین کننده قطبیت یک مولکول است. وقتی ممان های دو قطبی پیوندهای تشکیل دهنده یک مولکول، به شکل برداری جمع شوند می توانند به گشتاور دو قطبی کل مولکول برسند.
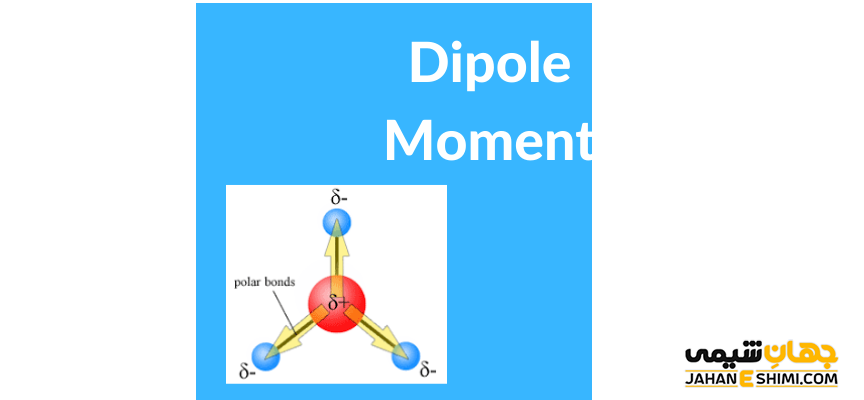
گشتاور دوقطبی یا ممان دوقطبی در مولکول های غیرقطبی
مثالی که در اینجا برای فهم درک ممان دو قطبی یک مولکول چند اتمی به کار برده می شود، دی اکسید کربن است. در این مولکول دو پیوند قطبی دو گانه کربن – اکسیژن وجود دارد. در این پیوند، جهت ممان دو قطبی از سمت اتم الکتروپوزیتیو کربن به سمت کربن الکترونگاتیو اکسیژن است. چون این دو فلش در اندازه های برابر و در جهت مخالف هم هستند، با خنثی کردن اثر یکدیگر، ممان دو قطبی کل مولکول را برابر صفر می کنند.
نمونه ای دیگر از مولکول چند اتمی که دارای ممان دو قطبی کل برابر با صفر است، تتراکلرید کربن است. در این مولکول چهار پیوند قطبی کربن- کلر وجود دارد ولی برآیند جمع برداری گشتاور دوقطبی آن ها در کل مولکول برابر صفر و مولکول غیر قطبی خواهد بود.
گشتاور دوقطبی یا ممان دوقطبی در مولکول قطبی
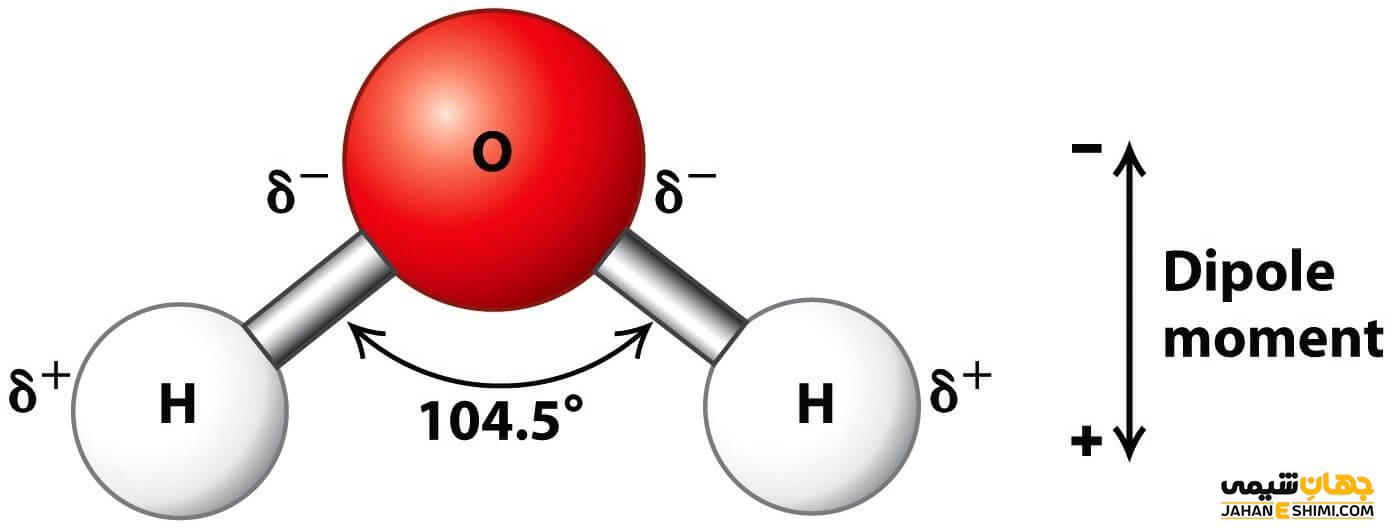
مولکول آب به عنوان مولکولی قطبی، از پیوند بین اتم های اکسیژن و هیدروژن تشکیل شده است. اختلاف الکترونگاتیوی بین این دو اتم برابر با ۱,۲ است. با توجه به بالا بودن میزان الکترونگاتیوی اکسیژن، جفت الکترون های پیوندی به سمت این اتم کشیده می شود. همچنین اتم اکسیژن دارای جفت الکترون های ناپیوندی است. پس در نتیجه جهت ممان دوقطبی به سمت اتم اکسیژن خواهد بود. با ضرب اختلاف بار بین دو اتم اکسیژن و هیدروژن در فاصله ای که بین آن ها وجود دارد، مقدار گشتاور دوقطی یا ممان دوقطبی مولکول آب به دست می آید که برابر با ۱,۸۴ دبی است.
گشتاور دوقطبی ذرات بنیادی
آزمایشاتی که برای اندازه گیری گشتاور دوقطبی الکتریکی در ذرات بنیادی انجام می گیرد با آزمایشاتی که مربوط به اسپین است متفاوت است. در آزمایشات اسپینی، گشتاورهای مغناطیسی ذرات بنیادی (الکترون ها و نوترون ها) مورد توجه است. مقدارهایی که برای گشتاور دوقطبی الکتریکی ذرات به دست می آید، وابسته به تخلف CP در طبیعت نیست. چون گشتاور دوقطبی الکتریکی، ناقض تقارن ضریب پاریته و تقارن در معکوس پذیری زمان است.
تعریف مولکول قطبی و غیرقطبی
به مولکولی، قطبی گفته می شود که بارهای مثبت و منفی در دو سر مولکول داشته باشد. وقتی بارهای مثبت و منفی، به طور مساوی در یک مولکول قرار نگرفته باشد، آن را قطبی می کنند. در این مولکول ها، چگالی الکترون ها در یک سمت بیشتر از سمت دیگر بوده و مرکز بارهای مثبت و منفی بر هم منطبق نیستند. شرط قطبی بودن یک مولکول، یکی داشتن حداقل یک پیوند کووالانسی قطبی است و دیگری این است که برایند بردارهای ممان دوقطبی برابر با یک عددی غیرصفر باشد.
مولکول غیرقطبی، مولکولی است که برآیند تمام بردارهای ممان دوقطبی پیوندهای آن، صفر شود. در این مولکول ها، الکترون های پیوندی و چگالی الکترون ها به طور مساوی بین اتم ها قرار می گیرد. در نتیجه گشتاورهای دوقطبی، یکدیگر را خنثی می کنند. با توجه به مثال تتراکلرید کربن که در بالا بررسی شد، با این که پیوندهای تشکیل دهنده این مولکول، قطبی است اما کل مولکول غیرقطبی است. مولکول هایی که دو یا چند اتم یکسان و جورهسته دارند، غیرقطبی هستند. این موضوع از شروط غیرقطبی بودن مولکول هاست. دو شرط دیگر، یکی نبود جفت الکترون غیرپیوندی در اتم مرکزی و دیگری یکسان بودن تمام اتم های چسبیده به اتم مرکزی است.
گشتاور دوقطبی آلکان ها
یک مولکول قطبی دارای بارهای مجزایی در ساختار مولکولی خود است. برای تعیین قطبی بودن یک مولکول، باید تمام دوقطبی های پیوند موجود در مولکول را بررسی کنیم. اگر پیوند دوقطبی وجود نداشته باشد، مولکول غیرقطبی است. اگر دوقطبی های پیوندی در مولکول وجود داشته باشد، باید به جهت گیری آنها در فضای سه بعدی نگاه کنیم. برای مولکول های دو اتمی، تنها یک پیوند وجود دارد، بنابراین گشتاور دوقطبی پیوند آن قطبیت مولکولی را تعیین می کند. مولکولهای دواتمی جور هسته ای مانند Br2 و N2 هیچ تفاوتی در الکترونگاتیوی ندارند، بنابراین گشتاور دوقطبی آنها صفر است. برای مولکول های ناجور هسته ای مانند CO، یک گشتاور دوقطبی کوچک وجود دارد. برای HF، یک گشتاور دوقطبی بزرگتر وجود دارد، زیرا تفاوت بیشتری در الکترونگاتیوی وجود دارد.
هنگامی که یک مولکول حاوی پیوندهای متعدد است، هندسه باید در نظر گرفته شود. اگر آرایش پیوندها در یک مولکول باعث شود که گشتاورهای پیوند آنها خنثی شود (که حاصل جمع برداری صفر است)، مولکول غیرقطبی می شود. هر یک از پیوندها قطبی هستند، اما مولکول به طور کلی غیر قطبی است. گشتاور دوقطبی آلکان ها نیز به دلیل ناقطبی بودن این ترکیبات تقریبا صفر است.




















عالی بود
سپاس