عدد اتمی چیست و چه ویژگی هایی دارد؟
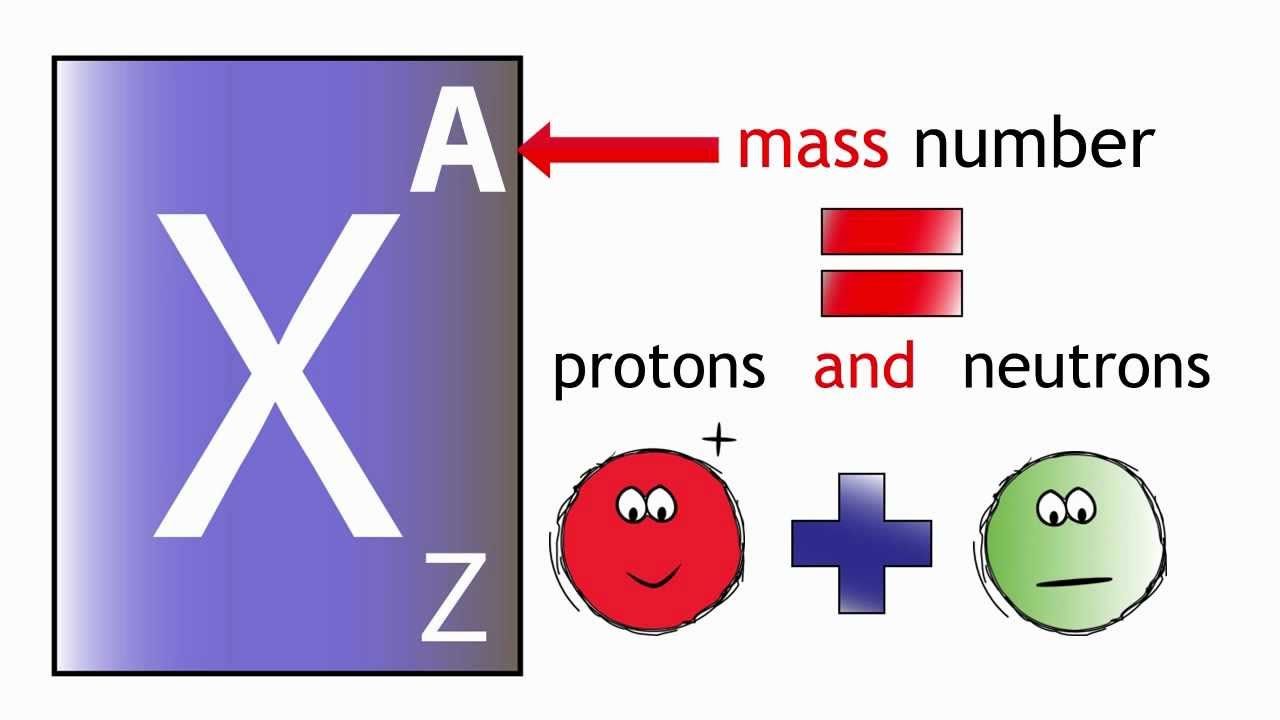
عدد اتمی که با Z نشان داده می شود به تعداد پروتون های یافت شده در هسته اتم یک عنصر اشاره دارد. عدد اتمی به طور منحصر به فرد یک عنصر شیمیایی را مشخص می کند و تعداد بارهای مثبت هسته را نشان می دهد. در یک اتم خنثی عدد اتمی یا همان پروتون ها برابر با تعداد الکترون است. مجموع عدد اتمی Z و تعداد نوترون های هسته ، عدد جرمی عناصر را تشکیل می دهد. در درس عدد اتمی چیست علوم هشتم و نهم و دهم این موارد بطور کامل شرح داده شده است.
اگر برای شما هم این سوال پیش آمده که چرا عدد اتمی را با Z نشان می دهند باید بگوییم که نماد متعارف Z از کلمه آلمانی Zahl به معنای عدد گرفته شده است. اتم هایی با عدد اتمی یکسان اما تعداد نوترون متفاوت و از این رو عدد جرمی متفاوت به عنوان ایزوتوپ شناخته می شوند. در واقع اندکی بیش از سه چهارم عناصر طبیعی به صورت مخلوطی از ایزوتوپ ها وجود دارند. در ادامه مقاله در نشریه جهان شیمی فیزیک توضیحات بیشتری در این رابطه ارائه می گردد لطفا همراه ما باشید.
فهرست مطالب
تاریخچه و روند کشف عدد اتمی
دیمیتری مندلیف ادعا کرد که اولین جدول تناوبی او که برای اولین بار در ۶ مارس ۱۸۶۹ منتشر شد بر اساس وزن اتمی مرتب شده است. اما با در نظر گرفتن خواص شیمیایی مشاهده شده از عناصر ، او ترتیب را کمی تغییر داد و تلوریم (وزن اتمی ۶/۱۲۷) را بالاتر از ید (وزن اتمی ۹/۱۲۶) قرار داد. این قرارگیری مطابق با روش مدرن است که عناصر را بر اساس عدد اتمی مرتب می کند.
با این حال ، یک شماره گذاری ساده بر اساس موقعیت جدول تناوبی هرگز کاملاً راضی کننده نبود. بعلاوه پس از ید و تلوریم ، بعداً مشخص شد که چندین جفت عنصر دیگر مانند آرگون و پتاسیم ، کبالت و نیکل دارای وزن اتمی تقریباً یکسان و وزن اتمی معکوس هستند ، بنابراین نیاز بود که محل قرارگیری آنها در جدول تناوبی توسط خواص شیمیایی آنها تعیین شود.
بعدها با شناسایی تدریجی عناصر لانتانید که عدد اتمی آنها مشخص نبود عدم تناسب و عدم اطمینان در شماره گذاری دوره ای عناصر حداقل از لوتتیوم (عنصر ۷۱) به بعد بیشتر شد.
بهتر است بدانید:
در سال ۱۹۱۱ ، ارنست رادرفورد مدلی از اتم ارائه داد که در آن هسته مرکزی بیشتر جرم اتم را در خود نگه داشته است. وی تخمین زد که طلا دارای بار مرکزی حدود ۱۰۰ (اما عنصر Z = 79 در جدول تناوبی بود) . یک ماه پس از انتشار مقاله رادرفورد ، آنتونیوس ون دن بروک ابتدا رسماً پیشنهاد کرد که بار اصلی و تعداد الکترون های یک اتم دقیقاً برابر با جای آن در جدول تناوبی است (همچنین به عنوان شماره عنصر ، عدد اتمی و نماد Z را معرفی کرد.
هنری موزلی مکان عناصر را در جدول تناوبی در سال ۱۹۱۳ با آزمایش مدلهای وان دن بروک و رادرفورد بهبود بخشید. وی طول موج داخلی ترین گذار فوتون تولید شده از عناصر آلومینیوم تا طلا را اندازه گیری کرد و مشاهده کرد که ریشه دوم فرکانس این فوتون ها به صورت تصاعدی افزایش می یابد. با این آزمایشات قانون موزلی بیان شد که می گفت Z به بار الکتریکی محاسبه شده برای هسته بسیار نزدیک است.
بعد از فوت این دانشمند Z تمامی عناصر از هیدروژن تا اورانیوم (Z=92) با همین روش اندازه گیری شد. در این محاسبات هفت اتم با عدد اتمی کمتر از ۹۲ وجود داشتند که هنوز کشف نشده بودند که بعدا بین سال های ۱۹۱۸ تا ۱۹۴۷کشف و در جدول تناوبی قرار گرفتند.
کشف نوترون و معرفی عدد اتمی
رادرفورد در سال ۱۹۱۷پس از بررسی هسته هیدروژن با واکنش هسته ای بین ذرات آلفا و گاز نیتروژن، ذرات هسته ای جدیدی را کشف کرد که آنها را پروتون نامید. موزلی نشان داد که هسته اتمهای سنگین، بیش از دو برابر جرم مورد انتظار از هسته هلیوم ، جرم دارند.
به همین دلیل دانشمندان فرض را بر این گذاشتند که هسته هلیوم از چهار پروتون بعلاوه دو الکترون هسته ای (Nuclear Electrons) تشکیل شده است. مثلا در رابطه با اتم طلا با هسته ای ۱۹۷ برابر سنگین تر از هیدروژن، فرض بر این بود که این اتم دارای ۱۱۸ الکترون هسته ای است تا بار +۷۹ را فراهم کند.
با کشف نوترون توسط جیمز چادویک در سال ۱۹۳۲ فرضیه های مختلف در این رابطه پایان یافت. بعد از این کشف مشخص شد اتم طلا دارای ۱۱۸ نوترون به جای ۱۱۸ الکترون هسته ای است. از سال ۱۹۳۲ به بعد عدد اتمی «Z» را به عنوان تعداد پروتون هسته در نظر گرفتند.
رابطه عدد اتمی با سطح انرژی اوربیتال
در یک اتم خنثی از روی Z می توان به تعداد الکترون ها پی برد. چون Z تعداد پروتون ها را نشان می دهد که با تعداد الکترون ها برابر است. به عنوان مثال، عدد اتمی کربن ۶ است بنابراین دارای ۶ الکترون است. همانطور که می دانید این ۶ الکترون در دو سطح انرژی با ۴ و ۲ الکترون قرار گرفته اند. یا عنصری با عدد اتمی ۱۲ از نظر ساختار الکترونی به ترتیب شامل ۲ و ۸ و ۲ الکترون خواهد بود یعنی ۲ الکترون در سطح انرژی داخلی، ۸ الکترون در سطح انرژی بعد و ۲ الکترون در بالاترین سطح انرژی. با یادگیری موارد فوق مسائل عدد جرمی و عدد اتمی را به راحتی جواب خواهید داد.
عدد اتمی در گازهای نجیب
بعضی از گروه های عناصر در جدول تناوبی از نظر خواص شیمیایی و فیزیکی بسیار مشابه هستند. یکی از این گروه ها گازهای نجیب هستند که شامل هلیم (He) ، نئون (Ne) ، آرگون (Ar) ، کریپتون (Kr) ، زنون (Xe) و رادون (Rn) است . این عناصر گازهایی بی رنگ و با واکنش پذیری پایین هستند که عدد اتمی آنها به ترتیب ۲ ، ۱۰ ، ۱۸ ، ۳۶ ، ۵۴ و ۸۶ است.
عدد اتمی در فلزات قلیایی
فلزات قلیایی گروهی ازعناصر با واکنش پذیری بالا هستند و شامل لیتیم (Li) ، سدیم (Na) ، پتاسیم (K) ، روبیدیم (Rb) ، سزیم (Cs) و فرانسیم (Fr) می باشند که عدد اتمی این عناصر به ترتیب ۳ ، ۱۱ ، ۱۹ ، ۳۷ ، ۵۵ و ۸۷ است.
عدد اتمی و جدول تناوبی
مقایسه اعداد اتمی عناصر در دو گروه ذکر شده یعنی گازهای نجیب و فلزات قلیایی نشان می دهد که اگر عناصر را به ترتیب افزایش Z در جدول تناوبی قرار دهیم به دنبال هر گاز نجیب ، یک فلز قلیایی قرار می گیرد. این ترتیب قرارگیری عناصر باعث می شود خواص مشابه عناصر نیز به طور تناوبی تکرارشود.



















