
این مقاله شامل اطلاعات مفید و کاربردی درباره ویژگیها، خواص و کاربرد بنزن و موارد مصرف گوناگون آن است. همچنین اگر تصمیم به خرید بنزن دارید، برای آگاهی یافتن از قیمت خرید و فروش بنزن در بازار مواد شیمیایی میتوانید از لیست پیشنهادی فروشندگان بنزن در انتهای مقاله استفاده نمایید. حجم محصول، درصد خلوص، نرخ ارز و شرکت تولیدکننده به طور کلی از عوامل بسیار مهم در تعیین قیمت مواد شیمیایی هستند؛ قیمت بنزن نیز تحت تاثیر این موارد است. لازم به ذکر است لیست فروشندگان پیشنهادی در پایان مقاله، همواره با اسامی معتبرترین شرکتهای خوشنام و با سابقه فعال در زمینه فروش بنزن به روزرسانی میشود.
در مباحث پیشین نشریه جهان شیمی فیزیک، مطالبی در خصوص هیدروکربن های آروماتیک ارائه شده است. ساده ترین و مهم ترین هیدروکربن آروماتیک تک حلقه ای، بنزن (Benzene) می باشد. فرمول شیمیایی این ترکیب به صورت C۶H۶ می باشد. بنزن در حقیقیت مایعی بدون رنگ، سمی، سرطان زا، در عین حال معطر با سرعت تبخیر بالا می باشد که قابلیت اشتعال فوق العاده بالایی نیز دارد. با توجه به ساختار ویژه و کاربردهای بنزن، این ترکیب به عنوان یکی از مهم ترین و در عین حال پر مصرف ترین ترکیبات آروماتیک شناخته می شود. در این مقاله ویژگی ها و خواص حلقه بنزن بیان می شود. در ادامه با ما همراه باشید.
فهرست مطالب
مراکز خرید و قیمت فروش بنزن در تهران و شهرستان ها
اغلب مراکز خرید و فروش بنزن و دیگر مواد شیمیایی در تهران وجود دارند و فروشندگان بنزن در سایر استان و شهرستان ها در بیشتر موارد، خرید خود را از تهران انجام می دهند. به همین دلیل، توصیه می شود که در صورت امکان سعی کنید تا خرید مواد شیمیایی از تهران انجام شود. چرا که
- اغلب شرکت های واردکننده بنزن در تهران مستقر هستند.
- به دلیل اینکه خرید بنزن در سایر استان ها و شهرستان ها در بیشتر موارد از طریق چندین واسطه انجام می شود، خرید در تهران می تواند از نظر قیمت مقرون به صرفه تر و ارزان تر باشد.
- از آنجایی که در تهران به تامین کننده اصلی کالا نزدیک تر هستید و بیشتر انبارهای اصلی مواد شیمیایی در شهر تهران قرار دارند، احتمال اصالت و مرغوبیت کالا نیز افزایش می یابد.
اما باید توجه نمود که تمامی شرکت های بازرگانی مستقر در تهران از نظر تجربه، سابقه و کیفیت در یک سطح قرار ندارند. به همین دلیل در این صفحه و سایر صفحات مرتبط با مواد شیمیایی در سایت جهان شیمی، تلاش کرده ایم برترین و باسایقه ترین شرکت های فعال در زمینه خرید و فروش بنزن را به شما معرفی کنیم. شرکت هایی که در بنر بالای این صفحه یا در کادر «فروشندگان پیشنهادی» در پایان این مقاله معرفی شده اند، همگی به طور مرتب مورد بازبینی قرار می گیرند. خالی از لطف نیست که یادآور شویم از جمله مهمترین شرایط شرکت ها برای قرار گرفتن در بخش های مذکور و معرفی به خریداران، میزان سابقه، اعتبار و تجربه آن ها است.
تاریخچه بنزن
بنزن برای اولین بار توسط مایکل فارادی (Michael Faraday) در قرن ۱۹ ام کشف شد. در واقع فارادی از گاز درخشان فشرده ای بنزن را جداسازی کرد و آن را بی کاربورت هیدروژن نامید.

این ترکیب در سال ۱۸۳۴ توسط شخص دیگری به نام آیل هارت میچرلیش (Eilhard Mitscherlich) با استفاده از گرما دادن بنزوئیک اسید با کلسیم اکسید سنتز شد. میچرلیش با اندازهگیری چگالی بخار بنزن، نشان داد که این ترکیب دارای فرمول مولکولی C۶H۶ می باشد. لازم به ذکر است که سال های زیادی طول کشید تا آرایش واقعی اتم ها و در نتیجه ساختمان بنزن معلوم گردد.

ساختار مولکولی بنزن
ساختار شیمیایی پیچیده بنزن سبب شده بود که توضیح و شناخت آن بسیار مشکل باشد. در واقع با توجه به فرمول مولکولی، ساختارهای متفاوتی برای بنزن پیشنهاد شد. برخی از آن ساختار ها با توجه به تعداد محصولات ایزومری مشتق شده از بنزن، رد و تعدادی دیگر مورد قبول قرار گرفتند. در نهایت ساختمان مولکول بنزن در سال ۱۸۶۵ توسط دانشمند آلمانی، ککوله (Kekule) در عالم رویا کشف شد.
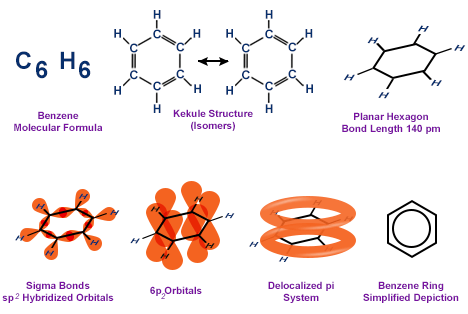
ککوله پیشنهاد کرد که بنزن یک مولکول حلقوی است. در این مولکول، شش اتم کربن هر کدام به یک اتم هیدروژن متصل اند و در نهایت یک ساختار شش ضلعی منتظم تشکیل می دهند. پیوند های کووالانسی تشکیل شده بین اتم های کربن به صورت یک در میان، یگانه و دو گانه می باشند. از آن جهت که طول پیوند های کربن – کربن در ساختار حلقه یکسان می باشند، ککوله پیشنهاد کرد جای پیوند های یگانه و دو گانه به سرعت عوض می شود. در حقیقت ککوله چیزی شبیه ساختار رزونانس امروزی بیان را بیان کرد.
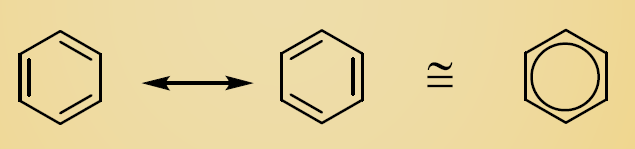
ساختار های پیشنهادی بنزن را در طول تاریخ در شکل زیر مشاهده می نمایید. این ساختارها به ترتیب از سمت چپ توسط آدولف کلوس (Adolf Cluss) در سال ۱۸۶۷، جیمز دیوئر (James Dewar) در سال ۱۸۶۷، آلبرت لادنبورگ (Albert Ladenburg) در سال ۱۸۶۹، هنری ادوارد آرمسترانگ (Henry Edward Armstrong) در سال ۱۸۸۷، یوهانس تیله (Johannes Thiele) در سال ۱۸۹۹ و فردریش آگوست ککوله در سال ۱۸۶۵ پیشنهاد شد.

بنزن در کجا یافت می شود
بنزن هم در طبیعت وجود دارد و هم توسط فعالیت های انسانی تولید می شود. این ترکیب در طبیعت از فوران ناگهانی آتش فشان ها و یا آتش سوزی جنگل ها به وجود می آید. اما این ترکیب از دود تنباکو، دود سیگار، بنزین، پمپ بنزین ها، گازهای منتشر شده صنعتی و خروجی اگزوز وسایل نقلیه موتوری نیز ایجاد می شود. علاوه بر آن، متاسفانه این ترکیب در هوای داخل ساختمان ها به دلیل استفاده از محصولاتی که حاوی این ماده می باشند (مانند چسب ها، رنگ ها، واکس مبلمان، شوینده ها و غیره) نیز وجود دارد.
روش های توليد بنزن + قیمت خرید و فروش بنزن
در گذشته از طریق حرارت دادن قطران زغال سنگ و در نهایت تبدیل بخار آن به مایع، بنزن تولید می شد. امروزه علاوه بر سنتز، می توان گفت که مهمترین منبع تهیه بنزن، نفت خام می باشد. در واقع از روش اصلاح کاتالیستی که در طی یک فرآیند شیمیایی نفت خام به محصولات مایع و هیدروکربن های آروماتیک تبدیل می شود استفاده می کنند. علاوه بر آن تعدادی از روش های تولید بنزن عبارتند از : ريفرمينگ کاتاليستی، تسهيم نا متناسب تولوئن و کراکينگ بخار.
جدول مشخصات، خواص و ویژگی های بنزن
| نام ماده | بنزن (Benzene) |
|---|---|
| فرمول مولکولی | C6H6 |
| جرم مولکولی | ۷۸.۱۱ g/mol |
| چگالی (دانسیته) | ۸۷۶ kg/m³ |
| نقطه جوش | ۸۰.۱ °C |
| دیگر نام ها | Benzol |
ویژگی های بنزن
از جمله ویژگی های بنزن می توان به موارد زیر اشاره کرد.
- این ترکیب در دسته مواد خوشبو و معطر (دارای رایحه خوب با بوی شیرین) قرار می گیرد.
- خصلت آروماتیک دارد.
- از قاعده هوکل پیروی می کند.
- گرمای سوختن و گرمای هیدروژن دار شدن پایینی دارد.
- به دلیل پایداری ساختار، تمایل زیادی برای شرکت در واکنش های افزایشی نشان نمی دهد. اما در واکنش های جانشینی شرکت میکند.
- این حلقه علاوه بر سرعت تبخیر بالا، قابلیت اشتعال زایی بالایی نیز دارد.
- حلالیت کم در آب، اما خودش به عنوان یک حلال آلی کاربرد دارد.
کاربرد بنزن
ویژگی های منحصر به فرد حلقه بنزن باعث شده است که کاربردهای زیادی در زندگی انسان داشته باشد. البته ذکر این نکته مهم است که کاربرد بنزن در گذشته بیش از زمان حال بود. این حلقه مدت ها در صنایع شیمیایی مختلف کاربرد داشت اما با ثابت شدن سرطان زا بودن آن، به کارگیری آن در صنایع شیمیایی مختلف ممنوع شد. در ادامه به چند کاربرد آن اشاره می کنیم.
- به عنوان ماده اولیه برای تولید مواد شیمیایی دیگر استفاده می شود. (به عنوان مثال در تولید سیکلوهگزان، اتیل بنزن، فنول، کیومن، نیتروبنزن، آلکیل بنزن و غیره).
- در صنعت چاپ کاربرد دارد. در واقع در ترکیب جوهر از بنزن برای حفظ حالت مایع جوهر استفاده می کنند.
- در صنایع تایرسازی و همچنین لاستیک سازی استفاده می شود.
- در صنایع کفاشی، برای چسباندن کفی کفش ها به عنوان چسباننده کاربرد دارد.
- در تولید مواد پلاستيکی، پلیمر ها، رزین ها، چسپ ها، استایرن، مواد مخدر، مواد منفجره و آفت کش ها استفاده می شود.
- از بنزن در روان کننده ها، پاک کننده ها به ویزه پاک کننده رنگ ها، لوسیون ها و به عنوان حلال برای از بین بردن چربی ها و تمیز کاری در فلزات صنعتی استفاده می شود. در واقع این ماده گریس های صنعتی را به راحتی در خود حل می کند بدون هیچگونه آسیبی به فلزات، تجهیزات هیدرولیکی و یا سیستم های سوخت.
- به عنوان ماده پیش ساز در تهیه شوینده ها، نایلون ها و الیاف نایلونی، رنگ ها و لاستیک مصنوعی کاربرد دارد.
پرسش های رایج در مورد بنزن
خرید بنزن در سایت جهان شیمی چگونه است؟
جهان شیمی شما را به بهترین فروشندگان بنزن متصل می کند. برای خرید بنزن تنها کافی است از طریق بنر بالای صفحه یا کادر فروشندگان در پایین مقاله، فروشنده مورد نظر را انتخاب نمایید و با او تماس بگیرید.
قیمت فروش مشتقات بنزن
همانطور که در ابتدای مقاله بیان شد، ساختمان بنزن شامل شش اتم کربن و شش اتم هیدروژن است که به صورت حلقه در کنار یکدیگر قرار گرفته اند. با جایگزینی یک یا چند اتم هیدروژن با گروه های عاملی مختلف، مشتقات بنزن به وجود می آیند. نام گذاری مشتقات بنزن کمی گیج کننده می باشد. زیرا در این مشتقات بیشتر از نام های رایج استفاده می کنند تا نام های آیوپاک. در ادامه به بررسی این مشتقات می پردازیم.
خرید مشتقات ساده بنزن
هنگامی که در ساختار حلقه، فقط یک گروه جایگزین شده باشد، مشتق ساده بدست می آید. در هنگام نامگذاری، معمولا نام گروه استخلافی را قبل از کلمه بنزن می نویسند.
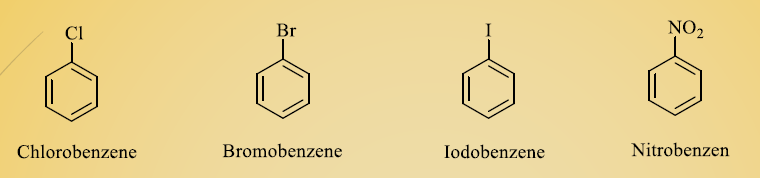
بعضی از مشتقات ساده بنزن اسامی خاصی دارند که تعدادی از آنها را در شکل زیر مشاهده می نمایید.
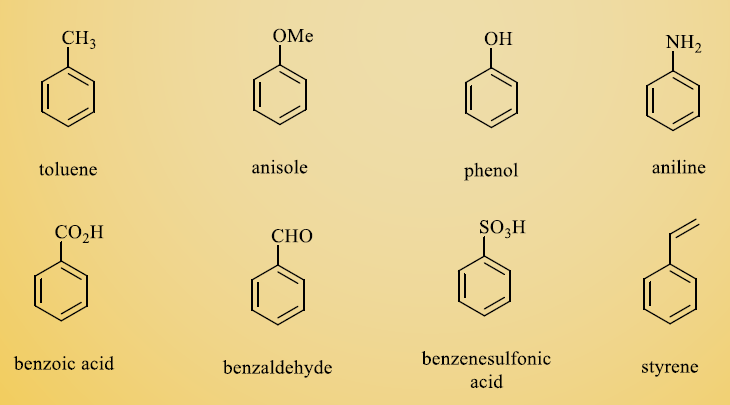
قیمت مشتقات جایگزین شده بنزن
هنگامی که دو موقعیت روی حلقه با یک اتم یا یک گروه جایگزین شود، این ساختار یک بنزن جایگزین شده می باشد. مشتقات دو استخلافی را با توجه به موقعیت استخلاف ها، به صورت اورتو، متا و یا پارا نامگذاری می کنند.
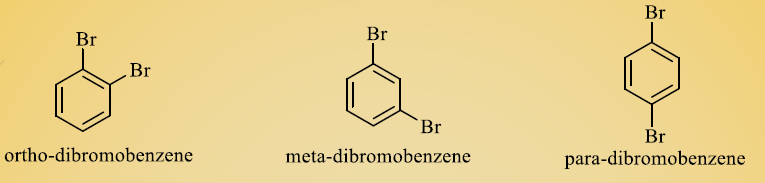
اگر یکی از دو گروه مختلفی که بر روی حلقه قرار گرفته اند، نام خاصی به مولکول دهد، در این صورت مولکول به صورت مشتقی از آن نامگذاری می شود. به عنوان مثال به مولکول های زیر دقت نمایید.
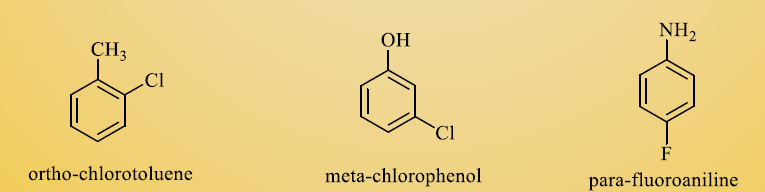
حال اگر هیچکدام از دو گروه مختلفی که بر روی حلقه قرار گرفته اند، نام خاصی به مولکول ندهند، دو گروه جایگزین شده را به ترتیب حروف الفبای لاتین نوشته و در آخر نام مولکول کلمه بنزن را ذکر می کنند.
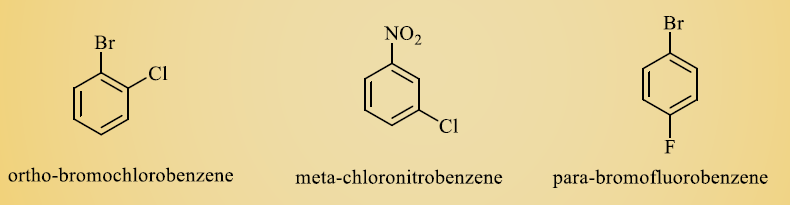
قیمت فروش مشتقات چند جانبه بنزن
هنگامی که بیش از دو موقعیت روی حلقه با یک اتم یا یک گروه جایگزین شود، این ساختار یک بنزن چند جانبه می باشد. در این دسته برای نامگذاری از اعداد استفاده می شود. حال اگر یک گروه جایگزین شده، به یک نام خاص مشهور است، نام مولکول به عنوان مشتق آن نام خاص است. در حالیکه اگر هیچ گروه جایگزین شده، به نام خاصی مشهور نیستند، آنها را به ترتیب حروف الفبا لیست کرده و کمترین مجموعه اعداد را به آنها اختصاص می دهیم.
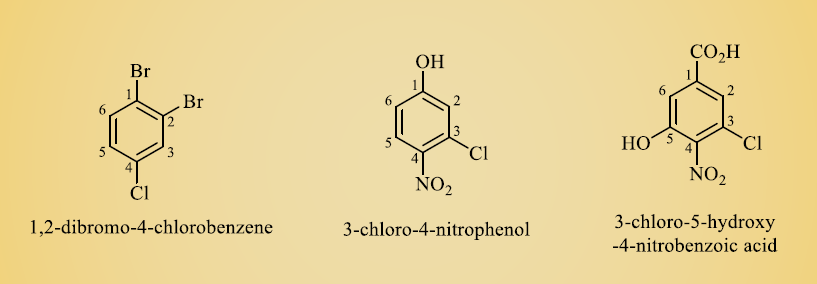
لازم به ذکر است که کاهش حق تقدم جهت نامگذاری مشتقات به صورت زیر می باشد :
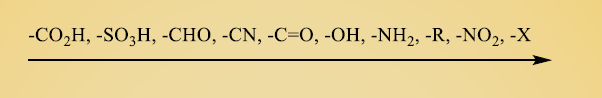
خطرات جدی برای بنزن سلامتی
سالهاست که حلقه بنزن به عنوان ترکیبی سرطان زا شناخته شده است. بنابراین تمام آزمایشات و کارهایی که شامل ترکیبات بنزن هستند را باید در زیر هود انجام داد و همزمان از دستکش های آزمایشگاهی استفاده کرد. قرار گرفتن در معرض دوز بسیار بالایی از این ماده می تواند حتی سبب مرگ شود. حال این سوال مطرح می شود که چگونه در معرض آن قرار می گیریم؟
- از طریق استنشاق بخارات و همچنین مقدار کمی از آن در دود سیگار وجود دارد
- از طریق بلعیدن
- از طریق نوشیدن منابع آب زیر زمینی آلوده
- از طریق تماس و جذب از راه پوست
لازم به ذکر است که مسمومیت با این حلقه دارای علایم مختلف و زیادی می باشد. به عنوان مثال در زیر اثرات مسمومیت با بنزن لیست شده است.
- اثرات مسمومیت از طریق استنشاق بنزن عبارتند از : خواب آلودگی، سردرد، گیجی و سرگیجه، افزایش ضربان قلب، رعشه و لرزش
- اثرات مسمومیت خوردن بنزن از طریق آب یا غذای آلوده عبارتند از : عدم تعادل، تهوع، استفراغ، سوزش معده، سرگیجه، سستی، خواب آلودگی، تشنج، افزایش ضربان قلب و احتمالا مرگ
- اثرات مسمومیت از طریق تماس با پوست: قرمزی، زخم شدن، سوزش و ناراحتی چشم و جراحات دردناک
به طور کلی قرار گرفتن مداوم در معرض بنزن، باعث به وجود آمدن مشکلات حادی از جمله تاثیرات مخرب بر روی بافت های سازنده سلول های خون، مغز و استخوان و همچنین تغییر در DNA انسان می شود. از جمله سایر عوارض تماس با بنزن می توان به کاهش خون سازی بدن، ناتوانی و ضعیف شدن سیستم ایمنی بدن، اختلال در سیستم تنفسی، سرطان خون، کم خونی، فراموشی مزمن، ناباروری، تولید تومورهای غدد لنفاوی و همچنین صدمه به کبد اشاره کرد.
بنزن و محیط زیست
بنزن در محیط زیست می تواند با مواد مختلفی واکنش داده و دود تولید کند. این ماده شیمیایی می تواند به قطره های باران یا برف متصل شده و آب و خاک را آلوده کند. از طرفی، آلودگی ناشی از آن در محیط های آبی، باعث تغییر در نوع و ظاهر ماهی ها و موجودات آبزی شده و طول عمر آنها را کاهش می دهد. علاوه بر آن انسان از غذاهای دریایی تغذیه می کند، بنابراین این آلایندگی می تواند وارد بدن انسان نیز شود. ذکر این نکته لازم است که رشد گیاهانی که در خاک های آلوده به بنزن زندگی می کنند، به شدت کاهش می یابد.
فروش بنزن صنعتی
بنزن صنعتی پایه مواد خام برای تولید پروپیلن اکسید و استایرن و مشتقات آن ( پلیالها و پروپیلن گلیکولها ) است. بنزن یک هیدروکربن مایع فرار، شفاف و قابل اشتعال با رایحه بسیار مشخص است. این ماده عمدتاً به عنوان ماده اولیه در سنتز تعداد زیادی از محصولات و همچنین به عنوان جزئی از بنزین استفاده می شود. بنزن به عنوان نقطه شروع برای سایر مواد شیمیایی مورد استفاده در ساخت پلاستیک، رزین و الیاف مصنوعی و برای ساخت انواع خاصی از روان کننده ها، رنگ ها، مواد شوینده و آفت کش ها نیز استفاده می شود.
قیمت فروش بنزن صادراتی
کشورهای توسعه یافته که توانایی تولید بنزن بالایی دارند اغلب صادر کننده بنزن و مشتقات آن هستند و بخش وسیعی از بنزن صادراتی خود را در حال حاضر از نفت خام بوسیله فرآیندهایی به نام « کراکینگ » یا «اصلاح» تولید می کنند. بنزن صادراتی اغلب در کاربردهایی مانند وسایل نقلیه موتوری، سوزاندن زغال سنگ و نفت، نقاشی و لیتوگرافی، خشک شویی و در ساخت مواد شیمیایی و در صنایعی مانند تولید کک و زغال سنگ پتروشیمی و نفت استفاده می شود.
حلقه بنزن
حلقه بنزن یا شکل ساختاری بنزن از زمان کشف آن مورد توجه بوده است. حلقه بنزن یک واحد ساختاری در مولکول های آلی معطر است که با حلقهای متشکل از شش اتم کربن با پیوندهای دوگانه متناوب بین اتم های کربن نشان داده می شود. در مولکول بنزن شش اتم هیدروژن به حلقه متصل شده اند و یک اتم به هر اتم کربن وصل شده است. اما در مشتقات بنزن یک یا چند اتم هیدروژن با اتم های عناصر دیگر یا گروه هایی از اتم ها جایگزین می شود.
کاربرد بنزن
بنزن یکی از ۲۰ ماده شیمیایی پرمصرف در کشورهای اروپایی است. هنوز هم در بسیاری از فرآیندهای صنعتی برای تولید پلاستیک، روان کننده، لاستیک، الیاف مصنوعی و رنگ استفاده می شود. با این حال، استفاده های غیر صنعتی آن محدود است زیرا بنزن سرطان زا و سمی است. بیشتر بنزن تولید شده برای تولید سایر مواد شیمیایی استفاده می شود. با این حال، حدود ۸۰٪ از بنزن عمدتا برای ساخت سه ماده شیمیایی اتیل بنزن، کومن و سیکلوهگزان استفاده می شود.
خرید مشتقات بنزن
زمانی که بنزن با سایر ترکیبات در طی واکنش های شیمیایی ترکیب شود، گروه های جدید جایگزین اتم های هیدروژن در برخی از اتم های کربن در حلقه می شوند و به این ترتیب مشتقات بنزن تشکیل می شوند. مشتقات بنزن مولکول های همه کاره هستند که امروزه در کاربردهای مختلفی مورد استفاده قرار می گیرند. مشتقات پرکاربرد بنزن شامل اتیل بنزن، فنل، آنیلین است که البته هرساله بیشترین مقدار بنزن تولیدی برای ساخت اتیل بنزن به کار برده می شود.
خرید بنزن
برای خرید بنزن می توانید به سایت های فروش مواد شیمیایی مراجعه کنید. این ترکیب شیمیایی کاربردهای بسیار گسترده ای دارد.
قیمت بنزن
قیمت بنزن به عوامل مختلفی بستگی دارد. برای آگاهی از قیمت این ماده شیمیایی بهتر است به دفاتر و سایت های فروش مواد شیمیایی مراجعه کنید.
بنزن چگونه تولید می شود + قیمت فروش
بنزن یک هیدروکربن معطر است که از کراکینگ بنزین در بسیاری از پالایشگاه ها به عنوان محصول نهایی استخراج و تولید می شود. بنزن یک ترکیب آلی و شیمیایی با بوی معطر است اما به عنوان یک ماده سرطان زا در نظر گرفته شده است. زیرا علاوه براینکه حاوی بنزین است خود بنزن و محصولات کاتابولسیم آن می توانند باعث سرطان شوند. بنزن به عنوان ماده اولیه برای استایرن، فنل، سیکلوهگزان و مواد شیمیایی مختلف دیگر و همچنین به عنوان حلال استفاده می شود.
نامگذاری مشتقات بنزن
برای نامگذاری ترکیبات بنزن، نام جایگزین را به کلمه بنزن اضافه می کنیم. برای ترکیبات بنزن متشکل از یک جایگزین، ما به سادگی نام جایگزین را به بنزن اضافه می کنیم (متیل بنزن یا تولوئن). هنگامی که دو جایگزین در ترکیب وجود دارد، هر یک از اتم های کربن را به گونه ای شماره گذاری می کنیم که جانشینها به کمترین شماره ممکن اتم کربن متصل شوند (۳-۱ دی کلروبنزن) و در مورد ترکیبات چند جانشین، اگر ترکیب پایه وجود داشته باشد. آن را به عنوان موقعیت ۱ نسبت می دهیم. سپس ترکیب بعدی را برای شماره گذاری انتخاب می کنیم تا کمترین عدد را به دست آورد.
تلفظ بنزن
بنزن یک ماده شیمیایی است که در دمای اتاق مایعی بی رنگ یا زرد روشن است و خیلی سریع در هوا تبخیر می شود. بخار آن از هوا سنگین تر است و ممکن است در مناطق کم ارتفاع به سمت پایین نشست کند. بنزن ساده ترین هیدروکربن معطر است و به عنوان اولین هیدروکربن های معطر با ماهیت پیوند آن برای اولین بار در قرن ۱۹ ایجاد شد.
فروش بنزن
بنزن کاربردهای متنوعی در صنعت دارد، که از آن اغلب به عنوان حلال، یک واسطه شیمیایی و یک ماده تشکیل دهنده در سوخت موتور استفاده می شود. ایالات متحده ۵۱۵۵ متریک تن بنزن در سال ۲۰۱۷ تولید کرد. پالایشگاه ها بنزن را به عنوان محصول جانبی تولید بنزین تولید می کنند و حدود ۶۰ درصد از تولید بنزن ایالات متحده را تشکیل می دهند. بنابراین این کشور بیشترین مقدار فروش بنزن (صادرات بنزن) را در کل دنیا دارا می باشد. فروش این ماده بازار گسترده ای در سراسر جهان دارد.
بنزن چیست
بنزن یک ترکیب شیمیایی آلی است که گاهی به نام بنزول نیز شناخته می شود. این ترکیب شیمیایی بوی شیرینی دارد و مایعی بی رنگ و قابل اشتعال است. بنزن یک حلال اصلی صنعتی است و در فرآیند تولید پلاستیک، روغن، لاستیک مصنوعی و بسیاری از رنگ ها استفاده می شود. دانشمند مایکل فارادی در سال ۱۸۲۵ بنزن را کشف کرد. او آن را از نفت جدا کرد و آن را بی کربنات هیدروژن نامید. این ماده به طور طبیعی در آتش سوزی های جنگلی و آتشفشان ها نیز تولید می شود و یک ماده سرطان زا و جزء اصلی در دود سیگار است
بنزن به عنوان یک ماده شیمیایی سرطان زا شناخته می شود، زیرا قرار گرفتن در معرض مقادیر زیاد (یا مقادیر کم به طور مداوم در یک دوره زمانی طولانی) می تواند باعث عملکرد نادرست سلول های بدن شود و با ایجاد بی نظمی در گلبول های قرمز خون و استخوان مرتبط است. علاوه بر این، قرار گرفتن در معرض زیاد این ماده در هوا با سرطان خون مرتبط است.
تا قبل از جنگ جهانی دوم، این ماده شیمیایی به عنوان محصول جانبی تولید زغال سنگ، عمدتا در صنعت فولاد تولید می شد. بنزن را می توان در هوای آزاد به دلیل دود تنباکو، اگزوز وسایل نقلیه موتوری و گازهای گلخانه ای صنعتی و همچنین در هوای داخل خانه در نتیجه استفاده چسب ها، رنگ ها و سایر محصولات حاوی مواد شیمیایی یافت.
در دهه ۱۹۵۰، تقاضای فزاینده ای برای بنزن، به ویژه در صنعت پلاستیک ایجاد شد. به دلیل این نیاز، تولیدکنندگان شروع به تولید آن از نفت کردند. بخش اعظم عرضه امروزی این ترکیب شیمیایی از صنعت پتروشیمی تامین می شود که تنها مقدار کمی از زغال سنگ به دست می آید.
بنزن سیر شده است؟
بنزن سیر شده یک ماده شیمیایی با کاربردهای فراوان است. قبل از دهه ۱۹۲۰، به طور منظم به عنوان یک حلال صنعتی استفاده می شده است. زمانی این ترکیب شیمیایی به طور گسترده ای به عنوان یک افزودنی به بنزین استفاده می شد، اما این کاربرد به دلیل نگرانی های بهداشتی و سلامتی کنار گذاشته شد.
معمولا بنزن سیر شده به عنوان افزودنی برای سایر مواد شیمیایی استفاده می شود. در صنایع از آن برای ساخت استایرن که در ساخت پلاستیک و پلیمر استفاده می شود. مقادیر کمی از این ترکیب شیمیایی در فرآیندهای تولید داروها، شوینده ها، آفت کش ها و مواد منفجره استفاده می شود.
مضرات بنزن
از آنجایی که بنزن با تماس با هوا به سرعت تبخیر می شود، اکثر مردم با تنفس آن در معرض بنزن قرار می گیرند. بنزن همچنین می تواند در طول تماس با منبع مایع حاوی بنزن از طریق پوست نیز جذب شود، اما این امر کمتر رایج است. بالاترین سطح قرار گرفتن در معرض از لحاظ تاریخی در محل کار در صنایعی بوده است که با بنزن کار می کنند. با این حال، بسیاری از صنایع در حال کاهش استفاده از بنزن خود هستند، بنابراین این میزان در سال های اخیر کاهش یافته است.
افراد عادی با تنفس دود تنباکو، به ویژه از طریق سیگار، بیشتر در معرض بنزن قرار می گیرند. در واقع، در میان افراد سیگاری، ۹۰ درصد از قرار گرفتن در معرض بنزن ناشی از استنشاق دود سیگار است. بنزن همچنین در بنزین نیز یافت می شود و اگر فردی بخار بنزین را استنشاق کند می توان آن را استنشاق کرد. همچنین می توان این ترکیب شیمیایی خطرناک را در چسب ها، پاک کننده های رنگ و محصولات تمیز کننده نیز یافت کرد.
قرار گرفتن در معرض کوتاه مدت بنزن می تواند باعث خواب آلودگی، سردرد و سرگیجه شود. مصرف مقادیر زیاد این ترکیب شیمیایی می تواند باعث استفراغ، تشنج و از دست دادن هوشیاری شود. همچنین با تغییر سطح آنتی بادی ها در خون، سیستم ایمنی را تضعیف می کند. قرار گرفتن در معرض این ماده شیمیایی می تواند باعث کم خونی آپلاستیک، خونریزی بیش از حد، و افزایش خطر ابتلا به سرطان خون شود.
قیمت پودر بنزن
بنزن یک مایع شفاف، بی رنگ و بسیار قابل اشتعال با بوی شیرین و شبیه بنزین است. بنزن کمی در آب حل می شود، در حالی که باقیمانده آن شناور باقی خواهد ماند. برای تهیه پودر بنزن، تولید کنندگان آن را با مواد شیمیایی دیگر ترکیب می کنند. آلکیل بنزن سولفونات سدیم به عنوان پودر بنزن در بازار شناخته می شود. پودر بنزن در مقایسه با بنزن مایع راحتتر حمل و نقل و ذخیره می شود.
خرید بنزن
یکی از مهمترین دغدغه های فعالان حوزه شیمیایی، خرید بنزن از یک فروشنده معتبر، باسابقه و قابل اطمینان است. با هدف افزایش اعتماد بین فروشندگان و خریداران از کیفیت محصول موردنظر در فرایند خرید بنزن، ما به عنوان مرجع مواد شیمیایی در ایران، تمام تلاش خود را کرده ایم که بهترین فروشندگان بنزن را در این بخش و همچنین بنر بالای صفحه به شما معرفی نماییم. امیدواریم با معرفی تامین کنندگان منتخب، نگرانی های خریداران محترم کاهش یافته و بتوانیم لذت تجربه خرید بنزن با قیمت و کیفیت مناسب را به شما هدیه نماییم.
- محل تبلیغ شما




















تفاوت قیمت بنزن بین ایران و عراق چقدره؟ قطعا توی این هفته های اخیر برای خریداران در کشورهای همسایه خرید محصولات از ما خیلی جذاب تر شده ، افزایش قیمت ارز برای مردم ایران سودی نداشت. امیدوارم حداقل برای صادرکنندگان سود داشته باشه.
عصر بخیر
کاربرد بنزن به عنوان ماده اولیه، در تولید چه مواد شیمیایی استفاده می شود؟ در مورد کاربردهای دیگر بنزن خصوصا در جوهر چاپ واقعا انتظار این همه کاربرد را نداشتم!!!
سوال اول من، مشتقات بنزن چگونه بدست می آید؟
سوال دوم من هم اینکه برای معرفی انواع مشتقات بنزن، مثل مشتقات ساده و جایگزین شده، بهتر نیست که از روش مصور بیشتری مثل اینفوگرافی استفاده کنید. یک تصویر گرافیکی هم برای دانلود قرار بدید.