
در تمامی واكنش های برگشت پذير، لحظه اي وجود دارد كه در آن سرعت واکنش رفت با سرعت واکنش برگشت با هم برابر می شوند. به این زمان، زمان تعادل گفته می شود. در واقع در این حالت، واكنش متوقف نشده است، اما تغييری در غلظت ها در سطح ماكروسكوپی بوجود نمی آید. بنابراین از تقسیم ثابت سرعت واکنش رفت (kf) بر ثابت سرعت واکنش برگشت (kr)، ثابت تعادل (Equilibrium Constant) بدست می آید که با نماد K، نشان داده می شود. در ادامه این مقاله در نشریه جهان شیمی فیزیک به بررسی ثابت تعادل و عوامل موثر بر آن پرداخته می شود. لطفا با ما همراه باشید.
فهرست مطالب
تعادل شیمیایی
تعادل شیمیایی (Chemical equilibrium) به حالتی می گویند که در آن فعالیت شیمیایی و یا غلظت واکنش دهنده ها و فرآورده ها با گذشت زمان در واکنش شیمیایی تغییر نکند. این تعادل به طور معمول در شرایطی بوجود می آید که سرعت واکنش رفت با سرعت واکنش برگشت برابر باشد. به عنوان نمونه واکنش تعادلی ساده زیر را در نظر بگیرید.
A ⇌ B
نماد فلش دو طرفه (⇌) به خوبی بیانگر اینست که واکنش می تواند در جهت تولید واکنش دهنده یا فرآورده، انجام شوند. در واقع اگر در يك واكنش امكان آنکه فرآورده به طريقی دوباره به واكنش دهنده تبديل شود واكنش برگشت پذير می باشد. روابط سرعت و غلظت در واكنش برگشت پذير مورد نظر به صورت زیر است.
سرعت واکنش رفت Rf = kf [A]
سرعت واکنش برگشت Rr = kr [B]
در زمان تعادل Rf = Rr = kf [A] = kr [B]
بنابراین داریم :
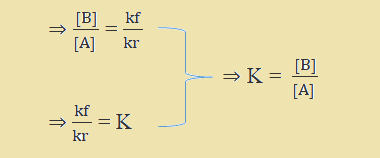
در معادله فوق، K ثابت تعادل است که برای يك واكنش معين در دمای ثابت مقداری همواره ثابت می باشد.
مثال
به عنوان نمونه تشکیل دی اکسید نیتروژن از دی نیتروژن تترا اکسید یک واکنش برگشت پذیر می باشد.
N۲O۴ (g) ⇋ 2NO۲ (g)
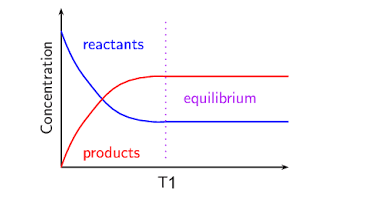
با توجه به نمودار مشخص می شود که در ابتدا تنها گاز N۲O۴ داریم. با تبدیل N۲O۴ به NO۲، غلظت گاز NO۲ (خط قرمز رنگ) تا یک مقدار مشخصی افزایش پیدا می کند (نقاط خط چین) و سپس مقدار آن در طول زمان بدون تغییر می ماند. از طرف دیگر، غلظت گاز N۲O۴ با گذشت زمان کاهش پیدا می کند (خط آبی رنگ) تا به غلظت تعادلی با گاز NO۲ برسد. هنگامیکه غلظت هر دو گاز در یک مقدار مشخص ثابت شد، در نتیجه واکنش به تعادل رسیده است.
شرايط لازم يك سیستم در حال تعادل
۱- سیستم بايد كاملا بسته و ايزوله باشد. در واقع بين سیستم و محيط هیج گونه تبادل جرم و یا انرژی انجام نشود.
۲- خواص ماكروسكوپی سیستم از جمله جرم، حجم، رنگ، جرم حجمی و غیره ثابت و بدون تغییر باشد.
۳- واکنش بین واکنش دهنده ها و فرآورده ها در سطح ميكروسكوپی ادامه داشته باشد. توجه داشته باشید که به این حالت، تعادل دینامیکی یا پویا گفته می شود.
۴- سرعت واکنش رفت با سرعت واکنش برگشت برابر و مساوی باشد.

تعریف ثابت تعادل
همانطور که بیان شد، به معادله ای که در یک تعادل، بین غلظت واکنش دهنده ها و فرآورده ها برقرار است، ثابت تعادل گفته می شود. در واقع این ثابت برابر با حاصل ضرب غلظت فرآورده ها به توان ضرایبشان بخش بر حاصل ضرب غلظت واکنش دهنده ها به توان ضرایبشان در لحظه تعادل است.
به عبارت دیگر می توان این طور بیان نمود كه برای آنکه بتوان رابطه بین غلظت واکنش دهنده ها و فرآورده ها را در یک تعادل بیان کرد از K استفاده می شود که در حقیقت بیانگر نسبت حاصل ضرب غلظت فرآورده ها به حاصل ضرب غلظت واکنش دهنده ها می باشد.
به کمک K می توان حالت تعادلی یا غیر تعادلی یک واکنش مورد نظر را تعیین نمود. همچنین این ثابت کمک می کند تا بدانید که در یک واکنش در حال تعادل، غلظت کدامیک از واکنش دهنده ها یا فرآورده ها بیشتر می باشد. در حقیقت مقدار عددی K برای هر تعادل، وضعیت آن تعادل را نشان می دهد. اگر ثابت تعادل بسیار تا بسیار کوچک باشد، انجام واکنش عملا غیر ممکن می باشد.
لازم به ذکر است که اگر عدد K کوچک باشد (حدود ۰.۰۰۱ یا کمتر)، واکنش از سمت راست به چپ کامل می باشد. در واقع مقدار بسیار کمی از واکنش دهنده ها به فرآورده تبدیل شده اند. در حالیکه اگر عدد آن بزرگ باشد (بیش از ۱۰۰۰)، واکنش به سمت راست کامل می باشد. در واقع نشان دهنده بیشتر بودن غلظت فرآورده ها است. یعنی مقدار بیشتری از واکنش دهنده ها به فرآورده تبدیل شده اند. در این حالت بازده واكنش بيشتر و واکنش کمی تر می باشد.اما اگر مقدار عددی K نه بسیار بزرگ و نه بسیار کوچک باشد، در این حالت وضع تعادل بینابینی می باشد.
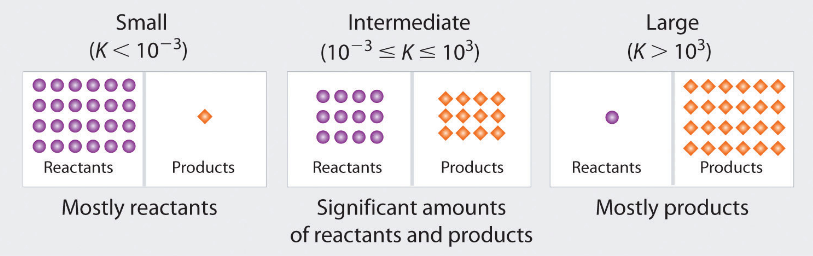
محاسبه ثابت تعادل
واکنش تعادلی زیر را در نظر بگیرید:
aA + bB ⇌ cC + dD
که در آن، حروف بزرگ بیانگر مواد واکنش دهنده و محصولات و حروف کوچک بیانگر ضرایب استوکیومتری آنها می باشند. در صورتیکه غلظت مولی یا مولاریته واکنش دهنده ها و فرآورده ها را داشته باشید، رابطه ثابت تعادل در حالت کلی به صورت زیر بدست می آید.
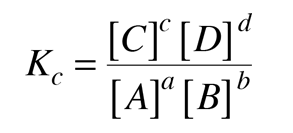
در رابطه بالا، [A] و [B] غلظت های تعادلی واکنش دهنده ها بر حسب مولاریته (مول بر لیتر)، [C] و [D] غلظت های تعادلی محصولات بر حسب مولاریته و ضرایب c ،b ،a و d ضرایب استوکیومتری معادله موازنه شده می باشند. محدوده تغییرات ثابت تعادل بین صفر تا بی نهایت می باشد. بنابراین مقدار عددی K می تواند عددی بسیار کوچک مثل ۳۲- 10 × ۱.۸ و یا عدد بسیار بزرگی مانند ۱۰۷۴ × ۳.۳ باشد.
لازم به ذکر است که در محاسبات دقیق ثابت تعادل، به جای استفاده از غلظت مولی مواد از فعالیت شیمیایی آنها استفاده می شود. توجه داشته باشید که فعالیت شیمیایی با غلظت و یا فشار جزئی متفاوت است. بنابراین این تفاوت را در محاسبات باید در نظر گرفت. با این حال در غلظت های پایین و یا در فشار هایی تا چند اتمسفر می توان ثابت های تعادل بر حسب غلظت و یا فشار را با دقت قابل قبولی استفاده نمود.
توجه داشته باشید که فعالیت دارای واحد نمی باشد، بنابراین ثابت های تعادل معمولا بدون واحد بیان می شوند. زیرا در واقع فعالیت از تقسیم کردن غلظت یا فشار واقعی یک ماده بر غلظت یا فشار همان ماده در حالت استاندارد بدست آمده است. لازم به ذکر است که که ثابت های تعادل تنها به دما وابسته می باشند. در نتیجه مستقل از غلظت های مواد شرکت کننده در واکنش به ویژه غلظت ها در شروع واکنش یا در حقیقت غلظت های اولیه می باشد.
ثابت تعادل Kc
در تعادلی که در آن غلظت های مواد اولیه و محصولات، بر حسب مول بر لیتر (مولاریته) بیان شوند، ثابت تعادل را می توان به جای K به صورت Kc نشان داد.
لازم به ذکر است که در معادله K فقط غلظت مواد گازی و محلول نوشته می شود، زیرا غلظت مواد جامد (s) و مایع خالص (l) عددی ثابت می باشد. پس در رابطه ثابت تعادل از نوشتن غلظت آنها صرف نظر می کنند و در نتیجه غلظت آنها را برابر با یک در نظر می گیرند. توجه داشته باشید که با اینکه غلظت مواد جامد و یا مایع در رابطه تعادل نوشته نمی شوند، اما وجود آنها برای برقراری تعادل واجب و ضروری است. به عنوان نمونه به معادله K در تعادل زیر توجه کنید :
2Mn (s) + O۲ (g) ⇋ ۲ MnO (s)
ثابت تعادل Kp
در صورتیکه هر یک از مواد واکنش دهنده یا فرآورده به شکل گاز باشند، ثابت تعادل را می توان بر حسب فشار جزئی گازها نوشت. در واقع فشار جزئی یک گاز اندازه ای از غلظت آن می باشد. این نوع از ثابت تعادل را با Kp نشان می دهند. در این صورت از محاسبات ثابت تعادل بر حسب مولاریته جدا می شود. به عنوان مثال واکنش زیر را در نظر بگیرید.
aA (g) + bB (g) ⇌ cC (g) + dD (g)
Kp عبارت است از :
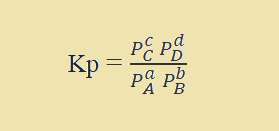
در رابطه بالا، p فشار جزئی هر یک از مواد واکنش دهنده یا فرآورده بر حسب اتمسفر (atm) یا بار (bar) می باشد. حال به عنوان نمونه واکنش تولید آمونیاک را در نظر بگیرید.
N۲ (g) + 3H۲ (g) ⇌ 2NH۳ (g)
Kp = [PNH3]۲ / [PN2] [PH2]۳
تبدیل Kc به ثابت Kp
برای تبدیل K به Kp از رابطه زیر استفاده می کنند.
Kp =Kc (RT)Δn
که در آن، R=0.0820575 Latmmol−۱K−۱ و یا R=8.31447 Jmol−۱K−۱ می باشد. علاوه بر آن T دما و Δn تعداد مول های گازی می باشند.
یکای ثابت تعادل
برای تعیین یکای ثابت تعادل، به جای غلظت هر ماده می توان یکای آنها یعنی mol.L-۱ را قرار داد. در نتیجه با ساده کردن یکا ها، در نهایت یکای K تعیین می شود. در بعضی از تعادلات، ممکن است که کلیه یکا های به کار رفته حذف شوند. در این صورت K یکا ندارد و فقط یک مقدار عددی خواهد بود. در واقع K، یک کمیت بدون بعد می باشد.
نکات اساسی مربوط به ثابت تعادل
۱- اگر یک تعادل به صورت معکوس نوشته شود، مقدار عددی K نیز معکوس می شود.
۲- اگر یک تعادل در عددی ضرب شود، مقدار عددی ثابت تعادل به توان آن عدد می رسد.
۳- اگر یک واکنش تعادلی را بتوان به صورت حاصل جمع دو واکنش تعادلی دیگر نوشت، مقدار عددی ثابت تعادل آن واکنش مورد نظر برابر با حاصلضرب مقادیر عددی ثابت تعادل دو واکنش اولیه می باشد.
۴- اگر در یک تعادل معین دما ثابت باشد، K نیز ثابت می ماند. اما با تغییر دما، مقدار عددی K نیز تغییر میکند.
۵- واکنش باید به صورت موازنه شده باشد. در نتیجه با کمترین اعداد صحیح ممکن بازنویسی می شود تا مقادیر درستی از K بدست آید.
۶- جامدات خالص، مایعات خالص و حلال ها در رابطه ثابت تعادل نوشته نمی شوند. اما در مورد محلول های مایع : همانطور که می دانید به طور معمول، غلظت مواد حل شونده نسبت به غلظت حلال بسیار کمتر می باشد. از طرفی تغییرات غلظت حلال در هنگام انجام واکنش داخل محلول اغلب قابل صرف نظر کردن می باشد. بنابراین، معمولا می توان حلال را تقریبا یک مایع خالص فرض کرد. در نتیجه می توان از غلظت حلال در روابط ثابت های تعادل مربوطه چشم پوشی نمود.
۷- همواره غلظت مواد فرآورده (مواد سمت راست در معادله شیمیایی) در صورت کسر و غلظت مواد اولیه (مواد سمت چپ معادله) در مخرج عبارت K نوشته می شوند.
خارج قسمت تعادل
در حالتی که غلظت ها در رابطه ثابت تعادل صدق کنند، یعنی با جایگذاری آنها در رابطه، عدد K بدست آید، غلظت های مورد نظر غلظت های تعادلی می باشند. در نتیجه واکنش با همان غلظت های مورد نظر در حالت تعادل قرار دارد. در حالیکه غلظت های مورد نظر در رابطه ثابت تعادل صدق نکنند، در نتیجه واکنش به تعادل نرسیده است و بنابراین واکنش در تعادل قرار ندارد. در چنین حالتی اگر غلظت واكنش دهنده ها و فرآورده ها را در رابطه ثابت تعادل قرا دهند، عددی که بدست می آید را خارج قسمت (Reaction Quotient) یا Q می نامند.
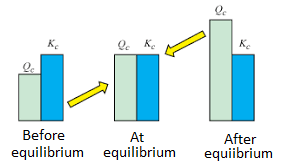
با مقایسه مقادیر بدست آمده از رابطه خارج قسمت واکنش و ثابت تعادل آن واکنش، می توان جهت پیشرفت واکنش را مشخص نمود. در این صورت ۴ حالت مختلف پیش می آید که عبارتند از :
۱- Q = K. در این حالت، سیستم در حال تعادل می باشد.
۲- Q < K. در این حالت، غلضت واکنش دهنده ها بیشتر از فرآورده ها می باشد. بنابراین واکنش به سمت فرآورده ها حرکت کرده و تا رسیدن به تعادل ادامه پیدا می کند.
۳- Q > K. در این حالت، غلضت فرآورده ها بیشتر از واکنش دهنده ها می باشد. بنابراین واکنش به سمت چپ پیش می رود.
۴- Q = 0. در این حالت، خارج قسمت واکنش از ثابت تعادل آن کمتر می باشد. بنابراین واکنش به سمت تولید فرآورده (سمت راست) در حال پیشرفت خواهد بود.
ثابت تعادل شیمی دوازدهم
در رشته شیمی یکی از مهمترین مفاهیمی که دانش آموزان باید یاد بگیرند فرمول ثابت تعادل است. این فرمول یک نمایش ریاضی از تعادلی است که در واکنش های شیمیایی وجود دارد. برای توصیف حالت تعادل یک واکنش شیمیایی استفاده می شود، به این معنی که سرعت واکنش رو به جلو برابر با سرعت واکنش معکوس است. فرمول ثابت تعادل برای پیش بینی جهت یک واکنش و همچنین مقدار واکنش دهندهها و محصولاتی که در حالت تعادل وجود خواهند داشت، ضروری است. درک این فرمول برای دانش آموزانی که به دنبال شغلی در شیمی هستند بسیار مهم است، زیرا اساس بسیاری از موضوعات پیشرفته در این زمینه را تشکیل می دهد.
فرمول ثابت تعادل عبارتی است که غلظت واکنش دهنده ها و محصولات در یک واکنش شیمیایی را به ثابت تعادل مرتبط می کند. ثابت تعادل مقداری است که مقدار واکنش دهنده ها و محصولات موجود در حالت تعادل را توصیف می کند. برای محاسبه ثابت تعادل، ابتدا باید غلظت واکنش دهنده ها و محصولات در حالت تعادل را تعیین کنید. این را می توان با انجام آزمایش و اندازه گیری غلظت واکنش دهنده ها و محصولات در زمان های مختلف انجام داد.
ثابت تعادل معیاری است از میزان پیشرفت یک واکنش تا تکمیل. مقدار زیاد Keq نشان میدهد که محصولات بیشتری نسبت به واکنشدهندهها در حالت تعادل وجود دارد، در حالی که مقدار کمی از Keq نشان میدهد که واکنشدهندهها بیشتر از محصولات است. اگر Keq برابر با ۱ باشد، واکنش دهنده ها و محصولات به مقدار مساوی در حالت تعادل وجود دارند. ثابت تعادل همچنین می تواند برای پیش بینی جهت یک واکنش استفاده شود. اگر Keq بزرگتر از ۱ باشد، واکنش در جهت جلو پیش می رود، در حالی که اگر Keq کمتر از ۱ باشد، واکنش در جهت معکوس انجام می شود.



















