
واکنش اکسایش و کاهش یا ردوکس (Redox) به واکنش های شیمیایی گفته می شود که در طی انجام آنها عدد اکسایش حداقل یک عنصر تغییر کند. به بیان دیگر می توان گفت که واکنشی است که در آن یک یا چند اتم الکترون از دست می دهند، در حالیکه یک یا چند اتم دیگر الکترون می گیرند. توجه داشته باشید که بسیاری از واکنش های اکسایش و کاهش در محلول های آبی یا سوسپانسیون انجام می شوند. در مطالب پیشین نشریه جهان شیمی فیزیک، با مفهوم عدد اکسایش و نحوه تعیین آن آشنا شده اید. در این مقاله به بررسی واکنش های اکسایش و کاهش و نحوه انجام آنها پرداخته می شود. لطفا همراهی بفرمایید.
فهرست مطالب
الکترو شیمی
الکترو شیمی علمی است که در واقع پل ارتباطی الکتریسیته به شیمی می باشد. در حقیقت آنچه که دو علم شیمی و الکتریسیته را به هم مرتبط کرده است، الکترون می باشد. علاوه بر آن، مسئولیت انتقال بار الکتریکی در مواد رسانا و مدارهای الکتریکی نیز بر عهده الکترون ها است. به بیان دیگر، الکترو شیمی علمی است که در آن می توان همزمان با استفاده از انرژی الکتریکی سبب انجام واکنش شیمیایی شد، و یا اینکه با انجام یک واکنش شیمیایی، جریان الکتریکی را نیز تولید نمود.
به این دسته از واکنش های شیمیایی که در آنها نقل و انتقال الکترون صورت می گیرد، واکنش های اکسایش – کاهش و یا اکسیداسیون – احیا گفته می شود. توجه داشته باشید که واکنش های اکسایش و کاهش باید همیشه به طور همزمان انجام شوند. در واقع در این واکنش ها، اتم یا مولکولی که الکترون از دست می دهد اکسایش یافته، در حالیکه اتم یا مولکولی دیگر که الکترون جذب کرده است کاهش می یابد. به بیان دیگر می توان گفت که در چنین واکنش هایی اتم یا مولکول دهنده الکترون اکسید و اتم یا مولکول گیرنده الکترون کاهیده می شود.
واکنش های اکسیداسیون – احیا می توانند شامل واکنش ساده ای مانند اکسایش کربن به دی اکسید کربن یا کاهش آن (کربن) به متان باشد. یا ممکن است شامل واکنش پیچیده ای مانند اکسایش قند در بدن انسان شود. به عنوان مثال می توان به واکنش سوختن منیزیم اشاره کرد. این واکنش شعله و نور شدیدی تولید می کند (به همين دليل از آن در آتش بازی استفاده می شود) که در شکل زیر مشاهده می کنید.
2Mg (s) + O۲ (g) → 2MgO (s)

اهمیت واکنش های اکسایش و کاهش
بسیاری از زنگ زدن ها و خوردگی های مربوط به فلزات را میتوان به عنوان واکنش های اکسایش – کاهش در نظر گرفت. از زمان های گذشته تاکنون، آهن بیشترین کاربرد را در میان فلزات در زندگی انسان داشته است. از این رو مخارج محافظت از خوردگی و همچنین زیان های ناشی از زنگ زدن آهن بسیار زیاد می باشد. از جمله عواملی که در زنگ زدن آهن دخالت دارند، عبارتند از : رطوبت، اکسیژن هوا، ناخالصی ها، برخی از گازهای خورنده موجود در محیط و PH.

تعریف واکنش اکسایش و کاهش
تاکنون تعریف های متفاوتی برای اکسایش و کاهش مطرح شده است که در ادامه به بررسی آنها پرداخته می شود.
۱- بر اساس مبادله اکسیژن
مطابق اين تعريف که قدیمی ترین و ابتدایی ترین تعریف محسوب می شود، اگر ماده ای در يك واكنش شیمیایی اكسيژن بگيرد اکسایش یافته، بنابراین اكسيد شده است. در حالیکه اگر ماده ای اكسيژن از دست بدهد کاهش یافته، پس كاهيده یا احیا شده است. به عنوان نمونه، مولکول V۲O۵ در واکنش زیر، اكسيژن از دست داده، پس احیا شده است، در حالیکه كربن مونوكسيد با گرفتن اكسيژن اکسایش یافته، پس اكسيد شده است.
V۲O۵ +2CO → V۲O۳ + 2CO۲
۲- بر اساس مبادله هیدروژن
مطابق اين تعريف اگر عنصری هیدروژن از دست بدهد اکسایش یافته (اکسید شده)، در حالیکه اگر هیدروژن بگیرد کاهش یافته ( کاهیده یا احیا شده) است. به عنوان نمونه، سدیم در واکنش زیر، هیدروژن گرفته، پس احیا شده است، در حالیکه مولکول آب با از دست دادن هیدروژن اکسایش یافته، پس اكسيد شده است.
Na + H۲O → NaOH + H۲
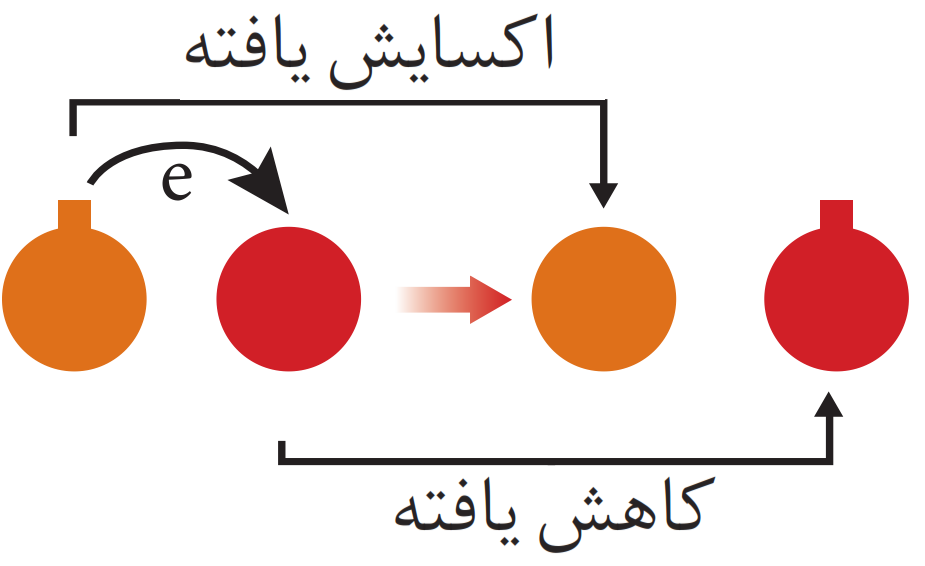
۳- بر اساس مبادله الکترون
مطابق اين تعريف اگر عنصری الکترون از دست بدهد اکسایش یافته (اکسید شده) است، در حالیکه اگر الکترون بگیرد کاهش یافته (کاهیده یا احیا) شده است. به عنوان نمونه، مس در واکنش زیر، الکترون گرفته، پس احیا شده است، در حالیکه روی با از دست دادن الکترون اکسایش یافته، پس اكسيد شده است.
Zn (s) + Cu۲+ (aq) ⟶ Zn۲+ (aq) + Cu (s)
۴- بر اساس عدد اکسایش
مطابق اين تعريف اگر عدد اکسایش عنصری افزایش یابد، اکسایش یافته است (اکسید شده)، در حالیکه اگر عدد اکسایش عنصری کاهش یابد، آن عنصر کاهش یافته (کاهیده یا احیا شده) است. این تعریف که تعریف امروزی بوده و از دیگر تعاریف جامعتر و کاملتر است به عنوان نمونه، در واکنش زیر عدد اکسایش گوگرد از صفر به ۴+ افزایش یافته است، بنابراین گوگرد اکسید شده است، در حالیکه عدد اکسایش اکسیژن از صفر به ۲- تغییر کرده است، پس احیا شده است.
S (s) + O۲ (g) → SO۲ (g)
علاوه بر آن، به تغییر اعداد اکسایش در واکنش زیر توجه کنید. عدد اکسایش آهن از ۳+ به صفر و عدد اکسایش کربن از ۲+ به ۴+ تغییر کرده است.
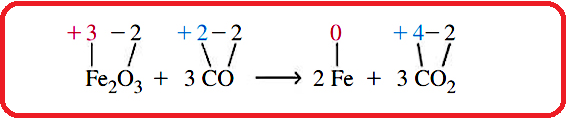
توجه داشته باشید که واکنش زیر یک واکنش اکسایش-کاهش نمی باشد، زیرا عدد اکسایش هیچ اتمی تغییر نکرده است.
NaOH + HCl → NaCl + H۲O
نیم واکنش های اکسایش و کاهش
لازم به ذکر است که از دست دادن يا گرفتن الكترون به تنهايي انجام نمی شود. به واكنش فرضي كه در آن يك عنصر تنها الكترون بگيرد و يا الكترون از دست بدهد يك نيم واكنش (Half-reaction) گفته می شود. در واقع نیم واکنش، واکنشی است که طی آن الکترون های آزاد به وسیله مواد گرفته یا آزاد می شوند. بنابراین طی یک نیم واکنش، در صورتی كه الكترون اضافی باقی نماند، فرآیند اکسایش یا کاهش انجام می گیرد. در حقیقت یک نیم واکنش بخشی از یک واکنش کلی اکسیداسیون – احیا می باشد.
تعریف فوق را به صورت دیگری نیز می توان بیان کرد. در واقع نیم واکنش به نیمی از یک واکنش اکسایش ـ احیا که در سمت چپ یا راست آن الکترون وجود دارد گفته می شود. توجه داشته باشید که مواد شرکت کننده در نیم واکنش ها، به صورت یون (با بار مثبت یا منفی) مشخص می شوند.
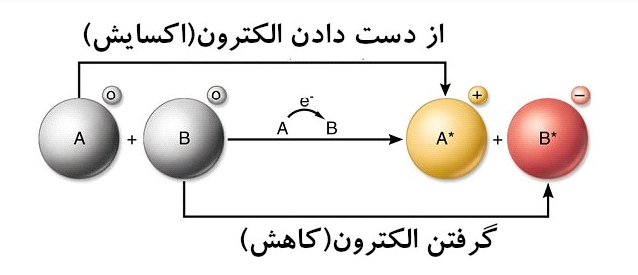
نیمه واکنش اکسیداسیون (اکسایش)
در ابتدا به واکنش یک ماده با اکسیژن و در نتیجه ترکیب شدن با آن را اکسایش می گفتند. اما با کشف الکترون مفهوم اکسایش دقیق تر تعریف شد. در واقع به کلیه واکنش هایی که طی آن ماده ای الکترون از دست می دهد و عدد اکسایش آن افزایش می یابد اکسایش گفته می شود. لازم به ذکر است که اتم اکسیژن ممکن است در چنین واکنشی شرکت داشته یا نداشته باشد. در نیمه واکنش های اکسایش، الکترون ها در سمت راست نیمه واکنش نوشته می شوند و این نیمه واکنش گرمازا می باشد. به عنوان مثال به نیمه واکنش زیر در سوختن مینزیم توجه کنید.
نیمه واکنش اکسایش : –2Mg (s) ⟶ 2Mg ۲+ (s) + 4e
در اینجا اتم منیزیم دو الکترون از دست می دهد، بنابراین خودش اکسایش یافته است و اکسیژن را می کاهد. علاوه بر آن، در طی این واکنش منیزیم دارای بار مثبت می گردد. عدد اکسایش آن از صفر به ۲+ تغییر کرده است.
نیمه واکنش احیا (کاهش)
به کلیه واکنش هایی که طی آن ماده ای الکترون می گیرد و عدد اکسایش آن کاهش می یابد احیا گفته می شود. در نیمه واکنش های کاهش، الکترون ها در سمت چپ نیمه واکنش نوشته می شوند و این نیمه واکنش گرماگیر می باشد. به عنوان مثال به نیمه واکنش زیر در سوختن مینزیم توجه کنید.
نیمه واکنش کاهش: O۲ (g) + 4e– → 2O۲- (s)
در طی این واکنش، اتم اکسیژن الکترون های اتم منیزیم را به سمت خود می کشد و دارای بار منفی می شود. عدد اکسایش اکسیژن از صفر به ۲- کاهش پیدا می کند. لازم به ذکر است که دو نیمه واکنش به طور همزمان انجام می شوند، بنابراین الکترون به طور همزمان از منیزیم به اکسیژن انتقال پیدا می کند. در واقع در واکنش کلی، اتم منیزیم الکترون از دست داده، پس خودش اکسایش پیدا کرده و اتم اکسیژن را می کاهد.
عامل اکسنده و عامل کاهنده
همانطور که بیان شد، واکنش های اکسایش و کاهش به تنهایی امکان پذیر نمی باشند. زیرا یک ماده نمی تواند احیا شود مگر آن که همزمان ماده ای دیگر، اکسید شود. بنابراین، ماده ای كه اكسيد می شود كاهنده می باشد و ماده اكسنده خود کاهش می یابد.
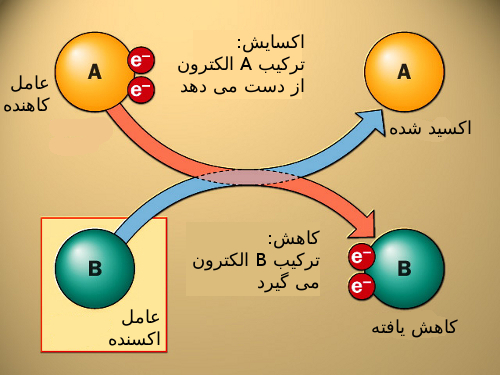
مواد اکسید کننده
در واقع اکسید کننده ها موادی می باشند که از سایر مواد الکترون می گیرند، پس آنها را اکسید کرده و خودشان احیا می شوند. به موادی که یکی از اجزای آنها به بالا ترین درجه اکسایش خود برسد (بالاترین درجه اکسایش برای یک عنصر برابر با شماره گروه آن عنصر می باشد) اکسید کننده قوی می گویند. به بیان دیگر، هر چه توانایی قبول الکترون بالاتر باشد، ماده شیمیایی مورد نظر اکسید کننده قویتری خواهد بود. مثلا، اسید نیتریک (HNO۳)، پتاسیم دی کرومات (K۲Cr۲O۷) و یا پتاسیم پرمنگنات (KMnO۴)، ید، کلرید آهن (III)، پروکسید هیدروژن، یدات پتاسیم، کلر، برم.
علاوه بر آن، بر اساس تعاریف اکسایش و احیا که در بخش قبلی بیان شد، می توان گفت که ماده اکسنده به ماده ای گفته می شود که یکی از این چهار خصوصیت زیر را داشته باشد. اکسیژن از دست بدهد، هیدروژن یا الکترون بگیرد و یا عدد اکسایش آن کوچک شود.
مواد احیا کننده
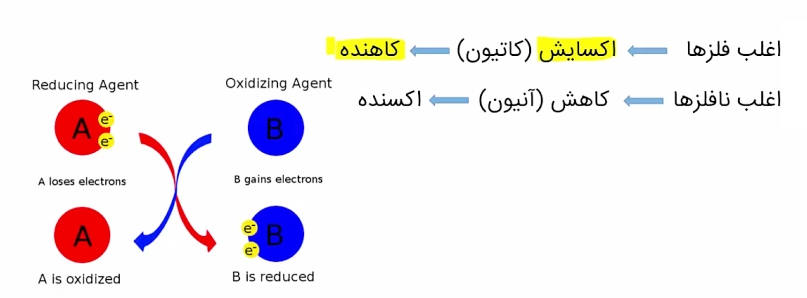
از طرفی دیگر، مواد کاهنده یا احیا کننده موادی می باشند که به سایر مواد الکترون می دهند، بنابراین آنها را کاهش داده و خودشان اکسید می شوند. به بیان دیگر، یک احیا کننده قویتر ترکیبی است که تمایلش به از دست دادن الکترون شدیدتر باشد. به عنوان نمونه تعدادی از کاهنده های قوی عبارتند از فلزات قوی همانند فلزات قلیایی و قلیایی خاکی، هیدروژن، دیاکسید گوگرد، سولفات آهن (II)، نمک های قلع (II) و آهن (II)، اسید اکسالیک، اسید یدیدریک، H۲S و غیره.
مشابه مواد اکسنده، بر اساس تعاریف اکسایش و احیا که در بخش قبلی بیان شد، می توان گفت که ماده کاهنده به ماده ای گفته می شود که یکی از این چهار خصوصیت زیر را داشته باشد. در واقع اکسیژن بگیرد، هیدروژن یا الکترون از دست بدهد و یا عدد اکسایش آن بزرگ شود.
انواع واکنش های اکسایش و کاهش
۱- در این نوع از واکنش ها، یک ماده کاملا اکسید و یک ماده دیگر کاملا احیا می شود. همانند واکنش زیر.
+Sn۴+ + Fe۲+ → Sn۲+ + Fe۳
۲- در این نوع از واکنش ها، یک تعدادی از اتم ها تغییر درجه اکسایش می دهند، اما تعدادی دیگر از همان اتم بدون تغییر باقی می مانند. به عنوان مثال اتم نیتروژن در اسید نیتریک یک بار از ۵+ به ۴+ در نیتروژن دی اکسید تغییر عدد اکسایش داده است و یک بار در Cu(NO۳)۲ بدون تغییر باقی مانده است.
Cu + HNO۳ → Cu(NO۳)۲ + NO۲ + H۲O
۳- در این نوع از واکنش ها، یک عنصر هم اکسید و هم کاهیده می شود. این دسته از واکنش ها به واکنش های تسهیم نامتناسب (Disproportionation) یا خود اکسایش-کاهش مشهور می باشند. به عنوان نمونه در واکنش زیر Br۲ همزمان اکسید و احیا شده است.
–Br۲ → BrO۳– + Br
توجه داشته باشید که واکنش تسهیم نامتناسب می تواند به صورت وارونه نیز باشد. یعنی در واقع یک عنصر در طرف اول با دو درجه اکسایش متفاوت به یک درجه اکسایش در طرف دوم برسند. مثلا درجه اکسایش ید در واکنش زیر، یک بار از یدات ۵+ پنج و یک بار از ید ۱- به ید مولکولی صفر رسیده است.
IO۳– + I– + H+ → H۲O + I۲
تشخیص واکنش های اکسیداسیون – احیا
برای تشخیص یک واکنش اکسایش ـ کاهش، باید اعداد اکسایش تمامی عناصر شرکت کننده در واکنش را در نظر گرفت تا بررسی شود که آیا تغییری در درجه اکسایش صورت گرفته یا خیر. توجه داشته باشید که اگر در سمت چپ یا سمت راست واکنش مورد نظر، عنصری به حالت آزاد وجود داشته باشد (مانند O۲ و یا Cu) آن واکنش حتما از نوع اکسایش ـ کاهش می باشد. لازم به ذکر است که عکس این مطلب صادق نیست. در حقیقت نباید اینگونه تصور شود که در یک واکنش اگر عنصری به حالت آزاد وجود نداشته باشد پس آن واکنش از نوع اکسایش ـ کاهش نمی باشد.
تعریف اکسایش و کاهش شیمی دوازدهم
واکنش های اکسیداسیون و کاهش مانند آتش، اکسیداسیون و انحلال فلزات، تغییر رنگ میوه ها، تنفس و فتوسنتز – فرآیندهای اساسی حیات – رایج و شناخته شده هستند. واکنش های شیمیایی به اشکال مختلف انجام می شود. برخی از این واکنشها، مانند سوختن بنزین و زنگ زدگی آهن، چیزهایی هستند که میت وانیم در زندگی روزمره ببینیم.
واکنش های شیمیایی شامل انتقال الکترون از یک ماده شیمیایی به ماده شیمیایی دیگر است. این واکنشهای انتقال الکترون «واکنش های کاهش اکسیداسیون» یا «واکنش های ردوکس» نامیده می شوند. انرژی با تغییرات گرما، نور، الکتریسیته و سایر پدیده ها با این واکنش ها همراه است. واکنش های اکسیداسیون و کاهش نیز شامل افزودن اکسیژن یا هیدروژن به مواد مختلف است.
تعریف اکسیداسیون از دست دادن الکترون یا افزایش حالت اکسیداسیون یک یون، اتم یا اتم های خاص در یک مولکول است. یک واکنش شیمیایی که شامل ترکیب یک عنصر با اکسیژن است معمولاً به عنوان اکسیداسیون شناخته می شود.احیا فرآیند به دست آوردن الکترون یا کاهش حالت اکسیداسیون یک یون، اتم یا اتم های خاص در یک مولکول است.
افزودن اکسیژن یا یک جزء الکترونگاتیو یا حذف هیدروژن یا یک قطعه الکترونگاتیو به طور کلاسیک به عنوان اکسیداسیون و افزودن هیدروژن یا یک قطعه الکترونگاتیو یا حذف اکسیژن یا یک قسمت الکترونگاتیو به عنوان کاهش شناخته می شود. این نشان می دهد که اکسیداسیون و کاهش فرآیندهای متضاد هستند. دو نوع معرف مختلف برای انجام واکنش اکسیداسیون – احیا مورد نیاز است.
عوامل کاهنده (Reductants): احیا فرآیندی است که شامل افزودن هیدروژن یا هر عنصر الکترومثبت یا حذف اکسیژن یا هر عنصر الکترونگاتیو است. معرفی كه تحت اكسيداسيون قرار می گيرد، عامل احيا كننده ناميده می شود.
عوامل اکسید کننده (اکسیدان): اکسیداسیون فرآیندی است که شامل افزودن اکسیژن یا هر عنصر الکترونگاتیو یا حذف هیدروژن یا هر قسمت الکترومثبتی است. معرفی كه تحت احياء قرار می گيرد، عامل اكسيدان ناميده می شود.
اکسایش و کاهش شیمی دهم فنی
اکسایش و کاهش دو فرایند مهم در شیمی هستند که در بسیاری از واکنش ها نقش کلیدی دارند. این دو فرایند معمولا همزمان اتفاق میافتند و به آنها واکنشهای اکسایش-کاهش یا ردوکس گفته می شود. اکسایش از نظر تعریف یعنی از دست دادن الکترون توسط یک عنصر یا ترکیب. بنابراین زمانی که یک ماده الکترون از دست می دهد دچار اکسایش می شود. مثلاً در واکنش بین آهن و اکسیژن، آهن اکسایش یافته و به اکسید آهن تبدیل می شود.
کاهش یعنی گرفتن الکترون توسط یک ماده دیگر. ماده ای که الکترون دریافت می کند کاهش یافته است. مثلاً در همان واکنش، اکسیژن که الکترون می گیرد کاهش می یابد و به ترکیب اکسید آهن وارد می شود. هر واکنش اکسایش-کاهش شامل دو نیم واکنش است که یکی اکسایش و دیگری کاهش است. الکترون ها در این نیم واکنشها جابهجا می شوند.
در زندگی روزمره، اکسایش و کاهش زیاد دیده می شود. برای مثال، زنگ زدن آهن یک فرایند اکسایش است که باعث تخریب فلزات خصوصا در فضای باز می شود. سوختن سوخت در موتور خودروها و تولید انرژی در سلول های بدن و بسیاری واکنشهای شیمیایی نمونه هایی از این موارد هستند. در آزمایشگاه و صنعت از این واکنش ها برای تولید مواد جدید، تصفیه فلزات، تولید انرژی و حتی درمان های پزشکی استفاده می شود.



















