انرژی یونش چیست؟ – روند تغییرات انرژی یونش
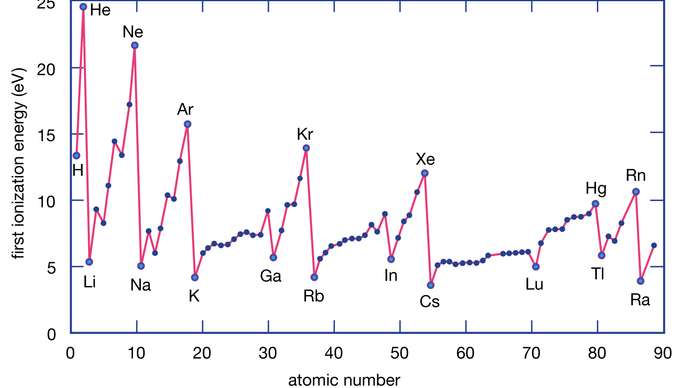
به مقدار انرژی لازم برای جداکردن سست ترین الکترون از یک اتم در حالت گازی و تبدیل آن به یک یون مثبت گازی را انرژی اولین یونش می گویند. این انرژی با واحد کیلوژول بر مول بیان می شود و وقتی اتم خنثی باشد جدا کردن الکترون از آن نسبت به یک یون راحت تر خواهد بود. این مقاله نشریه جهان شیمی فیزیک به تعریف انرژی اولین و دومین یونش و روند تغییر آن در جدول تناوبی عناصر می پردازد.
فهرست مطالب
فهرست مطالب :
۱- تعریف انرژی یونش
۲- انرژی یونش اول، دوم، سوم و بالاتر
۳- روند تغییر انرژی یونش در یک عنصر
۴- روند تغییرات انرژی یونش در جدول تناوبی
۵- استثنا در روند تغییرات انرژی یونش
۶- جهش در عناصر جدول تناوبی
۷- انرژی یونش در مولکول ها
۱- تعریف انرژی یونش :
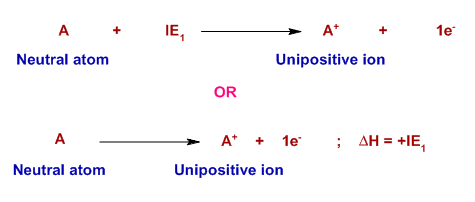
همان طور که گفته شد برای کندن الکترون از یک اتم گازی و تبدیل آن به یک کاتیون گازی انرژی لازم است، به این مقدار انرژی، انرژی یونش یا یونیزاسیون می گویند. چون در این واکنش باید بر نیروی جاذبه بین هسته و الکترون ها غلبه شود انرژی مصرف می شود و علامت این انرژی نیز مثبت است. مثلا انرژی اولین یونش سدیم +۴۹۶ kj ∕ mol است. فرمول اولین انرژی یونش به شکل زیر است.
X(g) + E۱ → X+ (g) + e
نکته :
دانستن انرژی یو نش در تشخیص نوع پیوندهایی که اتم ها می توانند باهم تشکیل دهند به ما کمک می کند. اگر اختلاف انرژی های یو نش دو اتم با هم زیاد باشد (با توجه به اختلاف الکترونگاتیوی)، پیوند بین آن ها یونی خواهد بود. به عنوان مثال انرژی یو نش کلر +۱۲۵۱ kj ∕ mol و برای سدیم هم که در بالا گفته شد، با هم اختلاف زیادی دارد بین آن ها پیوند یونی ایجاد می شود. اما اگر عناصر باهم اختلاف کمی در انرژی های یونششان داشته باشند بین آن ها پیوندهای کووالانسی ایجاد می شود. مثل کربن و اکسیژن که در جدول تناوبی در کنار هم هستند و پیوند کووالانسی تشکیل می دهند.
۲- انرژی یونش اول، دوم، سوم و بالاتر :
برای هر گونه شیمیایی به اندازه تعداد الکترون هایی که دارد می توان انرژی یونش تعریف کرد. میزان انرژی لازم برای جداکردن یک الکترون از اتم خنثی انرژی اولین یونش (IE۱)، انرژی لازم برای جداکردن یک الکترون از یک یون یک بار مثبت گازی و تبدیل آن به یون دو بار مثبت را انرژی دومین یونش (IE۲) می گویند. به همین ترتیب میزان انرژی مصرفی برای جداکردن الکترون از یک یون دو بار مثبت گازی و تبدیل آن به یون سه بار مثبت گازی را نیز انرژی سومین یونش (IE۳) می گویند. به همین ترتیب هر الکترونی که کنده می شود این انرژی به نام شماره آن الکترون خواهد بود.
توجه :
به عبارتی دیگر انرژی nامین یونش به انرژی لازم برای جداکردن الکترون از گونه ای با بار n-1 گفته می شود. در هر یونش نیز ناپایدارترین الکترون با بالاترین سطح انرژی جدا می شود.
۳- روند تغییر انرژی یونش در یک عنصر :
انرژی یو نش از اولین تا بالاترین مرتبه برای هر عنصری زیاد می شود. چون در اولین انرژی یونش الکترون از اتم خنثی جدا می شود ولی دومین الکترون از یک یون مثبت جدا می شود. الکترون ها توسط یون مثبت جذب می شوند و بین آن ها نیروی جاذبه ای که برقرار می شود باعث می شود به میزان انرژی بیشتری احتیاج داشته باشیم. به ترتیب در انرژی های یو نش بعدی بر تعداد بار مثبت کاتیون اضافه شده و میزان جاذبه بار مثبت و الکترون ها افزوده شده و نیروی دافعه بین الکترون ها کمتر خواهد بود و انرژی مصرفی برای جدا کردن الکترون بالاتر خواهد بود.
۴- روند تغییرات انرژی یونش در جدول تناوبی :
با افزایش شعاع اتمی چون فاصله الکترون ها از هسته دورتر می شود، جدا کردن آن از اتم راحت تر بوده و به میزان انرژی کمتری مورد نیاز است. برعکس با کمتر شدن شعاع اتمی انرژی کمتری مصرف می شود.
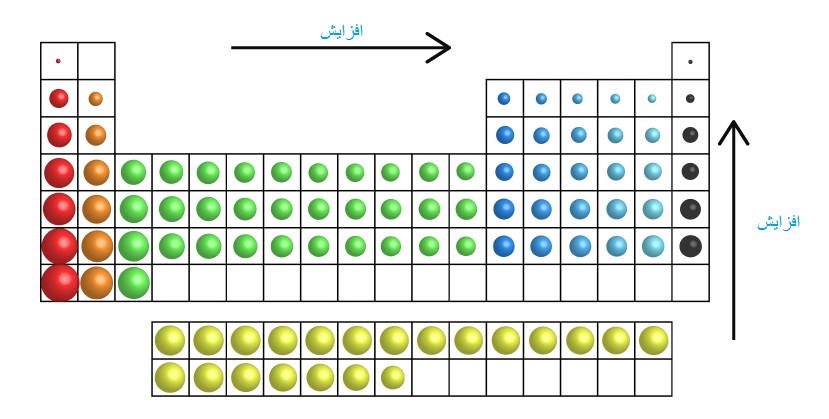
تغییر در گروه :
پس در یک گروه از بالا به پایین جدول و افزایش شعاع اتمی انرژی یو نش کاهش می یابد. در یک گروه با افزایش عدد اتمی بار موثر هسته افزایش می یابد اما این اثر با افزایش تعداد الکترون های داخلی که اثر پوششی دارند، کاسته می شود و با افزایش تعداد لایه های الکترونی و قرار گرفتن الکترون ها در فاصله دورتری نسبت به هسته الکترون ظرفیت آسان تر جدا می شود و به انرژی کمتری نیاز دارد.
تغییر در یک دوره :
در یک دوره از جدول تناوبی به تدریج با حرکت از چپ به راست با کاهش شعاع اتمی انرژی یونش افزایش می یابد. چون در یک تناوب با افزایش عدد اتمی بار موثر هسته افزایش می یابد و شعاع کوچکتر شده، جدا کردن الکترون سخت می شود. در جدول تناوبی عناصر فلوئور بیشترین و سزیم کمترین مقدار انرژی یو نش را دارد.
در عناصر واسطه انرژی مخصوصا در عناصر واسطه داخلی تقریبا ثابت است. چون در این عناصر الکترون متمایز کننده به لایه های داخلی اضافه می شود و با توجه به اثر پوششی این الکترون ها میزان این انرژی قابل توجیه خواهد بود.
توجه :
در کل عناصر گروه اول کمترین و هالوژن ها بیشترین انرژی یونش را دارند و همچنین فلزات انرژی یونش پایین و نافلزات انرژی بیشتری دارند. چون فلزات در هنگام واکنش شیمیایی تمایل به از دست دادن الکترون و نافلزات میل به گرفتن الکترون دارند.
۵- استثنا در روند تغییرات انرژی یونش :
در بین این قوانین منظم تغییرات انرژی در یک دوره و گروه عناصر گروه دوم (فلزات قلیایی خاکی) و عناصر گروه ۱۵ (گروه نیتروژن) از این روند تبعیت نمی کند. انرژی عناصر گروه سوم (مثلا بور) کمتر از عناصر گروه دوم (بریلیم) است. این استثنا با آرایش الکترونی آن ها قابل توضیح است. در بریلیم الکترون باید از اوربیتال پر و پایدار 2S جدا شود، اما در بور از اوربیتال نیمه پر 2P جدا می شود. اوربیتال 2S در فاصله نزدیک تری نسبت به اوربیتال 2P نسبت به هسته قرار دارد. پس جدا کردن الکترون از اتم بور راحت تر بوده و به انرژی کمتری نیاز است.
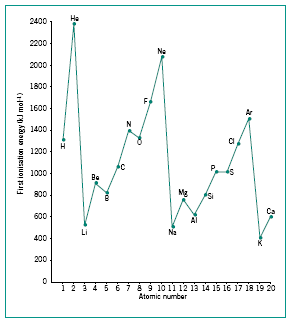
توجه :
این روند در تناوب سوم از منیزیم به آلومینیم و در تناوب چهارم از کلسیم به گالیم نیز صدق می کند. ولی در دوره های پنجم و ششم این حالت های استثنا صادق نیست و انرژی این دوره ها از قانون کلی افزایش در جدول تناوبی تبعیت می کنند.
همچنین :
استثنای دیگر، انرژی اتم نیتروژن از گروه ۱۵ باید کمتر از اکسیژن از گروه ۱۶ باشد، اما نیتروژن انرژی بیشتری دارد. چون نیتروژن دارای آرایش نیمه پر و پایدار P۳ است و این سه الکترون طبق قاعده هوند در سه اوربیتال P و با جهت های اسپین یکسان قرار گرفتند. اما در اکسیژن چهار الکترون در این سه اوربیتال قرار دارند. این الکترون اضافی نسبت به نیتروژن در یکی از این اوربیتال ها به صورت جفت شده وجود دارد که دافعه بین آن ها باعث می شود انرژی کمتری برای جدا کردن آن ها مصرف شود تا به حالت پایدار سه تایی مثل نیتروژن برسند.
پس:
در نیتروژن انرژی زیادی لازم است تا یک الکترون جدا شود چون از حالت پایدار خارج می شود. در اینجا نیز این حالت های استثنا در تناوب های سوم از فسفر به گوگرد و چهارم از آرسنیک به سلنیم نیز صادق، ولی در تناوب های پنجم و ششم صادق نیست.
۶- جهش در عناصر جدول تناوبی :
گفته شد انرژیهای یونش یک عنصر با افزایش مرتبه واکنش به علت افزایش تعداد بار مثبت و نیروی جاذبه افزایش می یابد. اما در بین این تغییرات دو نوع جهش (افزایش ناگهانی در مقدار انرژی) دیده می شود. وقتی در آرایش الکترونی اتم ها لایه ها عوض شود و الکترون از یک لایه دیگر برداشته شود جهش بزرگ اتفاق می افتد. اگر زیرلایه عوض شود جهش کوچک خواهیم داشت. به عنوان مثال در فسفر ۱۵ را با توجه به آرایش الکترونی آن داریم.
P : 1s۲ 2s۲ 2p۶ 3s۲ 3p۳
پس :
با توجه به آرایش الکترونی از IE۵ به IE۶ جهش بزرگ داریم چون لایه الکترونی از n = 3 به n = 2 تغییر می یابد. یک جهش بزرگ دیگر در مقدار IE۱۳ به IE۱۴ به دلیل تغییر لایه از n = 2 به n = 1 خواهیم داشت. در فسفر دو جهش کوچک نیز از IE۳ به IE۴ و از IE۱۱ به IE۱۲ داریم. این جهش های کوچک به ترتیب به خاطر تغییر زیرلایه ها از 3p به 3s و از 2p به 2s است.
نکته :
تشخیص جهش های بزرگ بسیار راحت تر از جهش های کوچک است. چون تغییرات انرژی در جهش های بزرگ خیلی بزرگ و گاهی چهار تا پنج برابر ولی در جهش های کوچک کمتر از دو برابر است.
۷- انرژی یونش در مولکول ها :
همان گونه که برای اتم ها این انرژی تعریف می شود می توانیم برای مولکول ها نیز انرژی یونش را به صورت میزان انرژی لازم برای جدا کردن الکترون از مولکول در فاز گازی را تعریف کنیم. برای مولکول اکسیژن داریم :
O۲ (g) → O۲+ (g) + e



















