محلول اشباع و فوق اشباع چیست؟ – طرز تهیه این محلول ها

محلول اشباع محلولی است که در آن ماده حل شونده به میزانی بیشتر از انحلال پذیری آن به حلال اضافه می شود. اگر مقدار بیشتری حل شونده به محلول اشباع اضافه شود، ماده به صورت جامد ته نشین می شود و به این محلول، فوق اشباع می گویند. در این مقاله نشریه جهان شیمی فیزیک به بررسی خواص این محلول ها می پردازیم.
فهرست مطالب
تعریف محلول
به مخلوط های همگن محلول می گویند که بر اساس حالت فیزیکی به سه دسته محلول های گازی، جامد و مایع تقسیم می شود. هوا مهم ترین محلول گازی است که رفتار آن ها با قانون فشارهای جزئی دالتون توصیف می شود. آلیاژها نیز از مهم ترین محلول های جامد هستند که سکه ی نقره ای که محلولی از مس و نقره است، نمونه ای از این محلول هاست. محلول های دسته سوم، مایع هستند که بیشترین کاربرد را در علم شیمی دارند. به محلول یکنواختی که از حل کردن حل شونده در حلال به دست می آید محلول غیراشباع می گویند.
هر محلولی از دو جزء حلال و حل شونده تشکیل شده که حلال مقدار بیشتری در محلول نسبت به حل شونده دارد و این راه شناسایی آن ها از یکدیگر در یک محلول است.
تعریف محلول اشباع
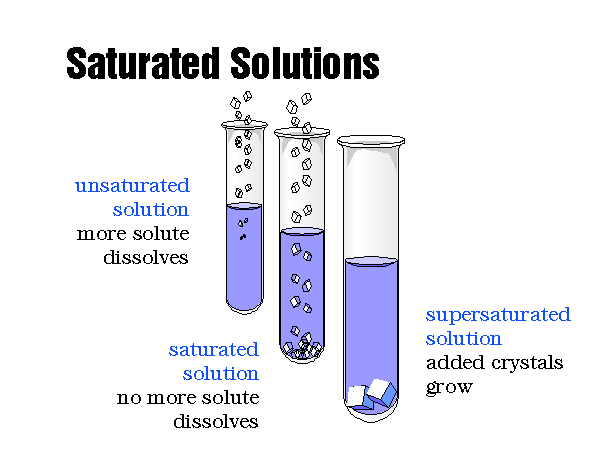
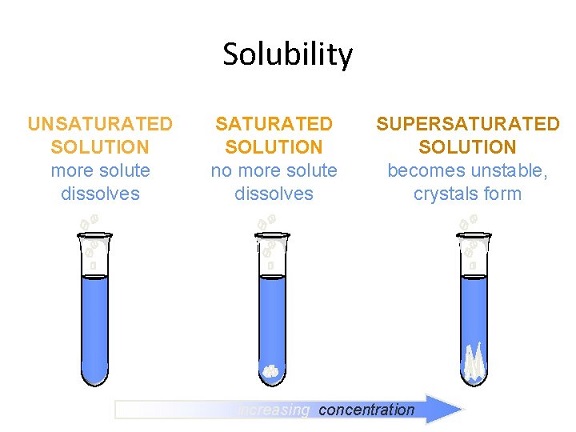
حال اگر ماده حل شونده به مقداری از حلال بیشتر از میزان انحلال پذیری آن اضافه شود، به حدی که دیگر نتواند در حلال حل شود، محلول اشباع یا سیر شده به دست می آید. به محلول غیراشباع ماده حل شونده اضافه می شود و محلول اشباع به دست می آید. در محلول اشباع بین ماده حل شونده و حلال تعادل برقرار می شود. وقتی تعادل برقرار شد، سرعت حل شدن ماده حل شونده با سرعت خارج شدن ماده از محلول برابر است و غلظت ماده حل شونده ثابت می ماند.
اگر محلول گازی باشد مقدار اضافی حل شونده به صورت گاز خارج می شود. همچنین در هنگام تهیه محلول اشباع باید دما ثابت باشد. چون تغییرات دما در میزان انحلال پذیری یک ماده در حلال اثر می گذارد.
تعریف محلول فوق اشباع
در نقطه اشباع با اضافه کردن ماده حل شونده بیشتر، غلظت تغییری نمی کند و مقدار اضافی ماده حل شونده به صورت جامد ته نشین می شود. به این محلول فوق اشباع یا فراسیرشده گفته می شود و یک محلول ناپایدار است. در محلول فوق اشباع مقدار ماده حل شونده بیشتر از مقدار آن در محلول اشباع است و این مقدار در محلول رسوب می کند.
چون حلالیت اکثر مواد جامد با زیاد کردن دما افزایش پیدا می کند، وقتی محلول اشباع در دمای بالا به دست آید، میزان ماده حل شونده در آن در دمای بالا بیشتر از دمای پایین خواهد بود. پس این محلول در دمای بالا یک محلول اشباع است اما وقتی سرد شد، یک محلول فوق اشباع خواهد بود. با افزودن یک بلور به یک محلول ناپایدار فوق اشباع تبلور انجام می شود. هر ماده ای وقتی حل می شود گرما مصرف می کند و وقتی متبلور شد، این گرما را از دست می دهد.
تهیه محلول اشباع و فوق اشباع
به عنوان مثال در ظرفی آب داریم و به آن کم کم نمک اضافه می کنیم. نمک در آب همراه با هم زدن حل می شود. افزودن نمک به محلول تا جایی پیش می رود که دیگر حلال نمی تواند نمک ریخته شده را در خود حل کند و نمک به صورت جامد می ماند، اینجاست که محلول اشباع به دست آمده است. اگر این آزمایش را در آب مقطر انجام دهیم می توانیم میزان انحلال پذیری آن را محاسبه کنیم (انحلال پذیری آن حدود ۳۵ گرم نمک در ۱۰۰ سی سی آب است). اگر نمک بیشتری اضافه کنیم مقدار اضافی در انتهای ظرف رسوب می کند و محلول فوق اشباع (ابرسیرشده) نمک در آب حاصل می شود.
روشی دیگر که می توان یک محلول اشباع تهیه کرد این است که یک محلول غیراشیاع را تبخیر کنیم. اگر به محلول فوق اشباع یک تکه بلور اضافه کنیم، مقدار اضافی ماده حل شده به آن تکه چسبیده و باعث تشکیل بلور بزرگ ترمی شود. با این روش نیز یک محلول اشباع به دست می آید.

تعریف انحلال پذیری وعوامل موثر بر آن
بیشترین مقداری از یک حل شونده که در دما و فشار معین، در مقدار معینی از یک حلال مخصوص حل می شود، را انحلال پذیری آن ماده گویند. انحلال پذیری به صورت جرم حل شونده به حجم یا جرم حلال بیان می شود. میزان انحلال پذیری مواد به عوامل زیر بستگی دارد.
رابطه ماده حل شونده و حلال
اولین عاملی که در انحلال مواد در هم نقش دارد رابطه ای است که مواد حل شونده و حلال باهم دارند. مواد قطبی در حلال های قطبی و مواد غیرقطبی در حلال های غیرقطبی بهتر حل می شوند. یک قانون کلی این است که مواد مشابه همدیگر را بهتر حل می کنند.
اثر یون مشترک
وقتی در یک محلولی که در حالت تعادل شیمیایی است نمکی اضافه شود که یون آن در محلول وجود داشته باشد (یون مشترک)، حلالیت آن کم می شود.
اندازه ماده حل شونده
هر چه ماده حل شونده کوچک تر باشد بهتر در حلال حل می شود. چون سطح تماس مواد حل شونده با مولکول های حلال بیشتر شده انحلال پذیری راحت تر انجام می شود.
دما
اثر دما در انحلال مواد با توجه به این که واکنش گرماگیر یا گرمازاست، بر طبق اصل لوشاتلیه متفاوت خواهد بود. در واکنش گرماگیر (مواد واکنش دهنده جامد و حل شونده هستند)، چون در تعادلی که در محلول ایجاد شده گرما در سمت واکنش دهنده در واکنش شیمیایی است، افزایش دما باعث می شود که تعادل به سمت راست واکنش پیشرفت کند و انحلال پذیری افزایش یابد و دوباره تعادل برقرار شود. اما در واکنش گرماده (مواد واکنش دهنده جامد و حل شونده باشند)، برعکس افزایش دما باعث پیشرفت واکنش به سمت چپ می شود و انحلال پذیری مواد حل شونده کاهش می یابد.
افزایش یا کاهش دما در انحلال پذیری مایعات بی تاثیر است. اما افزایش دما انحلال پذیری گازها را کاهش و کاهش دما انحلال پذیری آن ها را افزایش می دهد.
نمونه هایی از محلول غیراشباع
همان طور که گفته شد در محلول غیراشباع، غلظت ماده حل شونده خیلی پایین تر از غلظت آن در حالت تعادل است. بیشتر محلول هایی که در طبیعت وجود دارند محلول های غیراشباع هستند. نمکی که به غذا اضافه می شود، قند و شکری که در چایی و قهوه حل می شود، نمونه هایی از محلول های غیراشباع جامدات درحلال هاست. همچنین هوا نمونه ای از محلول گازی است.
نمونه هایی از محلول اشباع
بسیاری از غذاها و شیرینی ها دارای دستور پختی شامل تهبه محلول های اشباع هستند. تهیه این غذاها به دما بستگی دارد. وقتی مربا در دمای بالا تهیه می شود حلالیت شکر در آن افزایش می یابد. وقتی در تهیه مربا در دمای بالا به نقطه اشباع برسیم، هنگام سرد شدن لایه ای از شکر روی مربا تشکیل می شود. خاک محلولی اشباع از نیتروژن است که در نقطه اشباع گاز هیدروژن از آن خارج می شود.
محلول فرا سیر شده چیست
اشباع یا سیر شده حالتی است که یک محلول حداکثر مقدار املاحی را که می تواند در دما و فشار خاصی در خود نگه دارد حل کرده باشد. در این شرایط، هیچ املاح اضافی را نمی توان در حلال حل کرد. تعادل حلالیت تعادل دینامیکی بین املاح محلول و شکل جامد آن در محلول است. فرا شیر شده یا فوق اشباع زمانی اتفاق می افتد که غلظت املاح در یک محلول از حلالیت آن در دما و فشار خاص فراتر رود. این بدان معناست که محلول حاوی املاح محلول بیشتری نسبت به آنچه که در تعادل حلالیت معمولی ممکن است وجود دارد.
راه های مختلفی وجود دارد که می توان یک محلول فرا سیر شده ایجاد کرد. برخی از آنها عبارتند از: ۱. سرد شدن سریع: اگر محلول اشباع شده به سرعت سرد شود، حلالیت املاح کاهش می یابد، اما املاح ممکن است زمان کافی برای رسوب دادن نداشته باشد. این می تواند منجر به یک محلول فوق اشباع شود. ۲. تبخیر سریع: هنگامی که حلال به سرعت تبخیر می شود، املاح نمی تواند به اندازه کافی سریع رسوب کند و در نتیجه یک محلول فوق اشباع ایجاد می شود. ۳. محلول های فوق اشباع پایدار: برخی از املاح می توانند محلول های فوق اشباع پایدار را در جایی که تعادل حلالیت به هم نخورد، حتی اگر غلظت املاح از نقطه اشباع بیشتر شود، تشکیل دهند.
توجه به این نکته مهم است که حلالیت یک مقدار ثابت نیست. می تواند با دما، فشار و ماهیت حلال و املاح تغییر کند. به عنوان مثال، گازها در مایعات سرد بیشتر از مایعات گرم حل می شوند، در حالی که اکثر املاح جامد با افزایش دما، حلالیت خود را افزایش می دهند. این تغییرات در حلالیت با شرایط مختلف نقش مهمی در فرآیندهای آماده سازی محلول، خالص سازی و تبلور در آزمایشگاه ها و صنایع شیمیایی دارد.



















