
عنصر ایتریم (Yttrium) با نماد شیمیایی Y، یکی از عناصر شیمیایی جدول تناوبی است که عدد اتمی آن ۳۹ است. این عنصر در حقیقت سی و نهمین عنصر از جدول تناوبی بوده که در گروه IIIB و دوره پنجم جدول تناوبی قرار دارد. در واقع عنصر ایتریوم یک فلز واسطه (Transition Metals) نرم به رنگ سفید نقره ای یا خاکستری تیره است. این فلز با عناصر اسکاندیم (Sc)، لانتانید ها و اکتینید ها در گروه سه واسطه جدول تناوبی قرار گرفته است. در ادامه این مقاله در نشریه جهان شیمی فیزیک به بررسی عنصر ایتریوم پرداخته می شود. لطفا با ما همراه باشید.
فهرست مطالب این مقاله
۱- تاریخچه کشف عنصر ایتریم
۲- پیدایش و منابع عنصر شماره ۳۹ جدول تناوبی
۳- ویژگی های فیزیکی و شیمیایی عنصر ایتریم
۴- ایزوتوپ های عنصر ایتریم
۵- کاربرد های عنصر ایتریم
۶- ترکیبات عنصر ایتریم
۷- خطرات ایتریم بر روی سلامتی انسان
۸- طریقه نگهداری فلز ایتریوم
فهرست مطالب
تاریخچه کشف عنصر ایتریم
برای اولین بار در سال ۱۷۸۷ میلادی، کارل آرنیوس (Carl Axel Arrhenius) در یک معدن قدیمی در نزدیکی شهر استکهلم، یک سنگ معدنی سیاه غیر معمول را پیدا کرد. وی تصور می کرد که یک کانی معدنی جدید تنگستن یافته است. از این رو، نمونه را برای شیمیدان فنلاندی جوهان گادولینا (Johann Gadolin) در فنلاند ارسال کرد. بنابراین می توان گفت که ایتریا (اکسید ایتریوم یا Y۲O۳) برای نخستین بار در سال ۱۷۹۴ میلادی، توسط گادولینا در فنلاند کشف شد. بعد از آن، در سال ۱۸۲۸ میلادی، شیمیدان آلماني، فردريش ولر (Friedrich ohler)، به نمونه خالص آن دست يافت.

این عنصر در حقیقت از یک کانی معدنی به نام گادولینیت که در روستای ایتربای وجود دارد استخراج شد. این معدن سنگی شامل كانی هاي حاوی اين عنصر است. به عبارت دیگر، عنصر ايتريم يكی از چهار عنصری است كه از معادن سنگی شهر ايتربای سوئد استخراج گردیده است. همانطور که مشخص است نام این عنصر از روستای ایتربای گرفته شده است. سه عنصر ديگر عبارتند از اربيم (Erbium)، تربيم (Terbium) و ايتربيم (Ytterbium). عنصر ايتريوم برخلاف سه عنصر ديگر، در سری لانتانيد ها یا فلزات خاك های كمياب قرار ندارد. با این وجود و از آنجاییکه با عناصر لانتانيد ها در يك گروه واسطه قرار دارد، بنابراین خواص بسیار مشابه با آنها را نشان می دهد. لازم به ذکر است که حتی گهگاهی به مجموعه چهارتایی آنها، فلزات ايتريم نیز گفته می شود.
پیدایش و منابع عنصر شماره ۳۹ جدول تناوبی
عنصر ایتریوم در طبیعت به عنوان یک عنصر آزاد هرگز پیدا نمی شود. این فلز به طور تقریبی در بیشتر مواد معدنی کمیاب و همچنین در سنگ معدن اورانیوم یافت می شود. لازم به ذکر است که جدا کردن این عنصر از سایر عناصر کمیاب بسیار سخت می باشد. منابع تجاری اصلی ایتریوم عبارتند از كانی های منازيت، بستنازيت و گادولينيت. این عنصر همچنین به وسیله فرآیند کاهش فلورید ایتریم به کمک فلز کلسیم تولید می شود، اما می توان آن را به وسیله روش های دیگر نیز تولید نمود. نکته جالب اینست که این عنصر در سنگ های آورده شده به زمین به وسیله آپولو یازده از سفر به کره ماه، مقدار زیادی از این فلز به حالت آزاد پیدا شده است.

ویژگی های فیزیکی و شیمیایی عنصر ایتریم
عنصر ایتریوم، در واقع فلزی براق، فروزنده و کمیاب است. در حالیکه اغلب ترکیباتش بی رنگ هستند. خصوصیات قابل توجه ایتریم از ساختار اتمی ([۳۶Kr] 4d۱5s۲) آن ناشی می شود. همانطور که مشخص است، اوربیتال d لایه ماقبل آخر در این عنصر در حال پر شدن است. این عنصر به واسطه آرایش الکترونی که دارد، در دسته فلزات واسطه قرار می گیرد. فلزات واسطه در حقیقت بین فلزات قلیایی خاکی (گروه دوم) و عناصر گروه بور در جدول تناوبی قرار گرفته اند. به عناصر واسطه، عناصر گروه B نیز گفته می شود.
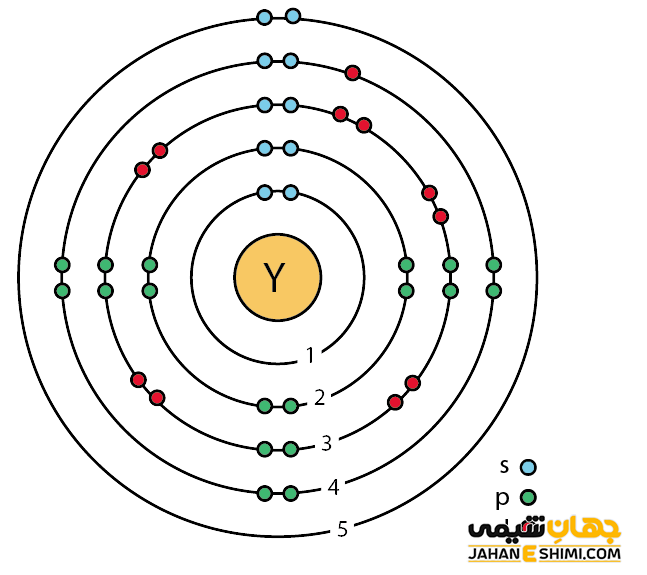
با توجه به آرایش الکترونی مشخص است که سه الکترون در دورترین لایه الکترونی ایتریم وجود دارد. پس در بیشتر ترکیبات به صورت یون سه بار مثبت (+Y۳) ظاهر می شود. دقت داشته باشید که خواص شیمیایی عنصر ایتریم شباهت زیادی به عناصر گروه لانتانید ها دارد. این فلز با آب سرد به آرامی واکنش می دهد، درحالیکه به سرعت با آب گرم وارد واکنش می شود. در حقیقت آب را تجزیه می کند و هیدروکسید ایتریوم و گاز هیدروژن محصولات این واکنش می باشند. علاوه بر آن، این فلز در هوا نسبتا مقاوم است. اما خرده های آن در دماهای بالاتر از ۴۰۰ درجه سانتیگراد در هوا مشتعل می شوند. به بیان دیگر، اگر فلز ایتریوم به ذرات بسیار کوچک تقسیم گردد، مقاومت خود را در مقابل هوا از دست خواهد داد. فلز ایتریم در اسید های رقیق و هیدروکسید پتاسیم محلول است. ایتریوم فلزی خورنده است.
از دیگر ویژگی های عنصر شماره ۳۹ جدول تناوبی می توان به موارد زیر اشاره کرد.
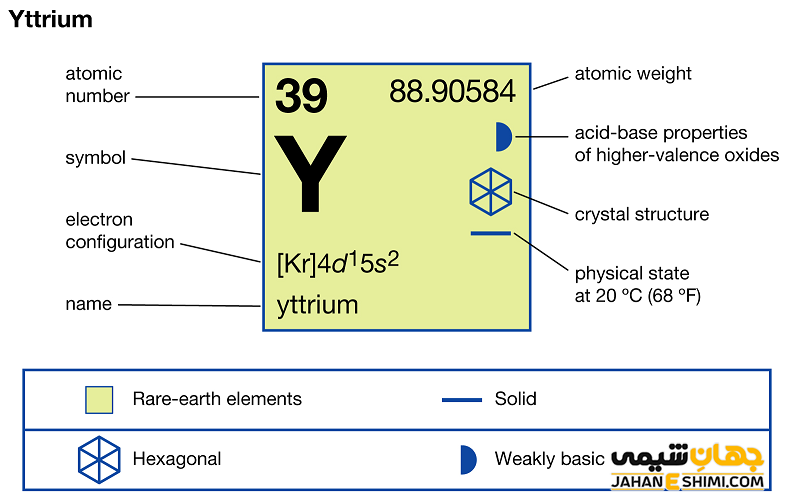
- حالت فیزیکی آن در دمای ۲۵ درجه سلسیوس و فشار ۱ اتمسفر به صورت جامد است.
- دمای ذوب و دمای جوش این عنصر به ترتیب ۱۵۲۶ و ۳۳۳۶ درجه سانتی گراد است.
- عنصر ایتریم در هوا به سرعت اکسید نمی شود.
- ساختار بلوری آن به شکل شش گوشه (Hexagonal) است.
- این عنصر آلوتروپ ندارد.
- جرم اتمی ایتریم برابر با ۸۸.۹۰۵۸۵ g/mol است.
- چگالی آن نیز برابر با ۴.۴۷۲ g/cm۳ می باشد.
- یون های ایتریم معمولا عدد اکسایش برابر با اعداد ۰، +۱، +۲ و +۳ را دارند. توجه کنید که عدد اکسایش +۳ از اعداد اکسایش متداول تر ایتریوم است.
- انرژی یونیزاسیون آن برابر با ۶۰۰ kJ/mol است.
ایزوتوپ های عنصر ایتریم
همانطور که در مقالات پیشین نشریه بیان شده است، ایزوتوپ های یک عنصر، تنها در تعداد نوترون ها با هم تفاوت دارند. ایتریم طبیعی تنها از یک ایزوتوپ پایدار ۸۹Y (100 %) تشکیل شده است. علاوه بر آن، ۲۶ ایزوتوپ ناپایدار ایتریوم نیز شناخته شده است. پایدارترین رادیو ایزوتوپ اکتیو آن، یعنی ۸۸Y با نیمه عمر ۱۰۶/۶۵ روز و همچنین ایزوتوپ ۹۱Y با نیمه عمر ۵۸/۵۱ روز شناخته شده اند. معمولا دیگر ایزوتوپ های آن، نیمه عمری کمتر از حتی یک روز دارند. در جدول زیر نیمه عمر تعدادی از رادیو ایزوتوپ های فلز ایتریم را مشاهده می کنید.
| نیمه عمر | ایزوتوپ |
| ۱۴/۷۴ ساعت | Y-86 |
| ۳/۳۵ روز | Y-87 |
| ۱۰۶/۶ روز | Y-88 |
| ۲/۶۷ روز | Y-90 |
| ۳/۱۹ ساعت | Y-90m |
| ۵۸/۵۱ روز | Y-91 |
| ۴۹/۷۱ دقیقه | Y-91m |
| ۳/۵۴ ساعت | Y-92 |
| ۱۰/۲ ساعت | Y-93 |

کاربرد های عنصر ایتریم
عنصر ایتریم یکی از کمیاب ترین عناصر شیمیایی است که می تواند در خانه و در وسایلی همچون مانیتور و تلویزیون های رنگی، لامپ های ذخیره انرژی، لامپ های فلورسنت و شیشه ها یافت شود. کاربرد های آن همچنان در حال افزایش است. زیرا به منظور تولید کاتالیزور و صیقل دادن شیشه ها گزینه مناسبی است. بیشترین کاربرد ایترویوم در صنعت سرامیک و فسفر است. در حالیکه مقادیر کمتری از آن در صنایع متالورژی، پرداخت شیشه، کاتالیزور و مواد افزودنی استفاده می شود. علاوه بر آن، کاربرد های الکترونیکی نیز برای این ماده وجود دارد. از میان این کاربرد های الکترونیکی، سنسور های اکسیژن بسیار مهم اند.
اکسید ایتریوم کاربرد های ویژه ای دارد. مثلا قبل از کشف مانیتور و تلویزیون های صفحه تخت، دستگاه های قدیمی دارای لوله های بزرگ شیشه ای و سیستم اشعه کاتدی بودند. در واقع تصاویر را بر روی یک صفحه، نمایش می دادند. ترکیب اکسید ایتریوم با عنصر اوروپیم، رنگ قرمز لامپ تصویر تلویزیون های رنگی را فراهم می کرد. علاوه بر آن، اکسید ایترویوم در ساخت گارنت آهن-ایتریوم کاربرد دارد. این کامپوزیت، فیلتر های مایکروویو بسیار مناسب و موثری می باشند. همچنین در فناوری رادار و ارتباطات نیز کاربرد دارند. اکسید ایتریم در شیشه می تواند شیشه ها را نسبت به حرارت و ضربه مقاوم کند. همچنین در ساخت لنز های دوربین استفاده شود. این اکسید به منظور ساخت ابر هادی ها نیز مناسب است. ابر هادی ها در واقع به اکسید فلزاتی گفته می شود که می توانند جریان الکتریسیته را بدون هیچگونه اتلاف انرژی هدایت نمایند.

جالب است بدانید که
عنصر شماره ۳۹ جدول تناوبی کاربرد های پزشکی نیز دارد. به عنوان مثال، ایزوتوپ رادیواکتیو ایتریوم ۹۰ در پرتو درمانی جهت درمان سرطان کبد و تعدادی دیگر از سرطان ها کاربرد دارد. علاوه بر آن، سوزن هاي داراي این ایزوتوپ رادیواکتیو، به کمک تشعشع می توانند به طور دقیق عصب هاي انتقال دهنده درد در نخاع را از بين ببرند. قطعا اين روش نسبت به روش سنتي استفاده از چاقوی جراحی جهت پاره كردن اعصاب انتقال دهنده درد، بسيار بهتر خواهد بود. از طرفی دیگر این عنصر در ساخت لیزر های پزشکی نیز بکار می رود. علاوه بر موارد ذکر شده، از اکسید ایتریم جهت تثبیت زیرکونیا در سرامیک های دندانی بدون فلز بهره می برند.
دیگر کاربرد های ترکیبات ایتریم
- در گذشته گارنت های مصنوعی تولید شده از کامپوزیت ایتریم-آلومینیوم به عنوان الماس شبیه سازی شده و یا دیگر سنگ های قیمتی فروخته می شدند. اما امروزه به جای آنها از زیرکونیا مکعبی استفاده می گردد. در حال حاضر، گارنت های ایتریم-آلومینیوم به عنوان بلور هایی بکار می روند که نور را در لیزر های صنعتی تقویت می نمایند.
- این عنصر برای کاهش عنصر وانادیوم و یا دیگر غیر فلزات بکار می رود.
- فلز ايتريم در آلياژ های فولاد باعث افزايش مقاومت در برابر خوردگی می شود.
- تعدادی از ليزر ها و همچنین سراميك هاي ابر رسانا نيز دارای ايتريم می باشند.
- ایتریوم در ساخت چدن گره دار نیز شناخته شده است. زیرا زمانی که به چدن اضافه شود، می تواند آن را کار پذیر تر کند. در حقیقت خاصیت رسانایی چدن را افزایش می دهد.
- ایتریم فلزی می تواند در مقادیر بسیار کم برای آلیاژ سازی استفاده شود. بدین صورت استحکام آلیاژ هایی مثل آلومینیوم و منیزیم را بالا می برد.
- این فلز همچنین می تواند جهت کم کردن اندازه دانه های کروبیوم، مولیبدنوم و زیرکنونیوم بکار برده شود.
- با وجود اینکه فلزات به طور معمول هادی حرارت اند، اما آلیاژی از فلزات ایتریوم، آلومینیوم و کروم وجود دارد که در حقیقت عایق حرارت خواهد بود.
- خاصیت مغناطیسی آهن- ایتریوم، آلومینیوم و گادولینیوم بسیار جالب است، این ترکیبات می تواند به عنوان فرستنده و یا پخش کننده انرژی شنوایی بکار روند و موثر باشند.

ترکیبات عنصر ایتریم
همانطور که بیان شد اکسید ایتریوم (Y۲O۳) از مهمترین ترکیبات فلز ایتریوم است. از دیگر ترکیبات معدنی آن می توا به موارد زیر اشاره کرد.
- ایتریم (III) آرسنید (YAs)
- ایتریم آلومینیم گارنت (Y۳Al۱۳O۵)
- ایتریم (III) آنتیموانید (YSb)
- ایتریم آهن گارنت (Y۳Fe۵O۱۲)
- ایتریم ایریدیوم (YIr)
- ایتریم باریم مس اکسید (YBa۲Cu۳O۷)
- ایتریم (III) برمید (YBr۳)
- ایتریم رودیم (YRh)
- ایتریم روی (YZn)
- ایتریم (III) سولفید (Y۲S۳)
- ایتریم طلا (YAu)
- ایتریم (III) فلورید (YF۳)
- ایتریم کادمیوم (YCd)
- ایتریم(III) کلرید (YbCl۳)
- ایتریم مس (YCu)
- ایتریم منیزیوم (YMg)
- ایتریم نقره (YAg)

خطرات ایتریم بر روی سلامتی انسان
عنصر ایتریم در طبیعت خیلی کم و به مقدار بسیار ناچیز پیدا می شود. اگرچه ترکیبات حاوی آن، بسیار سمی می باشند، اما خوشبختانه به ندرت در دسترس انسان قرار دارند. از آنجاییکه این عنصر معمولا در بافت انسانی وجود ندارد، پس نقش حیاتی نیز در زندگی ما بازی نمی کند. لازم به ذکر است که وجود ایتریوم در محیط کار، بسیار خطرناک است. زیرا در این محیط می تواند از طریق هوا استنشاق شود. در واقع استنشاق طولانی مدت آن، باعث ایجاد حباب در ریه خواهد شد. همچنین می تواند سبب سرطان هم باشد. به بیان دیگر، تنفس آن احتمال سرطان ریه را افزایش می دهد. از طرفی دیگر، تجمع ایتریوم در بدن مطمینا برای کبد مضر است. از طرفی دیگر، نمک های ایتریوم نیز ممکن است سرطان زا باشند.
این عنصر در اثر تولید نفت و صنایع تولید کننده بنزین در محیط زیست پراکنده می شود. همچنین زمانی که لوازم خانه حاوی ایتریوم بیرون ریخته می شوند، می توانند باعث شوند که ایتریم دوباره وارد محیط زیست گردد. به علاوه ایتریم به تدریج در خاک و آب جمع می شود. در نتیجه غلظت آن در بدن موجودات زنده و ذرات خاک افزایش پیدا می کند. تحقیقات نشان داده است که در جانوران دریایی و حیوانات آبزی، عنصر ایتریم می تواند باعث آسیب غشای سلولی گردد. در نهایت بر روی تولید مثل و همچنین عملکرد سیستم عصبی آنها اثر منفی بگذارد.
طریقه نگهداری فلز ایتریوم
همانگونه که بیان شد، اگر در هوا به عنصر ایتریم گرما دهید، شعله ور مي شود. از آنجاییکه لایه ای نازك از اکسید این فلز، بر روی آن قرار گرفته است، این فلز در هوا نسبتا پایدار است. زیرا این لایه نازک آن را از واکنش با اکسیژن در امان نگه می دارد. اما گرد این فلز می تواند در دما های بالا به طور خود به خود با اکسیژن واکنش دهد. به عبارت دیگر، این عنصر میل ترکیبی فراوانی به اکسیژن نشان می دهد. بنابراین باید از غلظت بالای اکسیژن دور نگه داشته شود.



















