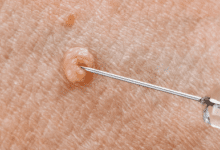
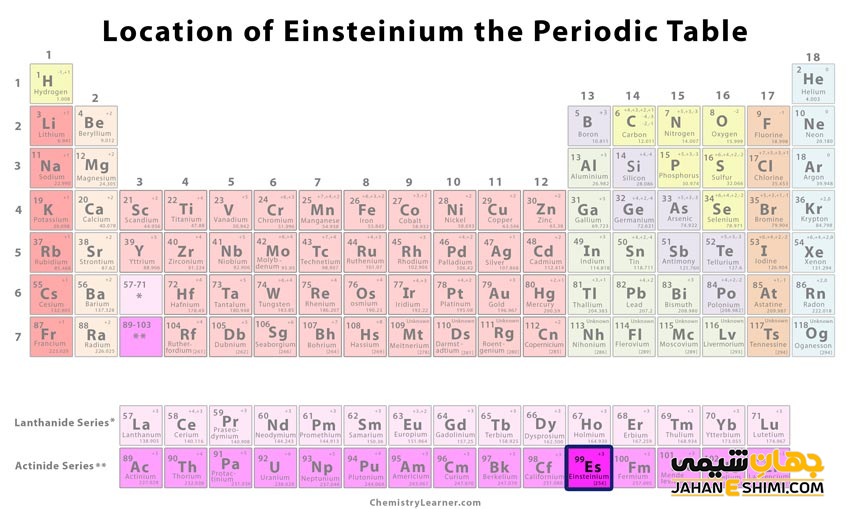
عنصر اینشتینیم (Einsteinium) با نماد شیمیایی Es، یکی از عناصر شیمیایی جدول مندلیف است که عدد اتمی آن ۹۹ می باشد. این عنصر در حقیقت نود و نهمین عنصر از جدول تناوبی عناصر بوده که در گروه IIIB و تناوب هفتم جدول تناوبی قرار گرفته است. در واقع عنصر اینشتینیم یک فلز واسطه (Transition Metals) نرم، رادیواکتیو به رنگ نقره اي و از عناصر سنتزی گروه اکتینید ها است. این فلز با عناصر اسکاندیم (Sc)، ایتریم (Y) و لانتان (La)، در گروه سه واسطه جدول تناوبی قرار دارد. در ادامه این مقاله در نشریه جهان شیمی فیزیک به بررسی عنصر اینشتینیوم پرداخته می شود. لطفا با ما همراه باشید.
تاریخچه کشف عنصر اینشتینیم
عنصر اینشتینیم برای اولین بار در سال ۱۹۵۲ میلادی، توسط آلبرت غیورسو (Albert Ghiorso)و همکارانش در دانشگاه کالیفرنیا برکلی و با همکاری آزمایشگاه های ملی آرگون (Argonne National Laboratory) و لوس آلاموس (Los Alamos National Laboratory)، در نتیجه آزمایش هسته ای آیوی مایک (Ivy Mike) در ایالات متحده امریکا شناسایی شد. این عنصر به عنوان جزئی از بقایای رادیواکتیو اولین بمب هیدروژنی در اقیانوس آرام کشف شده است. در واقع رادیوایزوتوپ اینشتینیم ۲۵۳ در این انفجار تولید شد. نام این عنصر به افتخار دانشمند برجسته تاریخ یعنی آلبرت اینشتین روی آن گذاشته شده است.

پیدایش و منابع عنصر شماره ۹۹ جدول تناوبی
عنصر اینشتینیم به طور طبیعی وجود ندارد، بنابراین در پوسته زمین یافت نشده است. در سال ۱۹۶۱ میلادی و برای جدا کردن مقدار ماکروسکوپی از ایزوتوپ اینشتینیم ۲۵۳، مقدار کافی از آن سنتز شد. وزن این نمونه آزمایشگاهی در حدود ۰/۰۱ میلی گرم بود. لازم به ذکر است که جرم آن به کمک تعادل مغناطیسی اندازه گیری شده است. علاوه بر آن، در آزمایشگاه ملی اواک ریج، با استفاده از تابش مقدار یک کیلوگرم پلوتونیم ۲۳۹ در یک راکتور هسته ای و ظرف مدت چند سال، توانستند ۳ میلی گرم اینشتینیم سنتز کنند.
ویژگی های فیزیکی و شیمیایی عنصر اینشتینیم
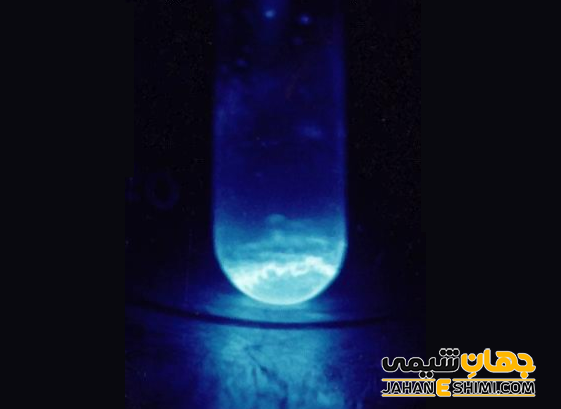
عنصر اینشتینیم، فلزی پرتوزا و رادیواکتیو است که در تاریکی به رنگ آبی می درخشد. این عنصر یازدهمین عضو از عناصر سری اکتینید ها (بلوک- f) محسوب می شود كه تنها به صورت مصنوعي توليد شده است. اینشتینیم فلزی به رنگ سفید- نقره ای است و مانند سایر اکتنید ها نسبتا واکنش پذیر می باشد. همانطور که بیان شد، حالت اکسیداسیون سه ظرفیتی آن در جامدات و محلول های آبی (رنگ صورتی کم رنگ)، پایدار ترین حالت است. البته توجه داشته باشید که وجود انیشتینیوم دو ظرفیتی نیز به ویژه در فاز جامد، ثابت شده است.
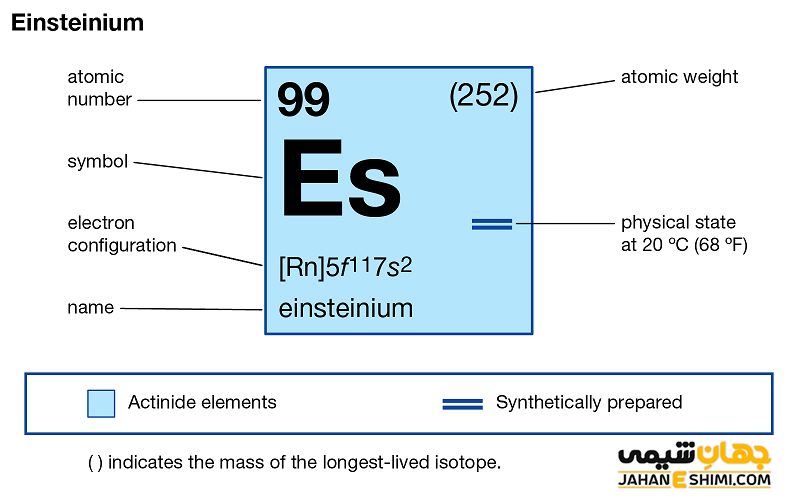
خصوصیات قابل توجه اینشتینیم از ساختار اتمی آن ([۸۶Rn] 5f۱۱۷s۲) ناشی می شود. همان طور که مشخص است، در این عنصر زیر لایه f در حال پر شدن است. این عنصر نیز مثل عناصر لانتانید ها و اکتینید ها و به واسطه آرایش الکترونی که دارد، در دسته فلزات واسطه داخلی (Inner Transition Metals) قرار می گیرد. در این دسته از عناصر، الکترون های متمایز کننده در زیر لایه های F(n-2) لایه ظرفیت که در واقع تراز های درونی تر هستند قرار می گیرند. به همین دلیل، به عناصر واسطه داخلی معروف می باشند. این عناصر جزء عنصر های فلزات واسطه قرار می گیرند. فلزات واسطه در حقیقت بین فلزات قلیایی خاکی و عناصر گروه بور در جدول تناوبی قرار گرفته اند. به عناصر واسطه، عناصر گروه B نیز گفته می شود.
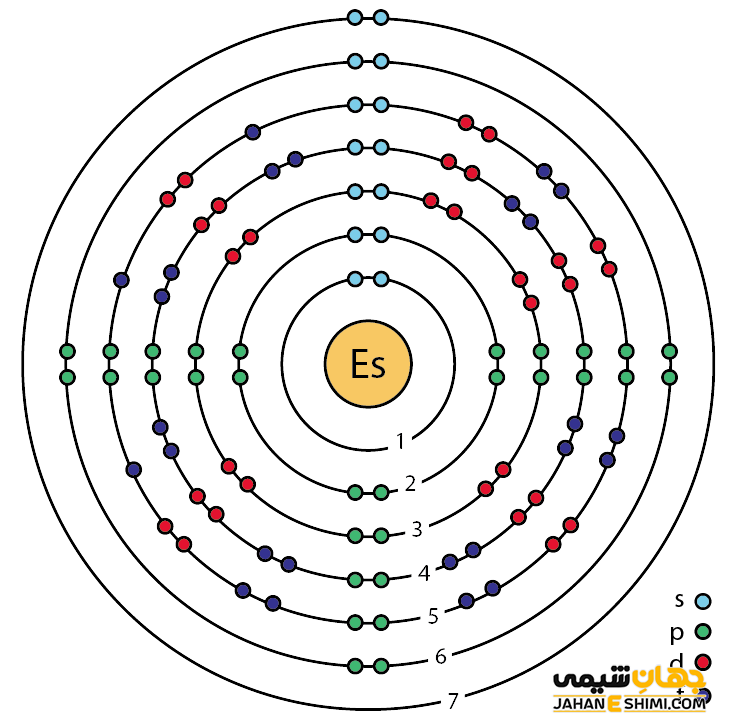
با توجه به آرایش الکترونی مشخص است که تعداد زیادی الکترون در دورترین لایه الکترونی اینشتینیم وجود دارد. پس می تواند در ترکیبات به صورت کاتیون های مختلف ظاهر شود. حالت اکسیداسیون آن بیشتر ۳+ است. از این رو می تواند در سه پیوند کووالانسی شرکت کند. به عبارت دیگر، بیشتر ترکیبات اینشتینیم سه ظرفیتی می باشند.
خواص ویژه اینشتینیوم
- حالت فیزیکی آن در دمای ۲۵ درجه سلسیوس و فشار ۱ اتمسفر به صورت جامد است.
- دمای ذوب و دمای جوش این عنصر به ترتیب ۸۶۰ و ۹۹۶ درجه سانتی گراد است.
- عنصر اینشتینیم پارا مغناطیس است.
- ساختار بلوری آن به شکل مکعبی وجوه پر یا ساختار مکعبی مرکز سطحی (FCC) است.
- این عنصر آلوتروپ ندارد.
- جرم اتمی اینشتینیم برابر با ۲۵۲ g/mol است.
- چگالی آن نیز برابر با ۸.۸۴ g/cm۳ می باشد.
- شعاع اتمی آن نیز برابر با ۱۸۶ pm تخمین زده می شود.
- یون های اینشتینیم معمولا اعدد اکسایش برابر با اعداد ۰، +۲، +۳ و +۴ دارند. اعداد اکسایش ۰ و +۳ متداول تر می باشند.
- اولین انرژی یونیزاسیون آن برابر با ۶۱۹ kJ/mol است.
اکتینید ها
کلمه اکتینید (Actinide) به معنای شبیه اکتینیوم است که به طور کلی با نماد شیمیایی An نمایش داده می شود. این گروه شامل ۱۵ عنصر شيميايي (عدد های اتمی ۸۹ تا ۱۰۳) است که خواص شيميايي مشابهي دارند. همانطور که واضح است، نام این سری از عناصر، از عنصر آکتینیوم برگرفته شده است. بنابراین، خواص شیمیایی این عناصر شبیه به عنصر اکتینیوم است. این گروه از عناصر با فلز اکتینیوم آغاز و به فلز لارنسیوم ختم می شود. به دلیل کمبود جا در جدول تناوبی عناصر و از آن جهت که نظم و ترتیب جدول بهم نریزد، این گروه از عناصر در یک ردیف ۱۴ تایی در پایین جدول و زیر سری لانتانید ها قرار دارد.
در این دسته از عناصر، زیر لایه ۵ اف عناصر در حال پر شدن است. تراز های انرژی ۵f و ۶d بسیار به هم نزدیک هستند. پس نمی توان با قطعیت گفت که در هنگام وارد شدن الکترون ها در عناصر مختلف این سری، اول کدامیک از این تراز ها پر می شود. اما به طور کلی، پر شدن تراز ها در این ردیف از عناصر به ترتیب ۵f و بعد ۶d می باشد. لازم به ذکر است که تمامی اکتینید ها به جز فلز اکتینیم جز بلوک f جدول تناوبی هستند. عنصر اکتینیم جز عناصر بلوک d جدول تناوبی محسوب می شود، اما خواص آن شبیه به چهارده اکتینید دیگر است.
خواص ویژه اکتینید ها
از عنصر چهارم این سری به بعد که به عناصر ترانس یا ترا اورانیوم مشهورند، اغلب در طبیعت پیدا نمی شوند. تمامی اکتینید ها هسته ناپایدار دارند، بنابراین جز عناصر پرتوزا محسوب می شوند. این عناصر، معمولا فلزاتی متراکم، نرم، انعطاف پذیر، چگالی بالا و الکتروپوزیتیو هستند. برخی از آنها با چاقو به راحتی برش می خورند. معمولا خاصیت پارامغناطیسی نشان می دهند و ممکنست آلوتروپ های زیادی تشکیل دهند. این فلزات در دمای اتاق جامد بوده و در هوا، خود به خودی آتش می گیرند. با عناصر گروه هالوژن ها، کالکوژن ها و یا کربن (تشکیل ترکیبات اورگانو اکتینید) واکنش می دهند. همچنین با آب جوش و اسید های رقیق، گاز هیدروژن آزاد می نمایند. توجه کنید که برای مطالعه اکتینید ها، ساختار هسته عناصر نسبت به آرایش الکترونی آنها از اهمیت بیشتری برخوردار است.
دقت کنید که اکتنيد ها نسبت به سری عناصر لانتانيد ها، شباهت رفتاري کمتري را نشان می دهند. اما شیمی اکتینید ها در مقایسه با شیمی لانتانید ها بسیار پیچیده تر است. زیرا عناصر سری اکتینید ها چندین حالت اکسایش مختلف نشان می دهند. بعد از عنصر امیرسیوم، حالت اکسایش عمده برای این سری از عناصر، حالت اکسایش سه است. از این رو، این دسته از عناصر رفتاری شبیه عناصر گروه لانتانید ها نشان می دهند.
ایزوتوپ های عنصر اینشتینیم
همانطور که می دانید ایزوتوپ های یک عنصر، در تعداد نوترون ها با یکدیگر متفاوت اند. عنصر اینشتینیوم ایزوتوپ های فراوانی دارد. نخستین ایزوتوپ شناسایی شده آن، رادیو ایزوتوپ ۲۵۳Es است که در سال ۱۹۵۲ میلادی کشف و ردیابی شد. از آنجاییکه اینشتینیوم، عنصری مصنوعی می باشد، بنابراین ایزوتوپ پایدار ندارد. همانطور که گفته شد، این عنصر به صورت سنتزی و در رآکتور های هسته ای تولید شده است. در نتیجه نمی توان برای آن جرم اتمی استاندارد تعریف کرد. ۱۸ ایزوتوپ پرتوزا از عنصر اینشتینیم شناسایی شده است. رادیوایزوتوپ ۲۵۲Es پایدار ترین ایزوتوپ اینشتینیوم با نیمه عمر ۴۷۱.۷ روز یا تقریبا ۱.۲۹۳ سال است. ایزوتوپ های رادیواکتیو این عنصر دارای جرم های اتمی در محدوده ۲۴۰ تا ۲۵۷ amu می باشند.
بعد از رادیوایزوتوپ ۲۵۲Es، رادیو ایزوتوپ ۲۵۴Es با نیمه عمر ۲۷۵.۷ روز، رادیو ایزوتوپ ۲۵۵Es با نیمه عمر ۳۹.۸ روز، رادیو ایزوتوپ ۲۵۳Es با نیمه عمر ۲۰.۴۷ روز از جمله ایزوتوپ های پایدار اینشتینیوم می باشند. بقیه ایزوتوپ های رادیو اکتیو آن، نیمه عمری کمتر از ۴۰ ساعت دارند. لازم به ذکر است که بیشتر آنها حتی نیمه عمری کمتر از ۳۰ دقیقه دارند. علاوه بر آن، اینشتینیوم دارای سه حالت متا (m) نیز می باشد.

کاربرد های عنصر اینشتینیم
عنصر اینشتینیم خیلی کم کاربردی خارج از پژوهش های علمی و تحقیقاتی دارد. هدف این تحقیقات در حقیقت تولید عناصر ترا اورانیم و ترا اکتینید های بالاتر است. به عنوان مثال، از رادیوایزوتوپ اینشتینیم- ۲۴۹ به عنوان فلز هدف به منظور تولید اکتنید های قوی تر همچون لورانسیم بهره می برند. ایزوتوپ رادیواکتیو اینشتینیم- ۲۵۳ نیز جهت تولید عنصر مندلیفیم (عنصر ۱۰۱) مورد استفاده قرار گرفته است. رادیوایزوتوپ انیشتینیوم- ۲۵۴ به عنوان نشانگر کالیبراسیون در طیف سنج آنالیز شیمیایی (آنالیزگر سطح پراکنده آلفا) کاوشگر ماه سنج Surveyor 5 استفاده شده است.

ترکیبات عنصر اینشتینیم
عنصر اینشتینیم به راحتی می تواند با اکسیژن، گوگرد و هالوژن ها واکنش دهد. در نتیجه اکسید، سولفید و هالید ها را تولید نماید. از جمله ترکیبات عنصر شماره ۹۹ جدول تناوبی می توان به موارد زیر اشاره کرد.
- تری اکسید دی اینشتینیم (Es۲O۳)
- سولفید اینشتینیم (Es۲S۳)
- تری فلوئورید اینشتینیم (EsF۳)
- نیترات اینشتینیم (Es(NO۳)۳)
- تری کلرید اینشتینیم (EsCl۳)
- کربنات اینشتینیم (Es۲(CO۳)۳)
- تری برمید اینشتینیم (EsBr۳)
- فسفات اینشتینیم (EsPO۴)
- تری یدید اینشتینیم (EsI۳)
- سولفات اینشتینیم (Es۲(SO۴)۳)
خطرات اینشتینیوم بر روی سلامتی انسان
عنصر اینشتینیوم نقش زیست شناختی مشخصی ندارد، اما به دلیل پرتوزا بودن، سمی محسوب می شود. بنابراین در هنگام کار با آن، باید مراقب بود. بیشتر داده ها و اطلاعات موجود درباره سمیت عنصر برکلیوم از تحقیقات بر روی حیوانات نشات گرفته است. به عنوان مثال، بعد از مصرف انیشتینیوم توسط موش ها، حدود ۶۵ درصد به استخوان ها، ۲۵ درصد به ریه ها، ۰/۰۳۵ درصد به بیضه ها، ۰/۰۱ درصد به تخمدان ها می رود. در حدود ۱۰ درصد نیز دفع می شود. در تمامی این اندام ها، انیشتینیوم ممکن است باعث سرطان شود.