
عنصر نوبلیم (Nobelium) با نماد شیمیایی No، یکی از عناصر شیمیایی جدول مندلیف است که عدد اتمی آن ۱۰۲ می باشد. این عنصر در حقیقت صد و دومین عنصر از جدول تناوبی عناصر بوده که در گروه IIIB و تناوب هفتم جدول تناوبی قرار گرفته است. عنصر نوبلیم یک فلز واسطه (Transition Metals) رادیواکتیو و از عناصر مصنوعی گروه اکتینید ها است. این فلز با عناصر اسکاندیم (Sc)، ایتریم (Y) و لانتان (La)، در گروه سه واسطه جدول تناوبی عناصر قرار دارد. نوبلیم در واقع عنصری است ترانزورانیک (یعنی عدد اتمی بالاتری نسبت به اورانیوم دارد). در ادامه این مقاله در نشریه جهان شیمی فیزیک به بررسی عنصر نوبلیوم پرداخته می شود. لطفا با ما همراه باشید.
فهرست مطالب
تاریخچه کشف عنصر نوبلیم
کشف عنصر نوبلیم بحث برانگیز بوده است. زیرا کشف آن توسط گروه های مختلفی از سوئد، ایالات متحده آمریکا و اتحاد جماهیر شوروی ادعا شده بود. برای نخستین بار در سال ۱۹۵۶ میلادی، گروهی از محققان به سرپرستی گئورگی فلروف (Georgy Nikolayevich Flyorov) در موسسه انرژی اتمی مسکو، عنصر پلوتونیم را با اکسیژن بمباران کردند. بدین صورت توانستند اتم های عنصر ۱۰۲ را به صورت ایزوتوپ ۲۵۲ بدست آوردند. اما این گروه موفق به گزارش این کشف نشدند.
لازم به ذکر است که عنصر نوبلیم برای اولین بار در سال ۱۹۵۷ میلادی، توسط موسسه نوبل در استکهلم سوئد نامگذاری شد. این موسسه ادعا کرده بود که توانسته است این عنصر را برای نخستین بار سنتز کند. آنها گزارش دادند که عنصر کوریم را با یون های کربن ۱۳ به مدت بیست و پنج ساعت در فواصل نیم ساعته بمباران کرده اند. نادرستي این ادعا بعد ها مشخص شد و دانشمندان سوئدی حرف و ادعای خود را پس گرفتند.
بعد از آن تصور مي شد كه عنصر نوبلیم را گروه دانشمندان آمریکایی دانشگاه كاليفرنيا بركلي، یعنی، گلن سیبورگ (Glenn T. Seaborg)، توربیورن سیکلند (Torbjørn Sikkeland)، جان والتون (John R. Walton) و آلبرت غیورسو (Albert Ghiorso) در سال ۱۹۵۸ میلادی با استفاده از یک تکنیک بازگشت پذیری جدید كشف كرده باشند. در این روش از یک شتاب دهنده خطی یون سنگین به منظور بمباران کردن عنصر کوریوم (۹۵ درصد کوریم ۲۴۴ و ۴/۵ درصد کوریم ۲۴۶) با یون های کربن ۱۲ و کربن ۱۳ جهت تولید عنصر ۱۰۲ استفاده شد. دقت داشته باشید که نام عنصر توسط این گروه تغییر نکرد.

نامگذاری عنصر نوبلیم
در همین زمان، آزمایشاتی در سال های ۱۹۵۸ و ۱۹۶۰ میلادی در دوبنای شوروی و با هدف سنتز عنصر ۱۰۲ انجام شد. بنابراین اولویت اکتشاف و نامگذاری این عنصر در میان دانشمندان شوروی و آمریکایی مورد بحث بود. لازم به ذکر است که اولین گزارش غیر قابل انکار و کامل از کشف نوبلیوم مربوط به سال ۱۹۶۶ میلادی توسط موسسه مشترک تحقیقات هسته ای در دوبنا (در آن زمان در اتحاد جماهیر شوروی بود) است. در نهایت و در سال ۱۹۹۲ میلادی، انجمن بين المللي شيمی محض و كاربردی (آيوپاك) امتیاز کشف نوبلیوم را به دانشمندان روسی در دوبنا واگذار کرد و به این مجادله ها پایان داد. نام این عنصر به افتخار دانشمند مبتكر و پيشگام سوئدي یعنی آلفرد نوبل (Alfred Nobel)، بر روی آن گذاشته شده است. این دانشمند کاشف دینامیت و بنیانگذار جایزه نوبل است.

پیدایش و منابع عنصر شماره ۱۰۲ جدول تناوبی
عنصر نوبلیم به طور طبیعی وجود ندارد و در پوسته زمین یافت نشده است. این عنصر در حقیقت به دست بشر ساخته شده است. ایزوتوپ های نوبلیوم اغلب از طریق بمباران اهداف اکتینیدی مانند عناصر اورانیوم، کوریم، پلوتونیوم، کالیفرنیوم و یا اینشتینیم سنتز می شوند. به طور کلی می توان گفت که این عنصر از طریق بمباران يك ايزوتوپ کوریم با هسته هاي يك ايزوتوپ كربن سنتز می شود.

ویژگی های فیزیکی و شیمیایی عنصر نوبلیم
همانطور که بیان شد، عنصر نوبلیم تاکنون تنها به مقدار بسیار نا چیزی توليد شده است. از این جهت، اطلاعات اندكي درباره شكل ظاهری و یا خواص شیمیایی آن وجود دارد. با این وجود، تعدادی پیش بینی و نتایج تجربی اولیه در مورد خواص آن انجام شده است. نوبلیم در حقیقت عنصری خاكي كمياب و فلزی پرتوزا و رادیواکتیو است. آزمایشات شیمی تایید کرده اند که عنصر نوبلیوم به عنوان همولوگ سنگین تری نسبت به عنصر ایتربیوم در جدول تناوبی رفتار می کند. این عنصر دهمین عنصر فرا اورانیومی است و عضو ما قبل آخر سری اکتینید ها است.
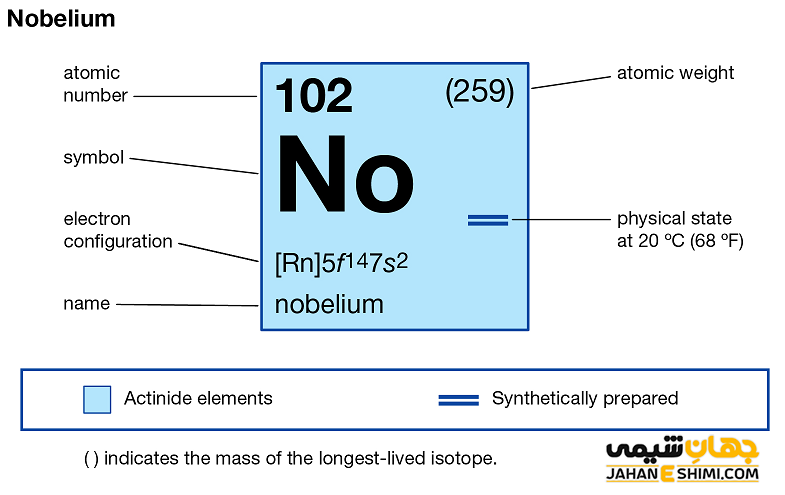
خصوصیات نوبلیم از ساختار اتمی ([۸۶Rn] 5f۱۴7s۲) آن ناشی می شود. همان طور که آرایش الکترونی نشان می دهد، زیر لایه f در حال پر شدن است. این عنصر نیز همچون سایر عناصر سری لانتانید ها و اکتینید ها و به واسطه آرایش الکترونی که دارد، در دسته فلزات واسطه داخلی (Inner Transition Metals) قرار می گیرد. در این دسته از عناصر، الکترون های متمایز کننده (الکترون های لایه والانس) در زیر لایه های F(n-2) لایه ظرفیت که در حقیقت تراز هایی درونی تر محسوب می شوند، قرار دارند. از این رو به آنها، عناصر واسطه داخلی می گویند. عناصر واسطه داخلی خود زیر مجموعه عناصر واسطه می باشند. فلزات واسطه در جدول تناوبی میان فلزات قلیایی خاکی و عناصر گروه بور قرار گرفته اند. عناصر واسطه، عناصر گروه B نیز نامیده می شوند.
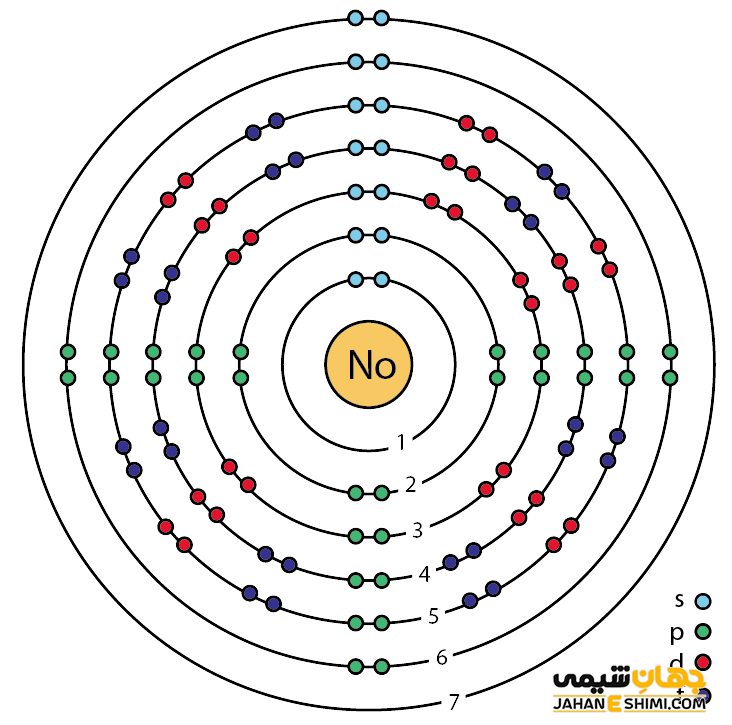
با توجه به آرایش الکترونی عنصر نوبلیم مشخص است که تعداد زیادی الکترون در دورترین لایه الکترونی آن وجود دارد. پس انتظار می رود که در ترکیبات به صورت کاتیون های مختلف ظاهر شود. اما اغلب می تواند در دو یا سه پیوند کووالانسی شرکت کند.
خواص ویژه نوبلیوم
لازم به ذکر است که شیمی عنصر نوبلیوم به طور کامل مشخص نیست و تنها در محلول آبی شناخته شده است. بنابراین پیش بینی شده بود که نوبلیم در فاز آبی می تواند، حالت های اکسیداسیون +۳ یا +۲ را به خود بگیرد که حالت اکسیداسیون +۲ پایدار تر است، در حالیکه نگه داشتن نوبلیوم در حالت +۳ دشوار است. این پیش بینی ها بعدا تایید شد. به عبارت دیگر، نوبلیوم تنها عنصر بلوک f، شناخته شده است که حالت +۲ برای آن رایج ترین و پایدار ترین حالت ممکن در محلول آبی است. این اتفاق به دلیل شکاف انرژی بزرگ میان اوربیتال های 5f و 6d در انتهای سری اکتینید ها رخ می دهد. از دیگر ویژگی های آن می توان به موارد زیر اشاره کرد.
- حالت فیزیکی آن در دمای ۲۵ درجه سلسیوس و فشار ۱ اتمسفر احتمالا به صورت جامد است.
- دمای ذوب این عنصر، ۸۲۷ درجه سانتی گراد پیش بینی می شود. در حالیکه دمای جوش آن نا شناخته است.
- خاصت مغناطیسی عنصر نوبلیم نیز نا مشخص است.
- انتظار می رود که ساختار بلوری آن به شکل مکعبی وجوه پر یا ساختار مکعبی مرکز سطحی (fcc) باشد.
- این عنصر احتمالا آلوتروپ ندارد.
- جرم اتمی نوبلیم برابر با ۲۵۹ g/mol است.
- چگالی آن نیز برابر با ۹.۹ g/cm۳ پیش بینی می شود.
- شعاع اتمی آن نیز تخمین زده نشده است.
- یون های نوبلیم معمولا اعدد اکسایش برابر با اعداد ۰، +۲ و +۳ دارند. اعداد اکسایش ۰ و +۲ متداول تر می باشند.
- اولین انرژی یونیزاسیون آن برابر با ۶۳۹ kJ/mol است.
اکتینید ها
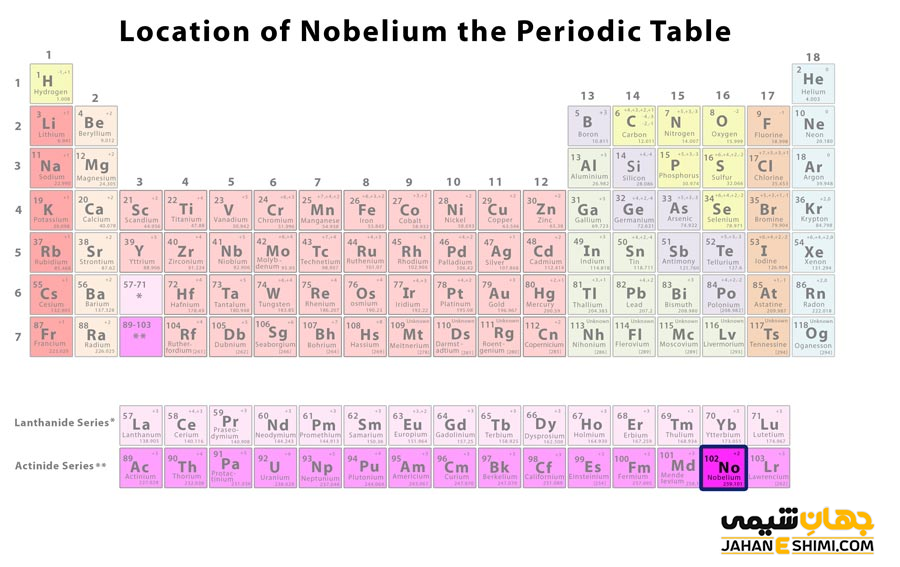
عنصر نوبلیوم چهاردهمین عضو از عناصر سری اکتینید ها (بلوک- f) محسوب می شود كه به صورت مصنوعي سنتز شده است. کلمه اکتینید (Actinide) به معنای شبیه اکتینیوم است که با نماد شیمیایی An نمایش داده می شود. همانطور که واضح است، نام این سری از عناصر، از عنصر اکتینیوم گرفته شده است. این گروه شامل ۱۵ عنصر شيميايی (عدد های اتمی ۸۹ تا ۱۰۳) است که خواص شيميايي مشابه ای (شبیه به عنصر اکتینیوم) دارند. این گروه از عناصر با فلز اکتینیوم آغاز و به فلز لارنسیوم ختم می شود. به دلیل کمبود جا در جدول تناوبی عناصر و از آن جهت که نظم و ترتیب جدول بهم نخورد، این گروه از عناصر در یک ردیف ۱۴ تایی در پایین جدول و زیر سری لانتانید ها قرار گرفته است.
در این دسته از عناصر، پوسته 5f آنها در حال پر شدن است. تراز های انرژی 5f و 6d بسیار به هم نزدیک می باشند. پس نمی توان با قطعیت گفت که اول کدامیک از این تراز ها در هنگام وارد شدن الکترون های والانس در عناصر مختلف این سری، پر می شود. اما به طور کلی، پر شدن تراز ها در این ردیف از عناصر به ترتیب 5f و بعد 6d می باشد. لازم به ذکر است که تمامی اکتینید ها به جز فلز اکتینیم جز بلوک f جدول تناوبی هستند. عنصر اکتینیم جز عناصر بلوک d جدول تناوبی محسوب می شود، اما خواص آن شبیه به چهارده اکتینید دیگر است.
خواص ویژه اکتینید ها
از عنصر چهارم این سری به بعد که به عناصر ترانس، فرا یا ترا اورانیوم مشهورند، اغلب در طبیعت وجود ندارند. تمامی اکتینید ها هسته ناپایدار دارند، بنابراین جز عناصر پرتوزا محسوب می شوند. این عناصر، معمولا فلزاتی با چگالی بالا، نرم، متراکم، انعطاف پذیر و الکتروپوزیتیو هستند. تعدادی از آنها با چاقو به راحتی برش می خورند. بیشتر خاصیت پارامغناطیسی نشان می دهند. این فلزات در دمای اتاق معمولا جامد هستند. در هوا، خود به خودی آتش می گیرند. با عناصر گروه هالوژن ها، کالکوژن ها و یا کربن (تشکیل ترکیبات اورگانو اکتینید) درگیر واکنش می شوند. به علاوه، با آب جوش و اسید های رقیق، گاز هیدروژن آزاد می کنند. توجه داشته باشید که به منظور مطالعه اکتینید ها، ساختار هسته عناصر نسبت به آرایش الکترونی آنها، اهمیت بیشتری دارد.
لازم به ذکر است که آکتنيد ها نسبت به عناصر سری لانتانيد ها، شباهت رفتاری کمتری را نشان می دهند. اما شیمی آنها در مقایسه با شیمی لانتانید ها بسیار پیچیده تر است. زیرا عناصر سری اکتینید ها اغلب چندین حالت اکسایش مختلف نشان می دهند. بعد از عنصر امرسیوم در این ردیف از عناصر، حالت اکسایش عمده برای آنها، حالت اکسایش سه است. از این رو، این دسته از عناصر رفتاری شبیه عناصر گروه لانتانید ها نشان می دهند.
ایزوتوپ های عنصر نوبلیم
همانطور که می دانید ایزوتوپ های یک عنصر، تنها در تعداد نوترون ها با یکدیگر تفاوت دارند. عنصر نوبلیوم ایزوتوپ های زیادی دارد. نخستین ایزوتوپ شناسایی شده آن، رادیو ایزوتوپ ۲۵۴No است که در سال ۱۹۶۶ میلادی کشف و ردیابی شد. از آنجاییکه عنصر نوبلیوم، عنصری مصنوعی می باشد، بنابراین ایزوتوپ پایدار ندارد. این عنصر در حقیقت به صورت سنتزی و در رآکتور های هسته ای تولید شده است. در نتیجه نمی توان برای آن جرم اتمی استاندارد تعریف کرد. ۱۳ ایزوتوپ پرتوزا از عنصر نوبلیم شناسایی شده است. رادیو ایزوتوپ ۲۵۹No پایدار ترین ایزوتوپ نوبلیوم با نیمه عمر ۵۸ دقیقه است. دقت داشته باشید که ایزوتوپ رادیواکتیو ۲۵۵No با نیمه عمر ۳/۱ دقیقه، بیشتر در شیمی استفاده می شود. زیرا این ایزوتوپ را می توان در مقیاس بزرگتر تولید کرد.
بعد از رادیوایزوتوپ ۲۵۹No و ۲۵۵No، رادیو ایزوتوپ ۲۵۳No با نیمه عمر ۱.۶۲ دقیقه، رادیو ایزوتوپ ۲۵۷No با نیمه عمر ۵۲ ثانیه، رادیو ایزوتوپ ۲۵۴No با نیمه عمر ۵۱ ثانیه، رادیو ایزوتوپ ۲۵۶No با نیمه عمر ۲.۹۱ ثانیه و رادیو ایزوتوپ ۲۵۲No با نیمه عمر ۲.۵۷ ثانیه از جمله ایزوتوپ های پایدار نوبلیوم می باشند. بقیه ایزوتوپ های پرتوزای آن، نیمه عمری کمتر از یک ثانیه دارند. لازم به ذکر است که بیشتر آنها حتی نیمه عمری کمتر از میلی ثانیه دارند. علاوه بر آن، نوبلیوم دارای چهار حالت متا (m) نیز می باشد. ایزوتوپ های رادیواکتیو این عنصر دارای جرم های اتمی در محدوده ۲۴۹ تا ۲۶۰ amu می باشند.
کاربرد های عنصر نوبلیم
از آنجاییکه عنصر شماره ۱۰۲ جدول تناوبی به میزان بسیار ناچیز سنتز شده است، بنابراین خیلی کم کاربردی خارج از پژوهش های علمی و تحقیقاتی دارد. به عبارت دیگر، این عنصر شیمیایی به هیچ وجه قابل استفاده در خارج از محیط آزمایشگاه نیست.

ترکیبات عنصر نوبلیم
پیش بینی می شود که عنصر نوبلیم بتواند به راحتی با عناصر اکسیژن، گوگرد و هالوژن ها واکنش دهد. در نتیجه اکسید، سولفید و هالید ها را تولید نماید. از جمله ترکیبات مهم آن می توان به دی کلرید نوبلیم (NoCl۲) و تری کلرید نوبلیم (NoCl۳) اشاره کرد.
خطرات نوبلیوم بر روی سلامتی انسان
از آنجاییکه عنصر نوبلیوم به صورت طبیعی وجود ندارد، پس در پوسته زمین نیز پیدا نشده است. بنابراین می توان گفت که دلیلی برای در نظر گرفتن خطرات سلامتی آن نیز وجود ندارد. به بیان دیگر، عنصر شماره ۱۰۲ جدول تناوبی نقش زیست شناختی مشخصی ندارد، اما به دلیل پرتوزا بودن، سمی محسوب می شود. بنابراین در هنگام کار با آن، باید مراقب بود.




















