
عنصر سلنیوم (Selenium) با نماد شیمیایی Se، یکی از عناصر شیمیایی جدول مندلیف است که عدد اتمی آن ۳۴ می باشد. این عنصر در حقیقت سی و چهارمین عنصر از جدول تناوبی بوده که در گروه XVI و دوره چهارم جدول قرار گرفته است. در واقع عنصر سلنیوم یک نافلز سمی، کمیاب و به رنگ خاکستری است که از عناصر گروه اکسیژن یا کالکوژن می باشد. این فلز با عناصر اکسیژن (O)، گوگرد (S)، تلوریم (Te)، پولونیوم (Po) و لیورمیوم (Lv)، در گروه شانزدهم یا گروه ششم اصلی (VIA) جدول تناوبی قرار گرفته است. در ادامه این مقاله در نشریه جهان شیمی فیزیک به بررسی عنصر سلنیم پرداخته می شود. لطفا با ما همراه باشید.
فهرست مطالب
تاریخچه کشف عنصر سلنیوم
عنصر سلنیوم برای نخستین بار در سال ۱۸۱۷ میلادی، توسط شیمیدانان سوئدی به نام برزلیوس (Jons Jacob Berzelius) و دستیارش گاهن (Johan Gottlieb Gahn) کشف شد. در حقیقت این دو دانشمند در بازدیدی که از یک کارخانه تهیه اسید سولفوریک، واقع در گریپسهولم داشتند، مقدار کمی از رسوبی در اسید سولفوریک پیدا کردند که نیمی از آن قرمز و نیمی دیگر قهوه ای روشن بود. آنها با گرم کردن رسوب مزبور بر روی شعله چراغ، ابتدا متوجه بوی ضعیفی شبیه تربچه شدند. سپس رسوب به شکل یک فلز ناخالص مشابه با سرب و با جلای فلزی تبدیل شد. آنها اعتقاد داشتند که بوی تربچه ناشی از وجود تلوریم در کانی بوده است.
برزلیوس رسوباتی را که طی چند ماه از احتراق گوگرد جهت تولید اسید سولفوریک حاصل شده بودند را جمع آوری کرد. سپس با تجزیه دقیق این رسوبات، نتیجه گرفت که سنگ معدن مزبور دارای فلزی نا شناخته اما با خواصی مشابه خواص تلوریم است. در واقع فلز جدید را به طریقی مشابه با عنصر تلوریوم (که از واژه یونانی سیاره زمین مشتق شده بود) سلنیم نامیدند. نام سلنیوم از واژه یونانی سلنوس (Selene)، به معنی ماه، بر گرفته شده است. به عبارت دیگر، سلنیوم را می توان یکی دیگر از عناصری دانست که شیمیدانان با آن، سال ها قبل از کشف واقعی اش مواجه شده بودند. اما به دلیل پنهان شدنش در پشت سایر عناصر مشابه، در شناسایی آن با شکست مواجه می شدند. سلنیوم در حقیقت سال ها زیر نقاب عناصر گوگرد و تلوریم مخفی مانده بود.

پیدایش و منابع عنصر شماره ۳۴ جدول تناوبی
سلنیوم یک عنصر کمیاب است. این عنصر به صورت گسترده به عنوان یک ماده جامد در پوسته زمین پراکنده شده است. مقدار آن در پوسته زمین در حدود ۰/۰۵ تا ۰/۰۹ میلی گرم در کیلوگرم می باشد. از نظر فراوانی در میان عناصر پوسته زمین، عنصر سلنیوم، شصت و هشتمین عنصر محسوب می شود. این عنصر اغلب در صخره ها و خاک ها پیدا می شود. می توان گفت که این ماده معدنی، در آب، خاک و بعضی از مواد غذایی وجود دارد.
لازم به ذکر است که سلنیم در طبیعت به شکل خالص یافت نمی شود. بلکه بیشتر به شکل سلنید از کانی های سولفیدی مانند پیریت و همرا عناصری همچون نقره، مس، سرب و نیکل بدست می آید. این عنصر در واقع از گل و لای آنودی مس و همچنین گل و لای سربی حاصل از گیاهان، اسید سولفوریک به صورت یک محصول جانبی تولید می شود. به عبارت دیگر، سلنیوم بیشتر به صورت نا خالصی در ترکیبات گوگردی به ویژه در سولفید ها وجود دارد. دقت داشته باشید که روش های فیزیکی و شیمیایی گوناگونی جهت سنتز سلنیوم عنصری استفاده شده است. از جمله این روش ها می توان به تابش فرابنفش، لیتوگرافی، تکنولوژی لیزری و آئروسولی، اولتراسونیک و تکنیک های احیاء فوتوشیمیایی اشاره کرد.

ویژگی های فیزیکی و شیمیایی عنصر سلنیوم
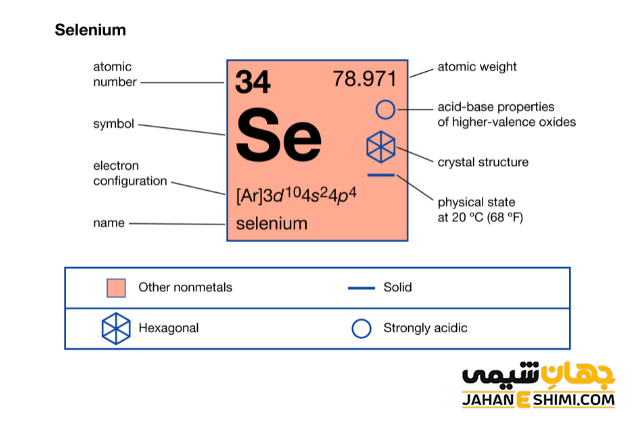
همانطور که گفته شد، عنصر شماره ۳۴ جدول تناوبی متعلق به خانواده اکسیژن (گروه ۶) است. عنصر سلنیوم یک نافلز است. خصوصیات قابل توجه سلنیم از ساختار اتمی آن ([۱۸Ar] 3d۱۰4s۲4p۴) ناشی می شود. همانطور که مشخص است، اوربیتال p لایه آخر در این عنصر در حال پر شدن است. بنابراین این عنصر به بلوک p جدول تناوبی عناصر تعلق دارد. این عنصر دارای دو اوربیتال نیمه پر و یک اوربیتال پر در اوربیتال p خود است. از این رو می تواند در دو پیوند کووالانسی شرکت کند. بنابرابن حالت های اکسیداسیون +۲ و -۲ را خواهد داشت. همچنین با توجه به آرایش الکترونی آن مشخص است که شش الکترون در دورترین لایه الکترونی این عنصر وجود دارد.
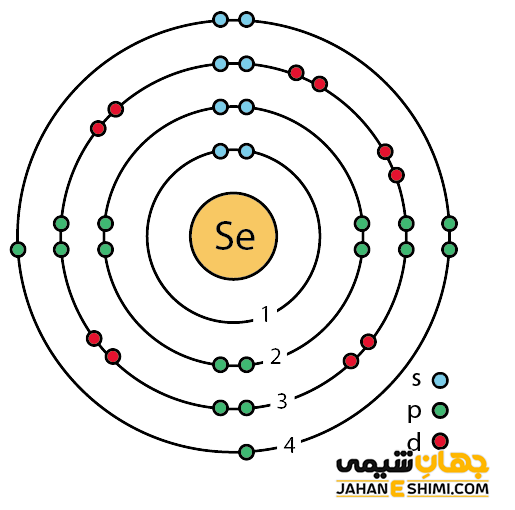
همانطور که گفته شد، سلنیم یک عنصر شیمیایی کمیاب است. این عنصر در گروه کالکوژن، بین عناصر گوگرد و تلوریوم قرار گرفته است. از این رو، خصوصیات شیمیایی آن نیز بین گوگرد و تلوریوم خواهد بود. سلنیم یک نیمه هادی، با هدایت اکسی متریک است. به این معنا که جریان الکتریکی در سلنیوم در یک جهت آسان تر از جهت دیگر جریان می یابد. لازم به ذکر است که همین خصوصیت، سلنیم را دارای ارزشی استثنایی و ویژه برای کاربرد در صنعت کرده است. سلنیم در دمای پایین تر از نقطه جوش، یک نیم رسانای نوع پی (p-type) است. رسانایی سلنیوم نسبت به نور حساس است. یعنی رسانایی آن در صورت مواجهه با نور تا حدودی افزایش پیدا می کند. سلنیوم همچنین اثر فتو ولتیک از خود نشان می دهد. در واقع نور را به الکتریسیته تبدیل می کند.
ویژگی های دیگر عنصر سلنیوم
عنصر سلنیوم به شکل های گوناگون و رنگ های مختلف پیدا می شود. سلنیوم به شکل پودر سلنیم به رنگ قرمز است، در حالت آزمایشگاهی سیاه رنگ است. کریستال شش گوشه سلنیوم نیز به رنگ خاکستری فلزی است. در حالیکه کریستال منو کلینیک آن، به رنگ قرمز تیره می باشد. سلنیوم بیشتر به شکل شبه فلز مانند (هادی جریان الکتریسیته) می باشد و در سلول های نوری کاربرد ویژه دارد.
- حالت فیزیکی آن در دمای ۲۵ درجه سلسیوس و فشار ۱ اتمسفر به صورت جامد است.
- دمای ذوب و دمای جوش این عنصر به ترتیب ۲۲۱ و ۶۸۵ درجه سانتی گراد است.
- عنصر سلنیوم دیا مغناطیس است.
- ساختار بلوری آن به شکل مونوکلینیک (Simple Monoclinic) است.
- این عنصر آلوتروپ دارد. سلنیوم بی شکل قرمز، سلنیوم بی شکل سیاه، سلنیوم مونوکلینیک (تک شیب)، سلنیوم هگزاگونال.
- جرم اتمی سلنیوم برابر با ۷۸.۹۶ g/mol است.
- چگالی آن نیز برابر با ۴.۸۱ g/cm۳ می باشد.
- شعاع اتمی آن نیز برابر با ۱۰۳ pm می باشد.
- یون های سلنیوم معمولا عدد اکسایش برابر با اعداد -۱، -۲، ۰، +۱،+۲ ، +۳، +۴، +۵و +۶ دارند. در حقیقت یک اکسید اسیدی قوی محسوب می شود. اعداد اکسایش -۲، ۰،+۱ ،+۲ ، +۴ و +۶ متداول تر می باشند.
- اولین انرژی یونیزاسیون آن برابر با ۹۴۱ kJ/mol است.
ایزوتوپ های عنصر سلنیم
همانطور که می دانید، ایزوتوپ های یک عنصر، در تعداد نوترون ها با یکدیگر تفاوت دارند. عنصر سلنیم ایزوتوپ های فراوانی دارد. سلنیمی که در طبیعت وجود دارد دارای پنج ایزوتوپ پایدار ۷۴Se(0.89 %)، ۷۶Se(9.37 %)، ۷۷Se(7.63 %)، ۷۸Se(23.77 %) و ۸۰Se(49.61 %) می باشد. دو ایزوتوپ دیگر یعنی ۷۹Se و ۸۲Se(8.73 %) رادیواکتیو می باشند. علاوه بر آن، ۲۳ ایزوتوپ پرتوزای سلنیم نیز شناخته شده است. پایدارترین رادیو ایزوتوپ آن، ۷۹Se با نیمه عمر ۳۲۷ هزار سال است.
کاربرد های عنصر سلنیوم
عنصر سلنیوم کاربرد های بسیار زیادی در صنایع مختلف از جمله صنایع الکترونیک (مرتبط با فتوسل ها و باطری های خورشیدی)، فتوکپی، عینک سازی، رنگ سازی، تولید آفت کش ها، لاستیک سازی، آلياژ های فلزی، افزودنی غذای ماکیان و چهار پایان، نساجی، عکاسی، دارویی (به ویژه در شامپو های ضد شوره و ضد قارچ) و پزشکی کاربرد دارد. به علاوه، رادیوایزوتوپ های آن در طب تشخیصی استفاده می شوند.
همان طور که بیان شد، یک کاربرد سلنیوم در واقع رنگ دادن به عکس ها و تصاویر است. از این رو، به طور گسترده به وسیله کمپانی های عکاسی فروخته می شود. از کاربرد های هنری آن می توان در شدت دادن به طیف رنگ ها به ویژه در تصاویر سیاه و سفید نام برد. همچنین در افزایش طول عمر عکس نیز موثر است. سلنیم همچنین برای پاک کردن رنگ از شیشه ها کاربرد دارد. به راحتی می تواند رنگ سبز را که شامل ناخالصی های آهن دار است، از بین ببرد. این عنصر در قرمز کردن رنگ شیشه و مینا کاری نیز بکار گرفته می شود. علاوه بر آن، عنصر شماره ۳۴ جدول تناوبی به عنوان ماده ضد خش در فرآیند تولید لاستیک های ولکانیزه نیز کاربرد دارد. این عنصر همچنین در فتوکپی نیز مورد استفاده قرار می گیرد.
کاربرد سلنیوم در سلامت انسان
عنصر سلنيوم يكي از املاح معدني كمياب و بسیار ضروري براي بدن انسان ها است. سلنیوم به عنوان یک آنتی اکسیدان عمل می کند و روند پیری را کند می نماید. آنتی اکسیدان ها در حقیقت موادی محسوب می شوند که سلول ها را می توانند از آسیب در برابر رادیکال های آزاد محافظت کنند. رادیکال های آزاد و تنش های اکسیداتیو در حقیقت عامل اصلی سرطان ها و بیماری های قلبی می باشند.
علاوه بر آن، سلنیوم به تولید آنزیمی دیگری در بدن به نام گلوتاتیون پراکسیداز کمک می کند. این آنزیم، ایفا کننده نقشی مهم در دفع مواد زائد و مخرب از بدن انسان ها از فلزت سمی گرفته تا مواد شیمیایی است. از این جهت، بيشترين غلظت سلنیوم در كبد و كليه است. همچنین باعث استفاده بهینه از ویتامین E در بدن می شود. این ویتامین دارای نقشی مهم در تقویت سیستم ایمنی بدن انسان ها است.
این ماده معدنی برای سلامت تیروئید نیز ضروری می باشد. تیروئید مسئول تنظیم هورمون ها، متابولیسم بدن، سلامت سیستم عصبی و سایر موارد است. در واقع غده تیروئید از سلنیم برای تولید هورمون T4 بهره می برد. به علاوه این عنصر در تبدیل هورمون T4 به هورمون T3 نیز نقش مهمی دارد. در حقیقت، یکی از دلایلی که امروزه کم کاری تیروئید (به ویژه در بانوان) بسیار زیاد شده است، کمبود عناصر ید و سلنیم در رژیم غذایی می باشد.

جالب است بدانید که
عنصر معدنی سلنیوم همچنین در کاهش احتمال ابتلا و پیشگیری از پوکی استخوان نقش دارد. در واقع می تواند آثار التهابی آرتروز و درد ها را کاهش دهد. از فواید دیگر این عنصر در بدن می توان به موارد درمان ناباروری مردان، افزایش عملکرد سیستم ایمنی بدن، کاربرد به عنوان عامل ضد التهاب، پیشگیری از سرطان، حفظ جوانی، گر گرفتگی دوران یائسگی، انعطاف بافت ها، معالجه شوره سر و محافظت چشم ها در مقابل بیماری آب مروارید اشاره کرد.
لازم به ذکر است که عوارض کمبود این عنصر در بدن عبارتند از : کم کاری تیروئید، ریزش مو، افزایش کلسترول بد، کاهش عملکرد سیستم ایمنی بدن، بیماری های قلبی، مشکلات مرتبط با پوست و ناخن ها، درد عضلاني، ضعف، بیماری های پارکینسون و آلزایمر، آسم، افسردگی، بی حوصلگی، اضطراب و پرخاشگری. از طرفی دیگر، تعدادی از تحقیقات نشان داده است که کمبود این عنصر می تواند باعث افزایش خطر ابتلا به سرطان پوست و پروستات گردد.
انسان ها در حالت عادی، روزانه نياز به حدود ده تا پانزده میلى گرم سلنیوم دارند. این مقدار مي تواند به وسیله حبوبات، خشکبار، تخم مرغ، فرآورده هاى لبنى به خصوص پنیر و کره ، ماهى، میگو، بادام برزیلی، گردو، جو، یونجه، دانه رازیانه، جینسنگ،تخم آفتابگردان، برگ تمشک، بومادران، سیر، نان سبوس دار، مخمر آبجو، کشمش، صدف دریایی، برنج قهوه ايی، جوانه گندم، مرغ و گوشت تامين شود. توجه داشته باشید که بادام برزیلی دارای مقدار بسیار زیادی از سلنیوم است، پس در مصرف آن نباید زیاده روی کرد. توجه داشته باشید که بیماران مبتلا به ایدز، استعمال دخانیات، استرس، زندگی در شهر های آلوده، ورزش و فعالیت های سنگین بدنی نیاز به سلنیوم را بالا می برد.

ترکیبات عنصر سلنیوم
همانطور که بیان شد عنصر سلنیوم در گروه عناصر گوگرد و تلوریم قرار گرفته است. بنابراین ترکیباتی مشابه آنها می سازد. توجه داشته باشید که سلنیوم مانند گوگرد در اکسیژن می سوزند. در این صورت دی اکسید سلنیوم یا انیدرید سلنیو (SeO۲) ایجاد می گردد. این فلز همچنین می تواند به راحتی با کربن، هیدروژن و هالوژن ها واکنش دهد و در نتیجه ترکیبات آلی سلنیوم و هالید تولید نماید. از دیگر ترکیبات آن می توان به موارد زیر اشاره کرد.
- سلنیوم تری اکسید، اکسید سلنیوم یا انیدرید سلنیک (SeO۳)
- سلنیوم دی اکسید، اکسید سلنیوم یا انیدرید سلنو (SeO۲)
- سلنیوم دی سولفید (SeS۲)
- سلنیوم هگزا سولفید (Se۲S۶)
- سلنید هیدروژن یا سلنوز هیدروژن (H۲Se)
- سلنیوم هگزا فلوئورید (SeF۶)
- سلنیوم تترا کلرید (SeCl۴)
- سلنیوم مونوکلرید (Se۲Cl۲)
- سلنیوم تترا فلوئورید (SeF۴)
- سلنیوم دی کلرید (TeCl۲)
- اسید سلنو (H۲SeO۳)
- اسید سلنیک (H۲SeO۴)
- سلنوسیستئین (C۳H۷N۱O۲Se۱)
- واکنشگر ولینس (C۱۲H۱۰P۲Se۴)
خطرات سلنیوم بر روی سلامتی انسان
سلنیوم خالص سمی نمی باشد، اما ترکیبات آن بسیار سمی اند. به عنوان مثال، سلنید هیدروژن بسیار سمی است. در واقع، ترکیبات سلنیوم خواصی همچون آرسنیک دارند. بدن انسان نمی تواند عنصر سلنیوم را بسازد، بنابراین باید از منابع خارجی آن را تامین کند. لازم به ذکر است که مقدار کمی سلنیوم می تواند کمک زیادی به سلامتی بدن انسان کند. در واقع، مقدار کم آن برای فعالیت سلول های بدن لازم است.
اما توجه داشته باشید که مقادیر زیاد این عنصر در رژیم غذایی می تواند بسیار سمی باشد. حتی مکمل های سلنیوم، برای افرادی که در رژیم غذایی خود سلنیوم کافی دارند ممکن است مضر باشد. مثلا مصرف زیاد مکمل های سلنیم (در دوزهای بیش از ۴۰۰ میکروگرم در روز) می تواند باعث مسمومیت کبد، ریزش مو، حالت تهوع، اسهال، خستگی مفرط، لخته شدن خون، تحریک پذیری، از دست دادن ناخن، مو و ناخن شکننده، کاهش وزن، بثورات پوستی، کهیر و خارش، بوی بدن دهان، طعم فلزی در دهان، تغییر رنگ دندان ها، و سایر عوارض گردد.




















