
در علم شیمی، هدایت الکتریکی (Electrical conductivity) یا رسانندگی ویژه الکتریکی به توانایی یک ماده شیمیایی جهت هدایت یا انتقال جریان الکتریکی گفته می شود. این کمیت، یک ویژگی فیزیکی بسیار مهم ماده است. به بیان دیگر، با هدایت الکتریکی می توان توانایی یک ماده شیمیایی را برای عبور جریان الکتریسیته و یا میزان توانایی آن ماده در انتقال جریان الکتریکی را اندازه گیری کرد. در واقع، هدایت الکتریکی بر اساس جریان الکترون ها ساخته شده است. این کمیت، یک خاصیت و ویژگی ذاتی ماده است. بطور کلی، هدایت به قابلیت مواد شیمیایی در انتقال گرما، صدا و یا جریان الکتریسیته گفته می شود. در ادامه این مقاله در نشریه جهان شیمی فیزیک به بررسی هدایت الکتریکی پرداخته می شود. لطفا با ما همراه باشید.
فهرست مطالب
مقدمه
هدايت كننده های جريان الکتریسیته را می توان به سه دسته مختلف تقسيم كرد:
- هدايت كننده های الكتروني: در اين نوع از هدايت كننده ها، الكترون ها عامل انتقال جريان الکتریکی می باشند. از جمله این نوع هدايت كننده ها می توان به فلزات (فلزات قلیایی و قلیایی خاکی)، تعدادی از شبه فلزات و همچنین نافزاتی مانند سيليسيم و گرافيت اشاره کرد.
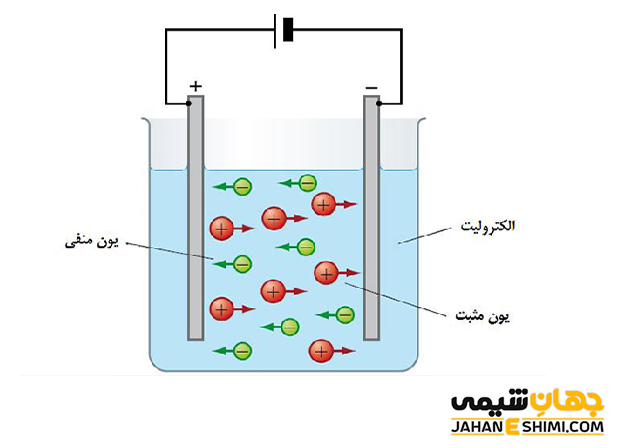
- هدايت كننده های يونی: اين نوع از هدايت كننده ها شامل نمك ها و همچنین تركيبات يوني در حالت مذاب هستند. در اينجا، عامل انتقال جريان الکتریکی، يون های آزاد می باشند.
- هدايت كننده های يون هيدراته: در اين حالت، همانطور که از نام آنها مشخص است، عامل انتقال جريان الکتریکی يون هاي آبپوشيده اند. به بیان دیگر، اين نوع از هدايت كننده ها شامل محلول تركيباتی می باشندكه انحلال آنها در آب باعث توليد يون می شود.
لازم به ذکر است که رسانندگی ویژه الکتریکی در یک محلول بر عهده يون های آن محلول است. بنابراین از جمله عوامل موثر بر هدايت الكتريكي در یک محلول مي توان به موارد مثل نوع ذرات، تعداد ذرات و جنس ذرات اشاره کرد. در یک محلول، نوع ذرات حل شده حتما بايستی به شکل يون باشند. علاوه بر آن، هر چه تعداد يون های داخل محلول بيشتر باشد، رسانندگی ویژه الکتریکی نیز بیشتر خواهد بود. از طرفی دیگر، هر چه تحرك و جنب و جوش يون ها در یک محلول بيشتر باشد، هدايت نیز بهتر انجام می گردد. به همین دلیل، يون های –OH و +H به دلیل کوچکی و تحرک زیاد، یون هايی مناسب برای هدايت الكتريكی محسوب می شوند. در طرف مقابل، آب مقطر به خاطر قدرت پایین در عبور دادن الکترون ها، یک هادی ضعیف جریان الکتریسته به شمار می آید.

هدايت الكتريكی
این کمیت با حرف یونانی سیگما (sigma) یا σ نشان داده می شود. اما توجه داشته باشید که در مهندسی برق با حرف یونانی کاپا (kappa) یا κ نیز مشهور است. همچنین در بعضی موارد ممکن است با نماد گاما (Gamma) یا γ نیز مشخص شود. واحد رسانندگی ویژه الکتریکی در سیستم بین المللی SI بر حسب زیمنس بر متر S/m است. این کمیت همچنین شامل واحد هایی همچون زیمنس بر سانتی متر (S/cm)، میلی زیمنس بر سانتی متر (mS/cm) و میکرو زیمنس بر سانتی متر (μS/cm) و دسی زیمنس بر متر (dS/m) می باشد. البته در صنعت، یکای میکرو زیمنس بر متر (μS/m) کاربرد دارد.
توجه داشته باشید که یکای زیمنس (نماد S)، در حقیقت واحد رسانایی الکتریکی در سیستم SI می باشد. این واحد، به افتخار مخترع و صنعتگر آلمانی یعنی ارنست ورنر فون زیمنس (Ernst Werner von Siemens) نامگذاری شده است. از آنجاییکه رسانایی در حقیقت مفهوم مقابل مقاومت الکتریکی می باشد، گاهی به جای استفاده از یکای زیمنس، از واژه بر عکس اهم که همان مهو است، استفاده می کنند. همانطور که مشخص است، یکای مهو (Mho) از خواندن واحد اهم (Ohm) از آخر به اول بدست آمده است. البته لازم است بدانید که واحد زیمنس به طور رسمی در کنفرانسی در سال ۱۸۸۱ میلادی جایگزین یکای مهو شد.
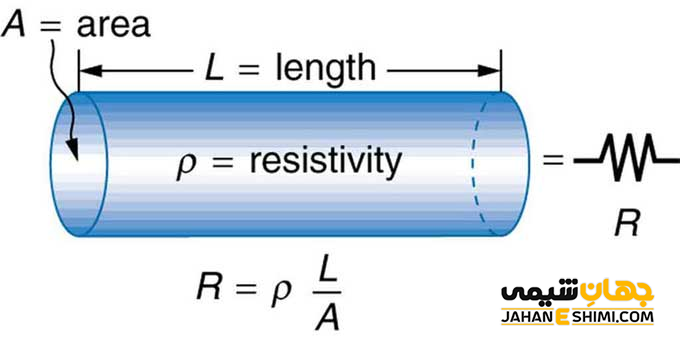
تفاوت مقاومت الکتریکی با هدایت الکتریکی
همانطور که بیان شد، رسانندگی ویژه الکتریکی بر اساس توانایی مواد در هدایت و انتقال جریان الکتریسیته در محدوده معینی تعریف می شود. به عبارت دیگر، هدایت الکتریکی بر اساس رسانایی (توانایی یک ماده در انتقال جریان) می باشد. در حالیکه، مقاومت الکتریکی (Electrical resistivity) نشان دهنده میزان مقاومت ماده مورد نظر در برابر عبور جریان الکتریسیته در محدوده معین است. مقاومت یک جزء به پارامتر های مختلفی مانند طول رسانا، مساحت هادی و مواد هادی بستگی دارد. کمیت مقاومت الکتریکی با حرف یونانی رُ (rho) یا ρ نشان داده می شود. واحد آن در سیستم بین المللی SI بر حسب اهم (Ω) در متر (Ω⋅m) است. هدایت و مقاومت الکتریکی هر دو در حقیقت واحد های قابل تبدیل به همدیگر می باشند. به بیان دیگر، کمیت هدایت الکتریکی برعکس کمیت مقاومت الکتریکی است (σ = 1/ρ).
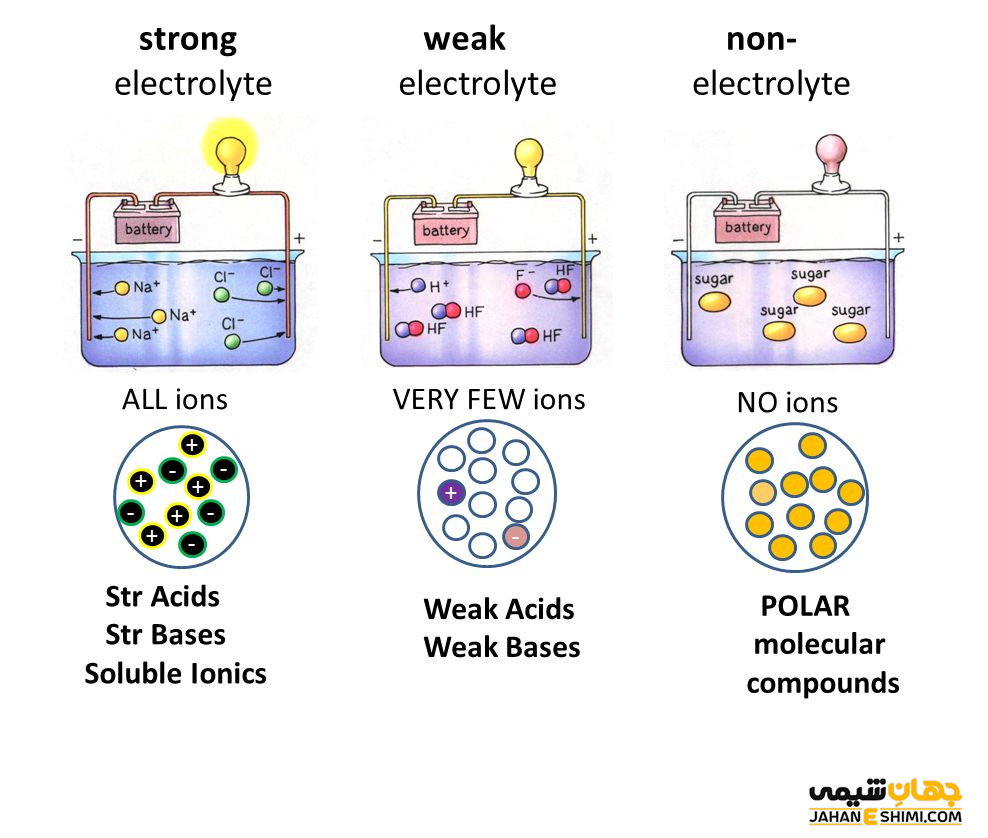
مواد الكتروليت و غير الكتروليت
به طور کلی به مواد شیمیایی كه در محیط آبی، يون توليد می كنند، الكتروليت می گویند. از طرفی دیگر، به موادی كه در آب هیچ يونی توليد نمی كنند، غير الكتروليت گفته می شود. بدین ترتیب، محلول مواد الكتروليت در آب را محلول الكتروليت و همچنین محلول مواد غير الكتروليت در آب را محلول غير الكتروليت می نامند. دقت داشته باشید که محلول يك ماده در آب در صورتی هادی خوبی برای جريان الكتريسیته خواهد بود که دو ويژگي زیر را داشته باشد:
- به میزان زیادی در آب حل شود.
- بخش عمده ای از ماده حل شده بتواند به يون تبديل گردد.
به بیان دیگر، يونيزه شدن بهتر یک الکتروليت باعث افزايش هدايت الکتريکي خواهد شد. زیرا همانطور که می دانید، عامل تاثیر گذار در هدايت الکتريکي محلول ها، وجود يون ها می باشد. زیرا انتقال بار الکتريکي (هدايت الکتريکي) از طریق یون ها در الکتروليت انجام می شود. با توجه به تعریف مشخص می شود که موادی که به شدت یونیزه شوند، الکترولیت هایی قوی (اسید های قوی و نمک ها) خواهند بود. به همین ترتیب می توان گفت که موادی که در آب به طور کامل یونیزه نمی شوند، در دسته الکترولیت های ضعیف (اسید و بازهای ضعیف) قرار می گیرند.
عوامل موثر در هدايت الکتريکی یک الکتروليت
پارامتر های موثر در هدايت الکتريکی یک الکتروليت عبارتند از: درجه يونيزاسيون الکتروليت، سرعت مهاجرت يون های مختلف، دمای الکتروليت و غلظت الکتروليت. درجه يونيزاسيون اسيد های قوی، باز های قوی و بعضي نمک ها بالا مي باشد. جالب است بدانید که سرعت مهاجرت يون های پروتون و هیدروکسید بسیار بالا است، پس به همين دلیل اسيد ها و باز هايی که در آب به خوبی يونيزه می شوند رسانندگی ویژه الکتریکی بالايي را نشان می دهند.
دمای الکتروليت نیز از عوامل موثر در هدايت الکتريکی است. زیرا در اثر افزايش دما در يک پتانسيل مشخص، اتم ها، مولکول ها و يون های محلول، تحرک بیشتری خواهند داشت که در نهايت باعث افزایش هدايت الکتريکی محلول می شود. علاوه بر موارد گفته شده، غلظت محلول نيز در رسانندگی ویژه الکتریکی موثر است. در واقع، با افزايش غلظت محلول به دلیل افزايش تعداد يون ها، هدايت الکتريکی نیز افزايش مي يابد. اما دقت داشته باشید که با افزايش غلظت، درجه يونيزاسيون کاهش پیدا می کند. بنابراين اگر منحنی رسانندگی ویژه الکتریکی بر حسب غلظت محلول را رسم کنید، در ابتدا افزايش هدايت بر اثر افزايش غلظت محلول مشاهده می شود. زمانیکه تعداد يون های محلول مورد نظر به ماکزيمم مقدار خود برسد، با افزايش بيشتر غلظت محلول، هدايت الکتريکی کاهش می یابد.

سرعت انتقال يون ها
علاوه بر درجه يونيزاسيون، سرعت انتقال يون ها نيز اهميت دارد که به اختلاف پتانسيل بين الکترود ها بستگي دارد. توجه داشته باشید که سرعت واقعي مهاجرت يون ها تحت تاثير مولکول های آب، يون ها و مولکول هاي مجاور نیز قرار دارد. بنابراین جهت اندازه گيری سرعت انتقال يون ها، الکترود ها را در فاصله یک سانتيمتری از یکدیگر قرار می دهند و بین آنها، پتانسيل يک ولت اعمال مي شود. در این صورت سرعت مهاجرت يون مشخص مي گردد. البته، این کمیت به نوع محلول، فشار، دما و غلظت نيز بستگي دارد.
دسته بندی مواد الكتروليت قوی، الكتروليت ضعیف و غير الكتروليت
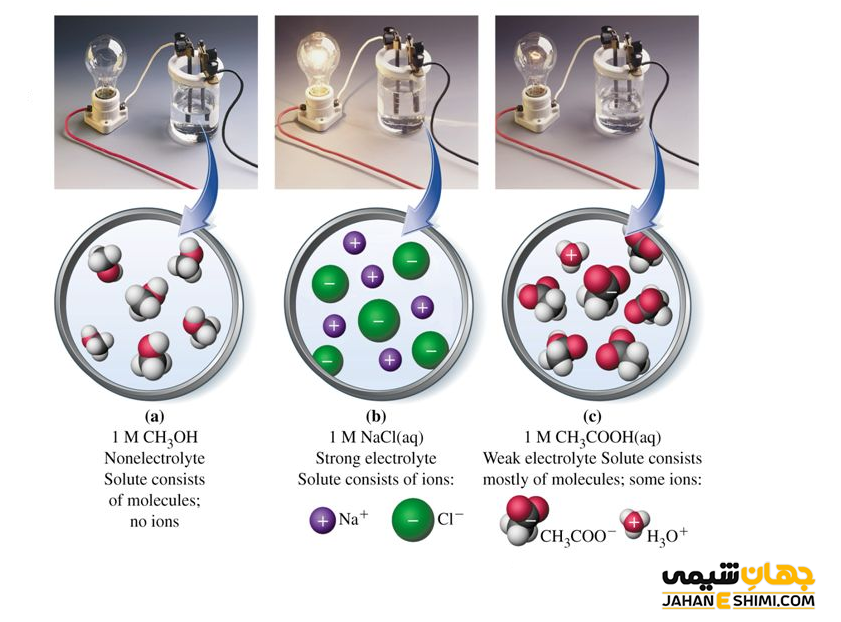
به عنوان نمونه می توان به محلول نمك كلريد سديم در آب اشاره کرد. این محلول در واقع یک الكتروليت قوی محسوب مي شود. زیرا اولا به میزان زيادی در آب حل می گردد. ثانیا، تفكيك يوني آن در آب كامل می باشد. حالا محلول اتانول در آب را در نظر بگیرید. با وجود اينكه اتانول به مقدار قابل توجهي در آب حل می شود، اما انحلال اتانول به شکل مولكولي است. بنابراین هيچ يونی توليد نمی شود و محلول نهایی غير الكتروليت است. بنابراین می توان گفت که موادی به شکل مولكولی در آب حل می شوند (مانند الکل ها و قند ها) در دسته غير الكتروليت ها قرار می گیرند.
از طرف دیگر، محلول آمونياك در آب يك الكتروليت ضعيف محسوب می شود. زیرا با این وجود که مقدار انحلال پذيری آن در آب نسبتا بالاست، اما تفكيك يوني آن پایین می باشد. به عبارت دیگر، تعداد كمی از مولكول های آمونياك محلول در آب به يون تبديل مي گردند. یا مثلا محلول باريم سولفات (BaSO۴) در آب نیز يك الكتروليت ضعيف می باشد. تفكيك يونی آن در آب كامل است، اما ميزان انحلال پذيری بسيار كمی در آب دارد.
الكتروليت های قوی
از نظر دسته بندی محلول ها در رابطه با رسانندگی ویژه الکتریکی آنها مي توان اینطور بیان کرد که بيشترين هدايت الکتريکي را اسيد هايی با درجه يونيزاسيون بالا نشان می دهند. زیرا اسید های قوی، یون پروتون (+H) ايجاد مي کنند که تحرک بالايي دارد. در جایگاه دوم، باز هايی همچون هيدروکسيد سديم يا هيدروکسيد پتاسيم قرار می گیرند. این بازهای قوی، يون هیدروکسید (–OH) ايجاد می کنند که از تحرک بالايی برخوردار است.
درباره محلول های حاوی نمک ها باید توجه داشت که هدايت الکتريکي آنها به درجه يونيزاسيون و تحرک يون هاي مربوطه بستگي دارد. احتمال دارد که بسياری از محلول های نمکی به صورت قوی يونيزه شوند، در حالیکه تحرک يون های آنها پایین باشد. در این صورت رسانندگی ویژه الکتریکی کمی دارند. همچنین ممکن است حالت بر عکس آن وجود داشته باشد. در این حالت، تفكيك يونی محلول نمکی در آب كامل است، اما از طرف دیگر، ميزان انحلال پذيری بسيار پایینی در آب دارد. به عنوان مثال، محلول های زير هادی خوبی برای جريان الکتریسیته محسوب می شوند:
- اسيد های قوی مانند HCl ،HBr ،HI ،HCIO۴ ،H۲SO۴ و HNO۳
- باز های قوی مانند NaOH ،LiOH ،KOH ،RbOH ،CsOH و Ba(OH)۲
- نمك های محلول مانند CaCl ،KBr ،NaCl ،ZnCl۲ و Na۲SO۴
اندازه گیری هدایت الکتریکی در الکترولیت
اندازه گیری رسانندگی ویژه الکتریکی در صنعت و همچنین محیط زیست، یک روش ارزان قیمت و قابل اعتماد به منظور بررسی مقدار یون های موجود در یک محلول محسوب می شود. این کمیت در یک محلول الکترولیتی از طریق اندازه گیری مقاومت محلول میان دو الکترود تیغه ای یا استوانه ای بدست می آید. هر دستگاه هدایت سنج (Electric meter)، EC متر (EC meter) یا کنداکتیومتر، دو الکترود یکسان فلزی پلاتینه شده دارد. این دو الکترود در فاصله معینی از یکدیگر و در یک محفظه شیشه ای (از جنس پیرکس یا شیشه مقاوم دیگر)، موازی هم قرار گرفته اند.
مجموعه این دو الکترود در محفظه شیشه ای، پیل کنداکتومتر نامیده می شود. به منظور اندازه گیری هدایت الکتریکی یک محلول، پیل کنداکتومتر را در محلول مورد نظر قرار می دهند. دستگاه هدایت سنج با فرستادن ولتاژ مناسب بین دو الکترود، هدایت محلول مورد نظر را نشان می دهد. لازم به ذکر است که جهت جلوگیری از بروز پدیده الکترولیز یا همان برقکافت، باید از ولتاژ متناوب با فرکانس زیاد (۶۰ تا ۱۰۰۰ هرتز) در دستگاه استفاده کرد.
امروزه دستگاه های هدایت سنج متنوعی (قلمی یا جیبی، رومیزی و پرتابل) برای محاسبه رسانندگی ویژه الکتریکی وجود دارند. دو نوع اصلی جهت این امر، مدل های الکترودی و یا القایی است. توجه داشته باشید که در بسیاری از دستگاه های کنداکتیومتر جدید، تصحیحات مربوط به دما به صورت خودکار انجام می شود.
کاربرد های هدایت الکتریکی
هدایت سنج ها جهت آنالیز آب خالص، تعیین میزان نمک در آب شور، آزمایشات محیطی جهت تعیین سلامت حوضچه ها، تعیین میزان اسیدیته و تعیین میزان شوری کاربرد دارند. هدایت الکتریکی نقش مهم و ضروری در کاربرد های کیفی آب های مختلف دارد. در واقع از این طریق، شوری آب خروجی تصفیه خانه های فاضلاب را با آب های جاری اطراف مقایسه می کنند. عدم تعادل و تناسب میان مقدار شوری این دو نوع آب، سبب آلودگی های محیطی و همچنین صدمات جبران ناپذیری به حیات گونه های آبزی موجود در آن محیط خواهد شد.

مقدار هدایت الکتریکی در استخر یا حمام های آبکاری نیز اهمیت زیادی دارد. این کمیت در صنایعی همچون جواهر سازی، هوافضا و اتومبیل سازی مورد استفاده قرار می گیرد. همچنین، رسانندگی ویژه الکتریکی جهت اندازه گیری میزان مواد جامد درون محلول (TDS)، نیز استفاده می شود. از طرفی دیگر، اندازه گیری کمیت هدایت الکتریکی خاک، نقشی مهم و اساسی در سلامت و رشد غلات ایفا می کند. به بیان دیگر، با اندازه گیری منظم هدایت، مقدار کمینه یا بیشینه مواد مغذی موجود در خاک (پتاسیم، کلسیم، فسفات ها و نیترات ها) که جهت رشد و نمو گیاهان ضروری هستن را نیز تعیین می کنند.





















سلام ممنون از سایت با کیفیتتون اطلاعاتتون خیلی جامع و عالی بود . من با ذکر منبع در پایان نامه م استفاده کردم. سوالی که دارم اینه که هدایت الکتریکی که عکس مقاومت الکتریکی هست، همون ضریب هدایت الکتریکی آب EC هست یا متفاوته؟ گاها در علوم مختلف صرفا نماد مفهوم تغییر میکنه نه خودش.